查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





研究名称:动态多组学解析不同营养负荷下胰岛与肠道激素分泌及其外周交互
发表期刊:《细胞医学报道》(Cell Reports Medicine,影响因子:10.6)
通讯作者:杨涛、戴皓、付麒
第一作者:汪嘉辰、刘玲
主要作者单位:南京医科大学第一附属医院
该研究首次全面描绘了餐后不同营养成分调控胰岛与肠道激素分泌模式及组织特异性胰岛素抵抗的分子基础,不仅为糖尿病等代谢性疾病的发病机制提供了新的解释框架,也为精准营养干预和个体化治疗策略提供了全新依据。
胰岛与肠道激素在餐后代谢稳态维持中发挥核心作用,然而,空腹与进食状态下激素分泌及其与代谢分子互作网络关系是否不同,以及不同宏量营养素(碳水化合物、蛋白质、脂肪)对胰岛β细胞和α细胞以及肠促胰素分泌的调控机制尚不清晰。
既往研究多聚焦于单一激素或特定营养素的作用,缺乏系统性的整合分析。同时,组织特异性胰岛素抵抗与胰岛功能之间的相互作用尚未被全面揭示。这些空白限制了对糖尿病等代谢性疾病发生发展的理解,也阻碍了精准营养干预策略的制定。
杨涛教授研究团队通过混合餐耐量实验和单一宏量营养素耐量实验,结合非靶蛋白质组学、代谢组学和脂质组学,系统分析了餐后胰岛素、胰高血糖素、GLP-1和GIP的动态分泌轨迹及多组学物质变化特征。
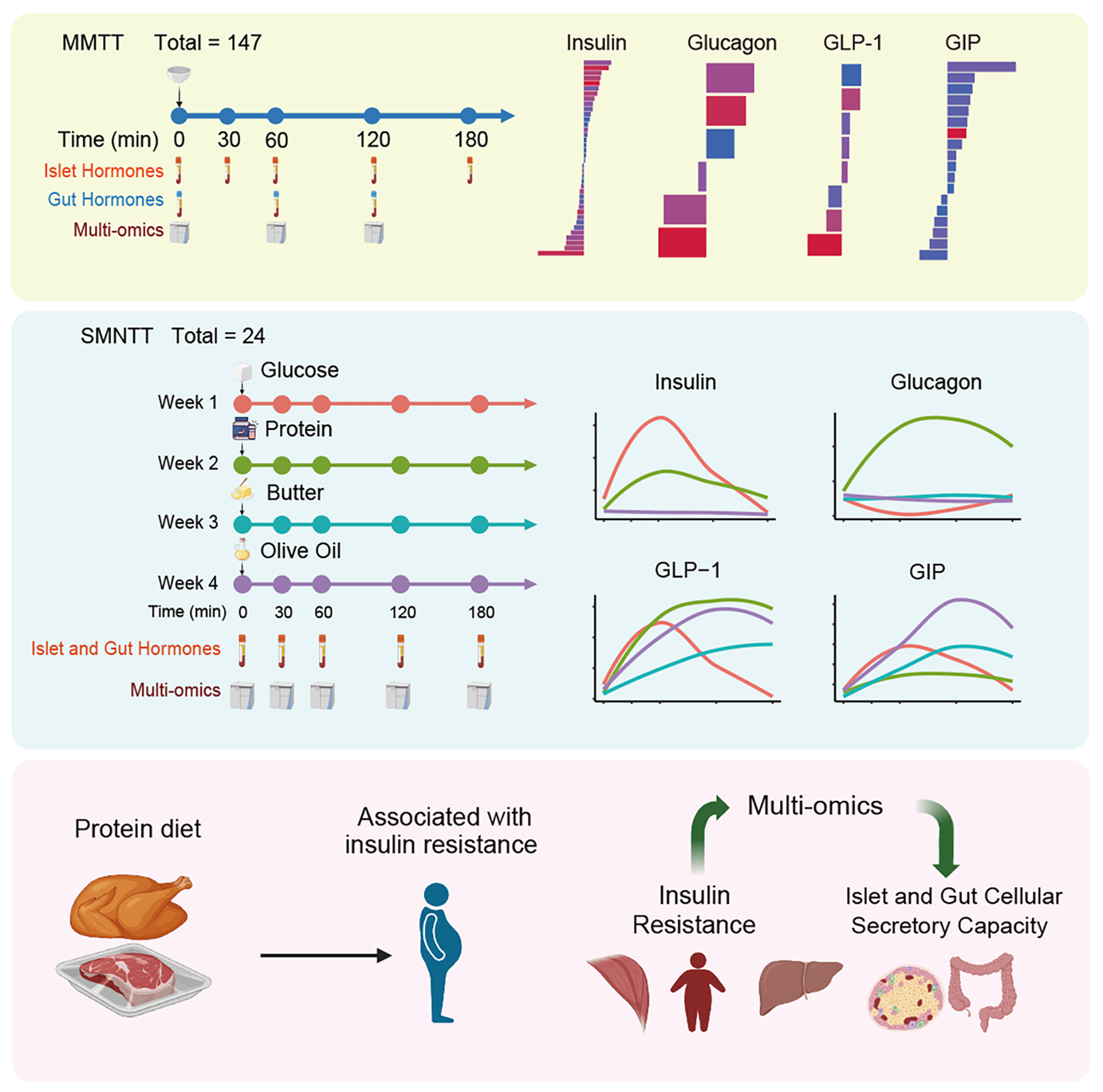
结果发现:胰岛与肠道激素在进食后的反应呈现高度异质性,不同营养素诱导的模式差异显著。葡萄糖最强烈地刺激胰岛素分泌,蛋白质显著增强胰高血糖素和GLP-1反应,而橄榄油则引发最明显的GIP升高。
进一步的分析表明,蛋白与肝脏和肌肉胰岛素抵抗关联最强,黄油则主要与全身性胰岛素抵抗相关。动物实验进一步验证,高蛋白饮食会削弱胰岛素信号并加重胰岛素抵抗,提示饮食结构对代谢稳态有深远影响。
通过多组学整合,研究还发现多种分子在“外周胰岛素抵抗--胰岛细胞分泌”之间发挥关键“桥梁”作用。例如ApoL1、IGFBP-2等蛋白以及甘油三酯、二酰基甘油、溶血磷脂等脂质,可能是调控胰岛β细胞功能的重要介质;而甘油磷脂等代谢物则参与胰岛α细胞功能的调节。
本研究揭示,相比空腹状态,餐后多组学分析更敏感、更全面地反映组织特异性胰岛素抵抗及胰岛和肠道激素分泌水平,不仅为糖尿病等代谢性疾病的发病机制提供了新的解释框架,也为精准营养干预和个体化治疗策略提供了全新依据。
二级教授,主任医师,博士生导师,江苏省人民医院(南京医科大学第一附属医院、江苏省妇幼保健院)内分泌科主任。
现任中华医学会内分泌学分会副主任委员、免疫内分泌学组组长,中国医师协会内分泌代谢科医师分会常委,中国生物化学与分子生物学会代谢专业分会副主任委员,中国老年医学学会内分泌代谢分会副会长。
江苏省医学会糖尿病学分会主任委员、江苏省医学会内分泌学分会前任主任委员、江苏省医师协会内分泌代谢科医师分会候任主任委员。
国际儿童青少年糖尿病协会(ISPAD)年会组委会委员、国际自身免疫糖尿病学会(IDS) 委员,国际胰腺胰岛移植学会(IPITA) 委员。
每一项临床研究都倾注着研究团队的心血结晶。学习过后,您是否有所收获?或有疑问想与主创团队分享?请在评论区留言,期待与您交流!

查看更多