查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过






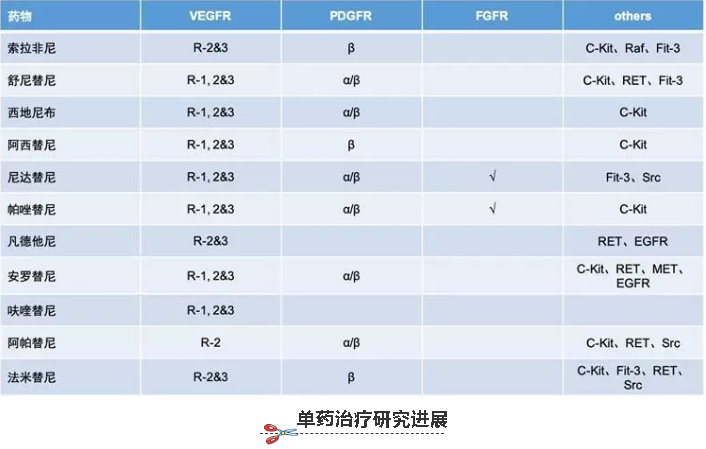
小分子VEGFR-TKI可与胞内段酪氨酸激酶域竞争性结合,抑制其磷酸化过程,阻断细胞下游信号转导通路的激活,从而抑制肿瘤血管生成。与大分子单抗类仅靶向VEGF通路不同,小分子VEGFR-TKI大多还会作用于VEGF、PDGFR和FGFR等多条通路。目前国内外的抗血管生成小分子靶向药及其作用靶点(如图1)所示。
图1 抗血管生成小分子靶向药的作用靶点
小分子多靶点TKI的一线治疗临床探索大多失败,仅少部分研究获得了无进展生存(PFS)或客观缓解率(ORR)的临床获益。然而,小分子多靶点TKI在NSCLC的后线治疗中的临床疗效有所突破。阿帕替尼单药三线治疗晚期NSCLC的Ⅱ期临床研究结果显示与安慰剂相比,阿帕替尼治疗组中位PFS延长2.80个月(4.70个月对1.90个月;HR=0.278;P<0.0001)。呋喹替尼单药治疗晚期非鳞状细胞NSCLC的Ⅱ期临床研究结果显示呋喹替尼治疗组相比安慰剂,PFS显著获益且安全性良好。今年世界肺癌大会(WCLC)公布了呋喹替尼单药三线治疗晚期非鳞状细胞NSCLC的Ⅲ期研究(FALUCA)结果,显示未能达到OS的主要终点;但是与安慰剂相比,呋喹替尼治疗组中位PFS延长2.69个月(3.68个月对0.99个月;HR=0.34;P<0.001);ORR、DCR也显著获益。安罗替尼三线及三线以上治疗晚期NSCLC的Ⅲ期临床研究(ALTER0303)结果显示,与安慰剂相比,安罗替尼组显著延长了OS (9.6个月对比6.3个月, P=0.0018),且PFS (5.4个月对比1.4个月, P<0.0001)、ORR (9.2%对比0.7%, P<0.0001) 和DCR (81.0%对比37.1%,P<0.0001) 等次要终点上也均显著优于对照组,且安罗替尼不良反应可以接受。目前, 安罗替尼已于中国被批准用于晚期NSCLC患者的三线治疗。

尼达尼布联合多西他赛二线治疗晚期NSCLC的Ⅲ期临床研究(LUNG-1研究)结果显示,联合治疗组相比多西他赛组中位PFS显著延长(3.4个月对比2.7个月,HR=0.79,P=0.0019),OS也显著延长 (12.6个月对比10.3个月, HR=0.83, P=0.0359),且不良反应未见显著增加。因此,欧洲药品管理局( EMA) 已经批准尼达尼布联合多西他赛用于晚期肺腺癌的二线治疗。此项研究提示,在二线化疗基础上联合多靶点药物治疗可能是提高疗效的有效途径。目前,关于阿帕替尼联合化疗治疗NSCLC的研究也正在开展,后续前瞻性临床研究的开展具有重要的临床指导意义。

一项晚期NSCLC埃克替尼治疗进展后,采用埃克替尼联合阿帕替尼治疗的回顾性研究结果显示,中位OS未达到,中位PFS为5.33个月(95%CI=3.63~7.03个月),ORR 和 DCR 分别为 11.1%、81.5%。
阿帕替尼一线联合吉非替尼治疗EGFR突变型ⅢB-Ⅳ期非鳞NSCSC研究(ahead-L303研究)的I期临床研究结果显示,在可评估的患者中,ORR为83.3%,DCR为91.7%;阿帕替尼(500mg)+吉非替尼组的中位PFS为19.0个月,阿帕替尼(250mg)+吉非替尼组的中位PFS为13.4个月。研究达到了预期疗效且安全性较好。期待阿帕替尼联合吉非替尼的随机对照Ⅲ期临床研究(NCT02824458)结果最终公布。
呋喹替尼联合吉非替尼治疗EGFR突变晚期NSCLC的Ⅱ期临床研究结果显示,呋喹替尼4mg组联合吉非替尼250mg安全有效。在评估疗效的患者中,ORR为76.5%,DCR为100%。这显示出呋喹替尼联合吉非替尼治疗初步的临床获益,且不良反应可控。
三代EGFR-TKI联合VEGFR-TKI的方案也正在探索。另外,法米替尼联合HS-10296治疗EGFR突变的晚期NSCLC的单臂、开放、多中心Ⅱ期临床研究正在入组开展。

免疫微环境异常导致的免疫抑制是PD-1/PD-L1单抗疗效降低的重要缘由。参与肿瘤血管化的多条分子通路皆能介导免疫微环境免疫抑制,使肿瘤细胞逃避免疫监视。
临床前动物试验显示,小剂量阿帕替尼使用,较中或者高剂量阿帕替尼,能够更好的实现免疫抑制性微环境向支持性微环境的重塑。小剂量阿帕替尼联合抗PD-L1治疗能显著延缓肿瘤生长,并延长肺癌动物模型生存期,提高存活率。这为抗血管生成药物联合PD-1/PD-L1免疫治疗的策略在NSCLC治疗的临床应用提供了理论基础。
一项国产PD-1卡瑞利珠单抗(SHR-1210)+阿帕替尼联合后线治疗非鳞NSCLC的,开放、多中心、Ⅰ/Ⅱ期临床研究结果显示,在91例可评估的患者中,总ORR为30.8%,DCR为82.4%,中位PFS为5.9个月,且整体耐受性良好。仑伐替尼联合帕博利珠单抗治疗NSCLC的Ⅰb/Ⅱ期临床研究结果显示,主要终点第24周的ORR为33.3%(95%CI:14.6~57.0)。次要终点中位PFS为5.9个月(95%CI:2.3~13.8),12个月PFS生存率为29.0%(95%CI:10.2~51.0),中位DOR为10.9个月(95%CI:2.4~不可估计),且一般耐受性良好。
一项尼达尼布联合PD-1抑制剂纳武利尤单抗+CTLA-4抑制剂易普利姆玛单抗后线治疗晚期NSCLC患者的Ⅰ期研究结果显示,尼达尼布+双免疫的治疗方案展现良好的安全性,在既往对免疫治疗耐药的患者也有抗肿瘤疗效,提示抗血管和双免疫的新联合方案的可能。
一项国产PD-1单抗信迪利单抗+安罗替尼用于一线治疗EGFR/ALK/ROS1阴性晚期NSCLC患者的Ⅰ期研究结果表明,联合方案初步观察安全、可耐受,主要研究终点ORR可达72.7%,同时DCR达100%,有望成为晚期NSCLC一线治疗新的选择。

确定疗效生物标志物是选择优势人群和实现精准抗血管生成治疗的前提,但对于抗血管生成药物在NSCLC中治疗有效性的相关生物标志物的探索,目前仍处于初始阶段。
韩宝惠教授团队通过采集Alter0303(安罗替尼疗法评估NSCLC临床抗肿瘤疗效)研究参与者循环DNA分析其ARID1A和BRCA2基因谱,确定三种可能预测因子:种系和体细胞突变负荷(G+S-MB),非同义和同义突变负荷(N+S-MB),循环DNA谱的不利突变评分(UMS)。通过整合三个独立预测因子的优缺点建立肿瘤突变指(TMI)预测模型。基于TMI的分层,IDH1exon4被确定为安罗替尼治疗的不利因素。TMI联合IDH1exon4可预测NSCLC患者对安罗替尼治疗的应答。

抗血管新生治疗是晚期NSCLC治疗重要的手段。以安罗替尼为代表的抗血管生成小分子靶向药已经成为我国NSCLC标准的三线治疗方案。抗血管生成小分子靶向药二线联合化疗,一线联合EGFR-TKI治疗方案正在探索。抗血管生成小分子靶向药联合免疫后线治疗NSCLC的前期研究结果令人鼓舞,Ⅲ期研究将探讨其一线治疗适应证。同时我们也期待VEGFR-TKI的疗效标志物的进一步验证。
参考文献
[1] Hall R D,et al.Angiogenesis inhibition as a therapeutic strategy in non-small cell lung cancer (NSCLC) .Lancet, 2014, 384 (9944) :665-673.doi:10.3978/j.issn.2218-6751.2015.06.09
[2] Ding L,et al. The use of apatinib in treating nonsmall-cell lung cancer: case report and review of literature[J/OL]. Medicine,2016[2017-08-11]. http: / / europepmc. org / art- icles/PMC4902403/.
[3]Lu S,et al. Randomized, Double-Blind, Placebo-Controlled, Multicenter Phase Ⅱ Study of Fruquintinib After Two Prior Chemotherapy Regimens in Chinese Patients With Advanced Nonsquamous Non‒Small-Cell Lung Cancer[J]. Journal of Clinical Oncology Official Journal of the American Society of Clinical Oncology, 2018, 36(12):JCO2017767145.
[4] Lu S, et al.A RANDOMIZED PHASE ⅡI TRIAL OF FRUQUINTINIB VERSUS PLACEBO IN PATIENTS WITH ADVANCED NON-SMALL CELL LUNG CANCER (FALUCA).2019WCLC abstract.p324-325
[5]Han B,et al.Efficacy and safety of third-line treatment with anlotinib in patients with refractory advanced non-small cell lung cancer (ALTER-0303) :A randomised, double-blind, placebo-controlled phase 3 study[J].Lancet Oncology, 2017, 18 (1) :S3.
[6] Reck M,et al. Docetaxel plus nintedanib versus docetaxel plus placebo in patients with previously treated non-small-cell lung cancer ( LUME-Lung 1) : a phase 3, double-blind,randomised controlled trial[J]. Lancet Oncol, 2014,15( 2) : 143-155.
[7] Jianping X, et al. Apatinib plus icotinib in treating advanced non-small cell lung cancer after icotinib treatment failure: a retrospective study[J]. OncoTargets and Therapy, 2017, Volume 10:4989-4995.
[8] Zhang Li, et al.2018 ASCO Annual Meeting, Abstract No: TPS9116
[9] Lu S , et al. A Phase Ⅱ Study of Fruquintinib in Combination with Gefitinib in Stage ⅡIb/IV NSCLC Patients Harboring EGFR Activating Mutations[J]. Journal of Thoracic Oncology, 2017, 12(11):S2228.
[10]Zhao S, et al.Low-Dose Apatinib Optimizes Tumor Microenvironment and Potentiates Antitumor Effect of PD-1/PD-L1 Blockade in Lung Cancer.Cancer Immunol Res. 2019 Apr;7(4):630-643
[11] Zhou CC,et al.2018ASCO Annual Meeting abstract e21017
[12] Brose MS et al, ASCO 2019 abstract No. 16 (board No. A9)
[13] J.E. Gray ,et al . PHASE I STUDY OF NIVOLUMAB AND IPILIMUMAB COMBINED WITH NINTEDANIB IN ADVANCED NON-SMALL CELL LUNG CANCER. 2019WCLC abstract.P671
[14] B. Han,et al.EFFICACY AND SAFETY OF SINTILIMAB WITH ANLOTINIB AS FIRST-LINE THERAPY FOR ADVANCED NON-SMALL CELL LUNG CANCER (NSCLC). 2019WCLC abstract.P180
[15] Jun Lu, et al. Circulating DNA-Based Sequencing Guided Anlotinib Therapy in Non-Small Cell Lung Cancer.Advanced Science.2019 Aug.DOI: 10.1002/advs.201900721
作者 | 王婉莹 任胜祥(上海市肺科医院)
编辑 | 郝冉(中国医学论坛报)

查看更多