查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





近年来,新兴抗癌“神药”ADC发展迅猛,疗效比靶向药更好,而且还能完美解决靶向耐药,甚至是PD1耐药后的治疗也能奏效。
2013年,FDA批准T-DM1上市,用于治疗HER2阳性的转移性乳腺癌患者,成为全球首个获批的单药治疗实体瘤的抗体药物偶联物。2020年1月,国家药品监督管理总局正式批准创新靶向药物赫赛上市。这是中国上市的第一个也是目前唯一一个HER2靶向与化疗偶联的ADC产品。
目前,除了TDM1还有很多国外已经上市以及正在研发的ADC药物,不仅靶向HER2,更不仅仅针对乳腺癌!下面,汝爱小编汇总了一下目前比较领先的几款ADC药物,供大家参考。
“抗癌神药”ADC
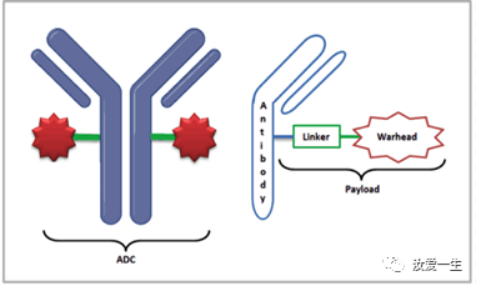
ADC,即抗体药物偶联物,就是将靶向特定抗原的抗体(mAb),通过连接子(linker)与药物载荷-细胞毒小分子(payload)连接在一起。ADC药物依靠抗体的特定靶向性到达肿瘤细胞,再通过内吞作用进入到细胞,在低pH值或溶酶体蛋白的作用下linker断裂,释放出细胞毒小分子,从而发挥对肿瘤细胞的杀伤作用。
DS8201靶向四大癌种,尽显神药本色
2019年12月21日,基于DESTINY-Breast01研究,FDA正式批准DS-8201用于HER2阳性乳腺癌的后线治疗。
2020年5月18日,阿斯利康和第一三共联合宣布,双方共同开发的DS-8201获得美国FDA授予的突破性疗法(BTD)认定,用于治疗HER2突变的铂类治疗中或治疗后疾病进展的转移性非小细胞肺癌(NSCLC)患者。
2021年1月15日,FDA批准DS-8201扩展适用范围,用于经曲妥珠单抗治疗的HER2阳性局部晚期或转移性胃癌和胃食管结合部(GEJ)腺癌患者。
而就在今天,欧盟批准了DS-8201用于HER2阳性乳腺癌的后线治疗。
该批准同样是基于著名的DESTINY-Breast01 2期试验,该试验纳入的患者均接受过2种以上HER2靶向方案。2020SABCS大会上公布的数据显示,截至2020年6月8日,中位随访20.5个月,37名患者(20.1%)仍在接受治疗。中位完全缓解时间(DoR)为20.8 个月;中位无进展生存期(mPFS)为19.4 个月(95%CI,14.1 mo-NE);确认的客观缓解率(ORR)为61.4%(其中有12个CR),疾病控制率(DCR)为97.3%(95%CI,93.8~99.1);
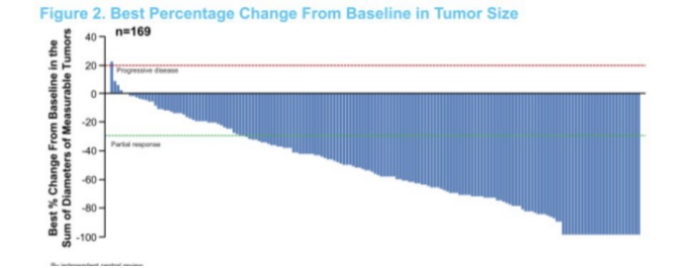
12个月OS率为85%(95%CI,79%~90%),在18个月OS率为74%(95%CI,67%~80%)。初步的mOS为24.6 个月(估计为35%的成熟度)。

DS8201的安全性与先前报道的相似。经过9个月的随访,仅报告了3例新的DS8201相关性间质性肺病(ILD)。
DS-8201的临床数据遍布乳腺癌、胃癌、肺癌、结直肠癌,给多癌种HER2突变患者带来了新的治疗希望,展现出非凡的潜力!期待DS-8201的国内获批。
ARX788 DCR高达100%!晚期HER2患者的有力保障
ARX788是由安博生物和浙江医药共同研制的ADC药物。在2020 CSCO大会上,复旦大学附属肿瘤医院胡夕春教授,介绍了ARX788在HER2阳性晚期乳腺癌患者中的安全性和有效性的研究。
与TDM1相比,ARX788的工艺控制、药物稳定性和体内代谢等方面均具有很好的优势。
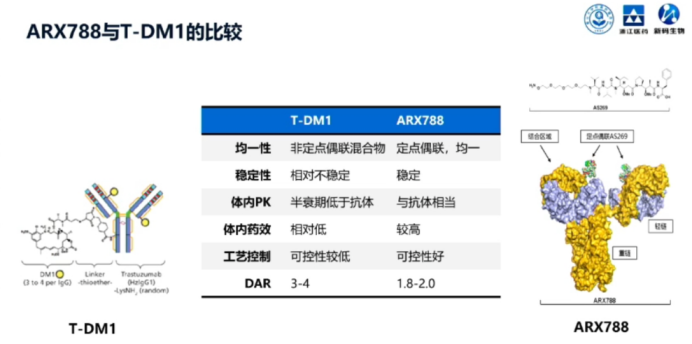
研究共入组59例HER2阳性晚期乳腺癌患者,94.9%的患者为HER2阳性,5.1%的患者为HER2低表达,所有患者均经历过曲妥珠单抗治疗。
疗效方面,从疗效瀑布图可见,大部分患者均得到显著改善,高剂量组患者疗效更好。也就是说,随着剂量的递增,ORR更好,1.5mg/kg组的ORR达到了68.4%,DCR100%,无DLT发生。既往使用过TKI治疗的患者ORR也达到了44.7%。
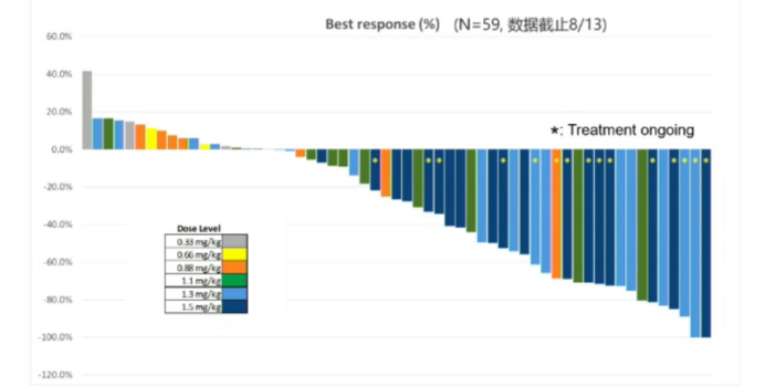
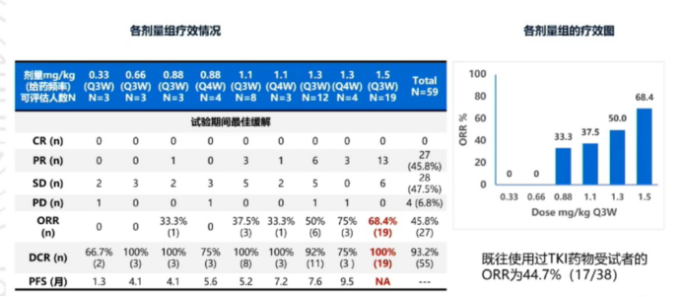
不良反应方面,在59名受试者中,仅出现了7例与药物相关的≥3级不良反应。
ARX788展现了巨大的潜力。虽然不同于DS-8201针对T-DM1等治疗失败的患者,但ARX788对曲妥珠单抗和拉帕替尼治疗失败的患者都表现出很高的响应率,1.5 mg/kg组DCR更是高达100%,且安全性较好。ARX788治疗HER2阳性乳腺癌的II/Ⅲ期研究正在进行中,静候佳音。
IMMU132拿下最难三阴乳腺癌
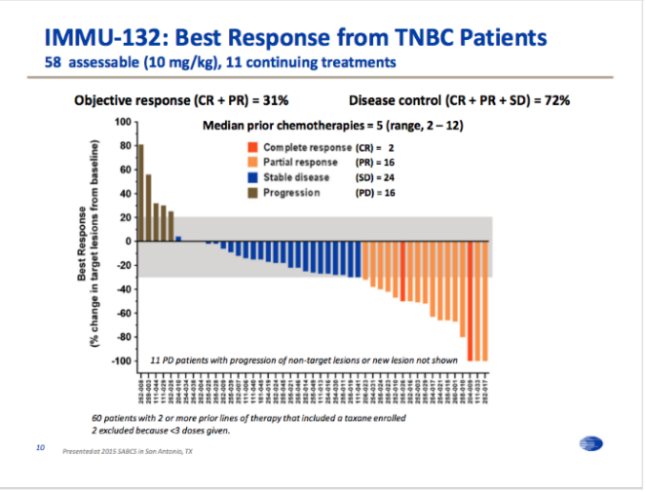
Trop-2是一种跨膜糖蛋白,在各种人类上皮癌中更是高度表达,这使得TROP2成为一个理想的治疗靶点。2020年4月22日,Trop-2 ADC药物Sacituzumab Govitecan (Trodelvy,IMMU-132)获得FDA加速批准,用于三线及以上转移性三阴乳腺癌,成为首个上市的Trop-2靶向药物。
该获批是基于ASCENT研究,IMMU-132在三阴乳癌后线临床研究结果,以33.3%的三线有效率,直接绿灯通行,成功上市。TROP2靶点的药物在各癌种数据中也相继报道,泛癌种治疗趋势逐渐成形!
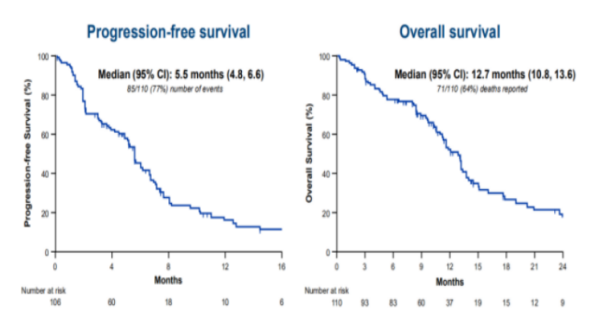
该研究中接受IMMU-132治疗的患者组ORR高达33.3%,远高于传统的化疗组疗效。中位PFS是5.5个月,中位OS为13个月。
全面覆盖的维迪西妥单抗
维迪西妥单抗(rc48-adc)是由荣昌生物开发,靶向多个癌种的ADC。
2018年9月,维迪西妥单抗被FDA授予治疗胃癌的孤儿药资格;
2020年11月12日,被FDA授予治疗胃癌的快速审批通道资格;
2020年12月28日,针对HER2阳性尿路上皮癌获得CDE的突破性疗法认证。
但是在乳腺癌这个大瘤种上,维迪西妥单抗进展最快的是针对HER2低表达的局部晚期或转移性乳腺癌,目前已经开展Ⅲ期临床,而针对HER2阳性乳腺癌的临床开发则处于II期。期待乳腺癌上市的好消息。
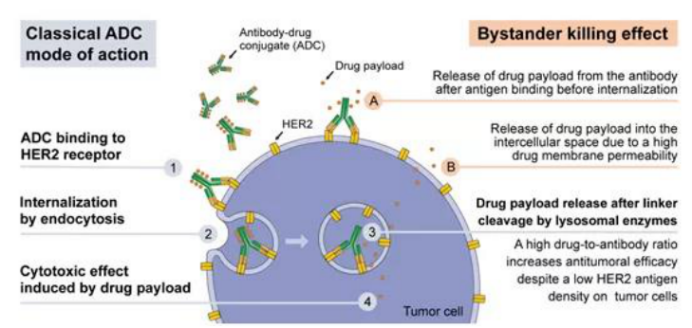
总之,ADC药物结合了靶向的精准与化疗的高效,既提高了靶向治疗的疗效,又降低了化疗的毒副作用,真正达到了1+1>2的效果,从而开启了靶向治疗2.0新篇章!未来,期待更多的ADC型药物用于乳癌治疗,为我们的患者带来更多的临床获益!
找药宝典平台发布
查看更多