查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





近日,复旦大学附属华山医院神经内科郁金泰教授团队联合复旦大学类脑智能科学与技术研究院程炜/冯建峰教授团队开展合作,通过对阿尔茨海默病(AD)病人的脑脊液蛋白组学数据进行深入研究,发现了具有不同分子特征及进展轨迹的三类AD亚型,并系统比较了三种亚型之间在认知功能及其纵向变化、神经影像学、核心脑脊液生物标志物以及遗传风险特征等方面的差异。相关研究成果以“Proteomics reveals three molecular subtypes of Alzheimer's disease with distinct progression patterns”为题发表于Alzheimer’s & Dementia杂志上。


大量临床与研究证据表明, AD并非单一疾病实体,而是一种具有显著异质性的神经退行性疾病。不同患者在分子病理、脑结构损伤模式、认知受损特征及疾病进展速度方面存在明显差异。既往基于临床表现、起病年龄或影像学特征的分型研究,因缺乏分子层面的直接证据,难以揭示其生物学基础。
因此,该研究利用阿尔茨海默病神经影像学计划(ADNI)队列中的脑脊液蛋白数据,识别具有稳定分子特征的AD生物学亚型,并阐释各亚型所涉及的关键分子通路。发现了不同亚型在认知功能及其纵向变化、神经影像学指标、核心脑脊液生物标志物以及遗传风险特征等方面的差异,并系统刻画各亚型的疾病进展轨迹。
基于脑脊液蛋白组学特征,本研究识别出三种具有明确分子特征的AD生物学亚型。三类亚型在人口学特征上基本一致,但在蛋白表达谱及其所涉及的上调生物学通路方面呈现出显著差异(图1)。

亚型1主要表现为核糖核酸(RNA)代谢和加工相关通路异常,代表性上调蛋白包括TMCC3和TSC2,而与轴突发生相关的蛋白水平整体降低,提示以转录与RNA处理功能受损为主要特征。

亚型2的分子异常集中于轴突发育和神经结构重塑过程,其代表性蛋白如SMOC1和14-3-3蛋白家族显著改变,反映神经轴突完整性和神经连接受损。

亚型3则以细胞分解代谢和蛋白降解通路异常为突出特征,代表性蛋白包括SPC25和LRRN1,提示细胞稳态调控紊乱和蛋白质代谢失衡在该亚型中占据主导地位。
整体来看,不同AD亚型由不同分子通路驱动,体现了AD在分子层面的显著异质性。
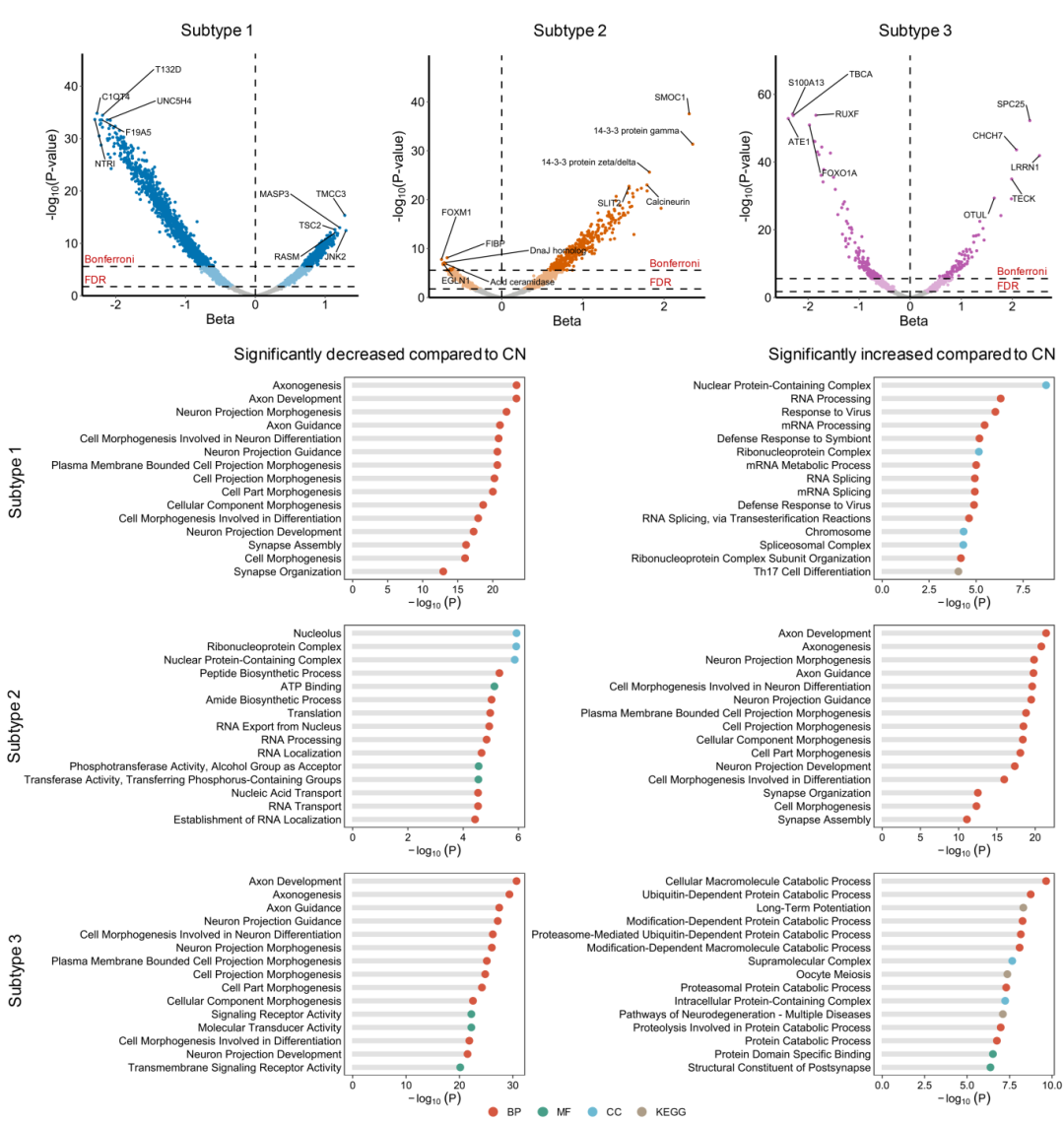
图1 基于脑脊液蛋白组学数据识别的三种AD亚型
及其相关生物学通路
不同AD生物学亚型在认知功能、遗传风险、神经影像学改变及AD核心生物学标志物等多个层面呈现出系统性差异。
总体而言
亚型1在基线时表现出相对保留的整体认知功能,在简易精神状态量表(MMSE)、记忆和执行功能等多个认知维度上均优于其他亚型,并在随访过程中显示出最缓慢的认知下降和临床进展;亚型3在基线即表现出最严重的认知受损,随后进展为痴呆的速度最快,认知下降和临床恶化最为显著,而亚型2多数指标介于两者之间。
遗传风险分析
亚型1的APOE ε4携带率和多基因风险评分最低,亚型3则具有最高的遗传风险,即使在剔除APOE区域变异后,该差异仍然存在,提示其遗传易感性并非仅由APOE ε4所驱动。
核心病理标志物
三种亚型在脑脊液β淀粉样蛋白(Aβ)42、总tau蛋白(t-tau)和磷酸化tau(p-tau)水平上显著不同,其中亚型2表现出最显著的tau升高,而亚型3则同时伴随更明显的淀粉样蛋白降低和tau病理增强。
神经影像学分析
三种亚型均存在典型AD相关脑区萎缩,但亚型3在基线和随访过程中均表现出最广泛、最严重的脑萎缩,尤其累及海马、内嗅皮层和颞叶结构,而亚型2的萎缩程度和进展速度整体高于亚型1。
上述结果共同表明,不同AD生物学亚型不仅在分子层面存在差异,其临床表现、病理负荷及疾病演变过程亦呈现出高度一致且系统性的分化特征(图2)。
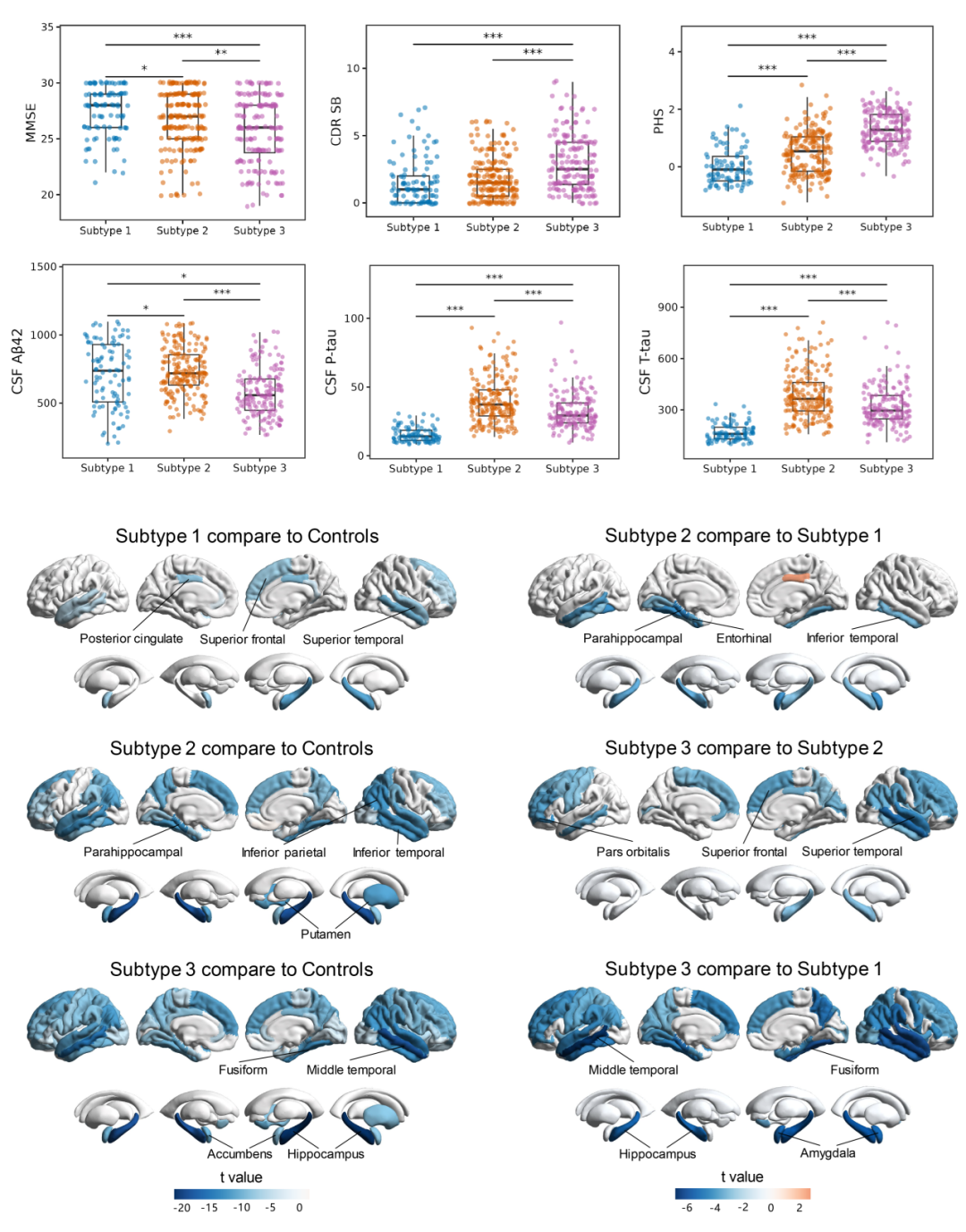
图2 不同AD生物学亚型在认知功能、遗传风险、AD核心生物学标志物以及神经影像学改变等多个层面均呈现出显著差异
在随访过程中,不同AD生物学亚型表现出显著不同的疾病进展轨迹。本研究分析对象为基线时尚未达到痴呆诊断标准的AD患者,随时间推移,各亚型在向痴呆进展的速度上出现明显分化。
其中,亚型3的疾病进展最快,更早发展为痴呆;亚型1的进展最为缓慢,表现出相对稳定的临床演变过程;亚型2的进展速度介于两者之间,但其与亚型1之间的差异相对较小(图3)。
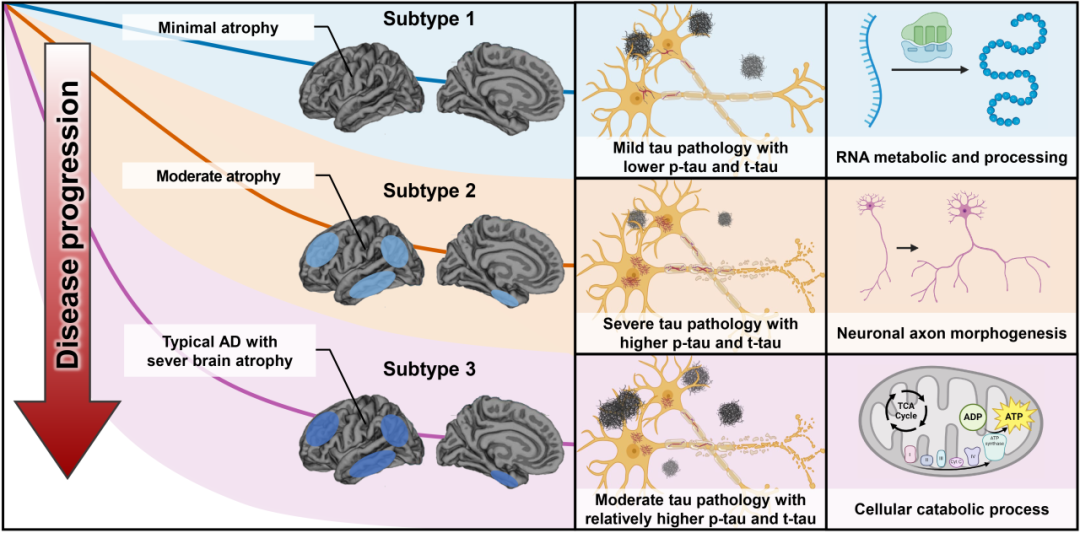
图3 三种AD生物学亚型的特征总结

本研究基于大规模脑脊液蛋白组学数据,系统揭示了AD在分子层面的显著异质性,识别并验证了三种具有稳定生物学特征的AD亚型。不同亚型在分子通路、遗传风险、核心病理标志物、脑结构损伤模式以及疾病进展轨迹等多个层面呈现出高度一致且相互区分的特征,表明AD并非由单一病理机制驱动。这一分子分型框架不仅为理解AD不同临床结局和进展速度提供了生物学依据,也为未来基于亚型的风险分层、临床试验设计及精准干预策略奠定了重要基础。



来源 复旦华山认知
查看更多