查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





编者按:随着抗反转录病毒治疗(ART)的不断优化,HIV/AIDS患者的长期管理已逐步向"简化、长效、耐受性好"的方向发展。2026年反转录病毒和机会性感染大会(CROI 2026)上,多项研究聚焦于新型长效制剂、广谱中和抗体联合方案及新型双药单片复方制剂的临床应用潜力。为深入解读这些研究的临床意义,特邀深圳市第三人民医院卢洪洲教授,从药物机制、临床数据及转化价值等维度,对三项代表性研究进行点评。
摘要号:175
注射用HIV-1衣壳抑制剂VH4011499(VH-499)制剂支持超长效给药
研究简介
VH4011499(VH-499)是一种HIV-1衣壳抑制剂,目前正在开发作为长效ART用于HIV-1治疗。在一项概念验证研究中,口服VH-499在HIV-1感染者中显示出快速且强效的抗病毒活性,且耐受性良好。本项首次人体研究旨在评估注射用VH-499制剂的超长效潜力,现报告其安全性和药代动力学结果。
研究方法
这项正在进行中的双盲(申办方非盲)Ⅰ期研究(NCT06724640)中,研究者将未感染HIV-1的参与者随机分配,接受单次递增剂量的VH-499肌内注射或皮下注射(本文评估100、200和400 mg剂量)或安慰剂。收集给药后的安全性和药代动力学数据。通过非房室分析评估单次给药的药代动力学参数。
研究结果
总体而言,48名参与者接受VH-499或安慰剂作为肌内或皮下注射(共6组,每组8人)。中位年龄为36岁,94%的参与者为男性,40%为非白人种族。所有治疗组中大多数不良事件的严重程度最高为1级或2级。与VH-499相关的不良事件主要为注射部位反应,最常见的是注射部位疼痛(27/36;75%)。所有组中注射部位反应的中位持续时间范围为1至3天。与肌内注射组相比,皮下注射组VH-499相关注射部位反应的发生率更高(83%-100% vs 33%-83%)。无参与者因安全性原因退出研究。未报告严重不良事件。
基于初步药代动力学分析,肌内注射后达到VH-499最大浓度中位时间约为给药后7至18天;由于吸收较慢,皮下注射后达到最大浓度中位时间约为给药后112天。在所有剂量水平下,皮下注射后的VH-499最大浓度均低于肌内注射。鉴于肌内和皮下两种给药途径的VH-499药代动力学曲线均相对平缓,根据现有数据无法确定终末半衰期,需要更长期的药代动力学数据。
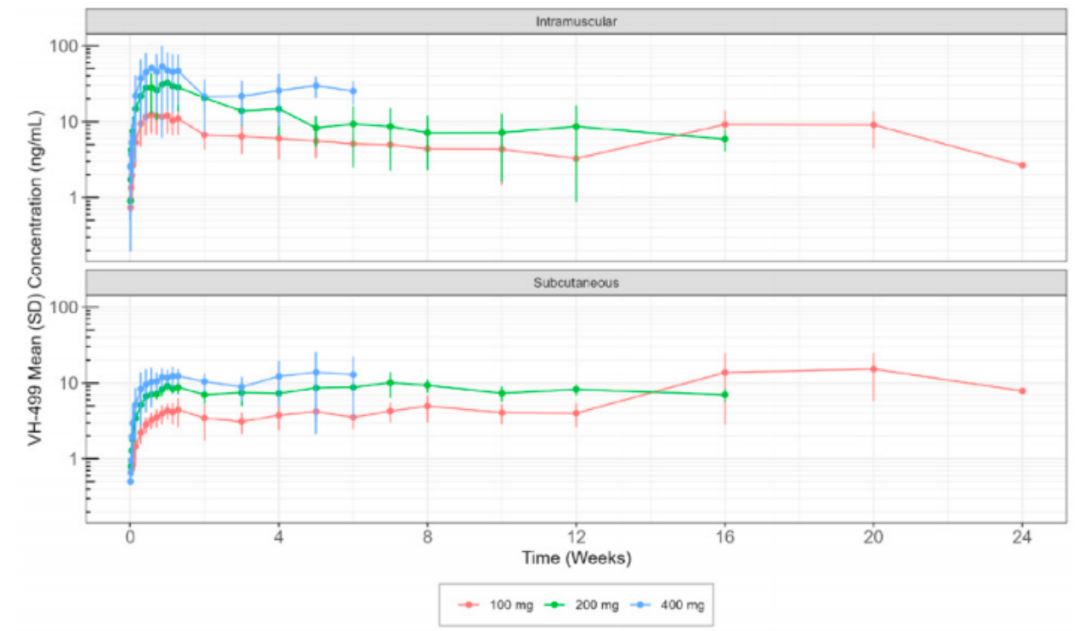
△肌内或皮下注射VH-499后的浓度-时间曲线图
研究结论
在未感染HIV-1的人群中,单次剂量VH-499肌内注射和皮下注射均耐受良好,且皮下注射表现出较慢的吸收速率。这些结果表明,长效注射用VH-499制剂具有支持超长效(即≥4个月)给药间隔的潜力,且可由医疗专业人员注射或自行给药。基于本研究中新出现的药代动力学和安全性数据,采用模型引导的药物开发方法将有助于优化VH-499未来开发的方案设计。
专家点评
半年注射一次的来那卡帕韦(Lenacapavir)已是大家较为熟知并且已经影响临床实践的新型长效衣壳抑制剂。本研究探讨的是另一种长效新型衣壳抑制剂VH-499的注射制剂,结果显示其具有良好的安全性和超长半衰期(47-56天),支持每3个月或更长间隔给药的潜力。VH-499作为一种靶向HIV-1衣壳蛋白的新型作用机制药物,与现有抗反转录病毒药物无交叉耐药,为多重耐药患者提供了新的治疗选择。值得注意的是,注射部位反应虽常见但多为自限性,提示其具有良好的临床可操作性。
然而,目前的研究仍处于早期阶段,样本量较小,且仅在HIV阴性人群中评估了安全性和药代动力学。后续需要在HIV感染者中验证其抗病毒活性、长期安全性及与其它药物的联合应用方案。
摘要号:178
VH3810109(N6LS)每4月一次联合卡替拉韦长效注射液每月一次维持HIV抑制12个月:EMBRACE研究
研究简介
VH3810109(N6LS)是一种靶向CD4结合位点的广谱中和抗体,正在开发用于超长效HIV-1治疗。EMBRACE研究评估了N6LS每4月一次联合每月一次肌内注射长效卡替拉韦(Cabotegravir)在维持HIV-1抑制中的疗效、安全性和耐受性。6个月结果显示,静脉注射和皮下注射N6LS方案在基线对N6LS敏感的参与者中分别有96%和88%维持病毒学抑制,其中N6LS静脉注射显示出良好的安全性和耐受性。本文报告EMBRACE研究预设中期分析中12个月的疗效、安全性、耐受性和临床评估结果。
研究方法
EMBRACE是一项在HIV-1 RNA ≤ 50copies/mL且对N6LS表型敏感(半数抑制浓度 ≤ 2微克/毫升,最大抑制百分比 > 98%)的成人感染者中开展的随机、开放标签、多中心Ⅱb期研究。参与者按2:2:1的比例随机分配至N6LS 60mg/kg静脉注射联合卡替拉韦长效注射液、N6LS 3000mg联合重组人透明质酸酶PH20皮下注射联合卡替拉韦长效注射液,或继续其基线前的标准治疗方案。主要终点是第6个月时HIV-1 RNA ≥ 50copies/mL的比例(美国FDA快照分析)。研究旨在确保失败率从2%到6%的有效性证据。
研究结果
共有125名参与者被随机分配;人口学数据先前已有报告。第12个月时,N6LS静脉注射组有3/50(6%),N6LS皮下注射组有5/49(10%),标准治疗方案组有1/26(4%)出现HIV-1 RNA ≥ 50copies/mL(美国食品药品监督管理局快照分析)。至第12个月,N6LS静脉注射组有2名(4%)、N6LS皮下注射组有3名(6%)、标准治疗方案组有1名(4%)参与者发生确认病毒学失败。
导致退出研究的不良事件发生在1/50名静脉注射参与者和5/49名皮下注射参与者中(N6LS相关不良事件导致退出:静脉注射组0/50,皮下注射组1/49),无N6LS相关的严重不良事件。3级及以上N6LS相关注射部位反应发生在0/50名(0%)静脉注射参与者和8/49名(16%)皮下注射参与者中。尽管存在安全性差异,两个N6LS组的参与者通过第12个月均报告了高耐受性和可接受性。
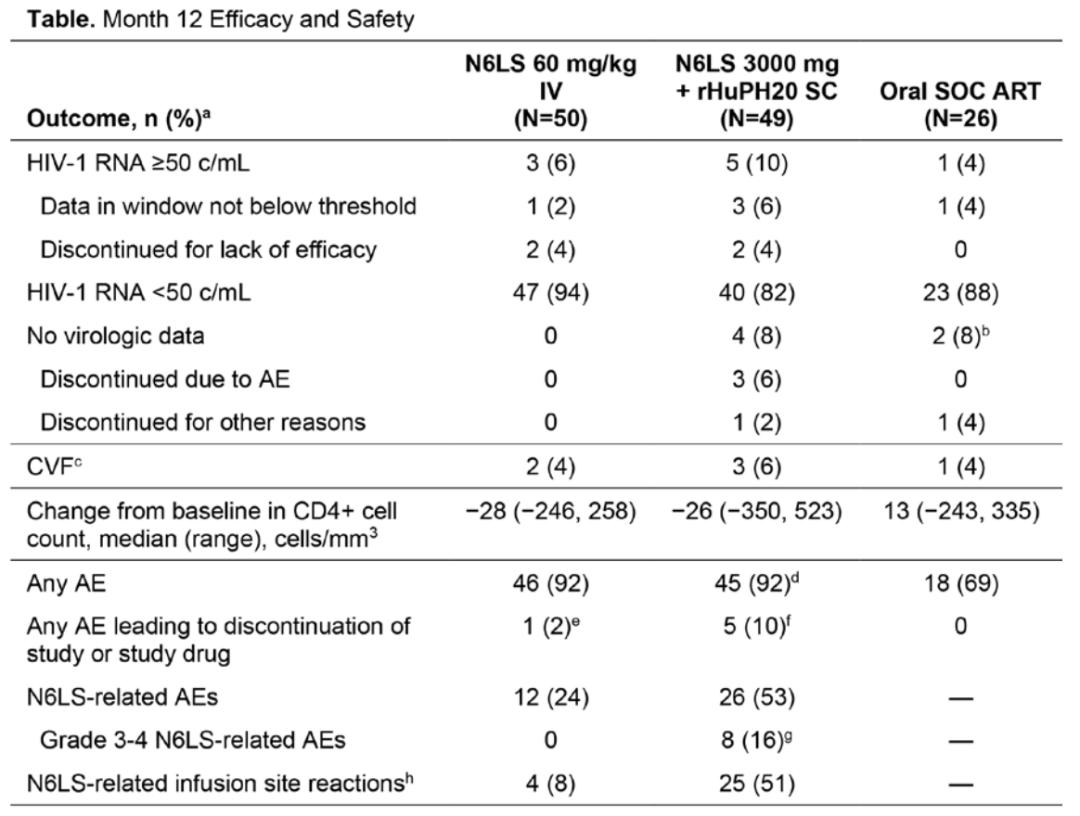
△三组感染者的12个月疗效和安全性
研究结论
N6LS静脉注射每4月一次联合每月一次卡替拉韦长效注射液在基线对N6LS敏感的成人中维持了高比例的病毒抑制,并在12个月的联合给药期间显示出比N6LS皮下注射每4月一次更好的耐受性。
专家点评
EMBRACE研究证实了广谱中和抗体N6LS联合卡替拉韦长效注射液的长效维持方案在HIV感染者中的可行性。研究结果显示,N6LS静脉注射每4月一次联合每月一次卡替拉韦长效注射液在第12个月时病毒抑制率高达94%,且注射部位反应发生率低(8%),无严重不良事件,显示出良好的安全性和耐受性。而N6LS皮下注射组注射部位反应发生率较高(51%),但多为自限性,提示皮下给药途径仍需优化。
该研究证实了“广谱中和抗体+长效整合酶抑制剂”的联合模式可作为每日口服药物的有效替代方案;其次,N6LS每4月一次的给药频率大幅延长了给药间隔,为不愿或不能坚持每日服药的患者提供了新选择。期待未来有更多研究数据披露,包括新发耐药的情况,以证实N6LS与卡替拉韦之间无交叉耐药风险,以及探索优化皮下注射制剂以降低注射部位反应发生率、探索更长用药间隔的可行性等。
摘要号:181
从复杂方案转换为单片比克替拉韦/来那卡帕韦的Ⅲ期疗效和安全性:ARTISTRY-1研究
研究简介
单片复方制剂彻底改变了HIV治疗,改善了依从性和临床结局;然而,许多接受复杂方案治疗的HIV感染者由于病毒耐药、不耐受、禁忌症或药物相互作用等原因,无法使用现有的单片复方制剂。一种新型比克替拉韦(Bictegravir,BIC)和来那卡帕韦(Lenacapavir,LEN)单片复方制剂(BIC/LEN)可能提供一种替代治疗选择。ARTISTRY-1(NCT05502441)是一项随机、开放标签的试验,评估BIC/LEN在接受复杂方案治疗且达到病毒学抑制的HIV感染者中的应用。在Ⅱ期研究中,比克替拉韦+来那卡帕韦在大多数基线存在耐药的参与者中维持了至第48周的病毒学抑制。本文报告BIC/LEN单片复方制剂的Ⅲ期疗效和安全性。
研究方法
在稳定复杂方案上达到病毒学抑制的HIV感染者按2:1的比例随机分配,转换为每日一次口服BIC/LEN(75/50mg)单片复方制剂或继续其复杂方案。主要终点是第48周时HIV-1 RNA ≥ 50copies/mL的比例(美国FDA快照分析;非劣效界值为4%)。次要终点包括第48周时HIV-1 RNA < 50copies/mL和CD4细胞计数的变化,以及至第48周的不良事件发生率;探索性终点包括第48周时的治疗满意度(HIV治疗满意度问卷现状版)。
研究结果
总体而言,557名HIV感染者被随机分配并接受治疗;371名转换为BIC/LEN,186名继续其复杂方案。基线时,中位年龄为60岁(范围:22-84岁);18%为女性。中位HIV治疗持续时间为28年(范围:3-45年),80%的患者至少有一种合并症,包括血脂异常、高血压、糖尿病或慢性肾脏病。参与者每日服用ART中位数为3片(范围:2-11片);77%的患者正在使用蛋白酶抑制剂(PIs)。第48周时,BIC/LEN组有0.8%(3/371)的参与者HIV-1 RNA ≥ 50copies/mL,复杂方案组为1.1%(2/186)(百分比差异[95.002%置信区间]:-0.3% [-2.3, 1.8]);BIC/LEN组有96.0%(356/371)的参与者HIV-1 RNA < 50copies/mL,复杂方案组为93.5%(174/186)。无参与者出现新发耐药。
BIC/LEN组的总体药物相关不良事件相较于复杂方案组更为常见(14.3% vs. 1.6%);3/4级药物相关不良事件(0.5% vs. 0)和严重药物相关不良事件(0.3% vs. 0)在两组均罕见且相似。第48周时,转换为BIC/LEN组的治疗满意度总分平均变化为+7分(标准差10.6),复杂方案组为0分(标准差9.6)(P < 0.0001)。
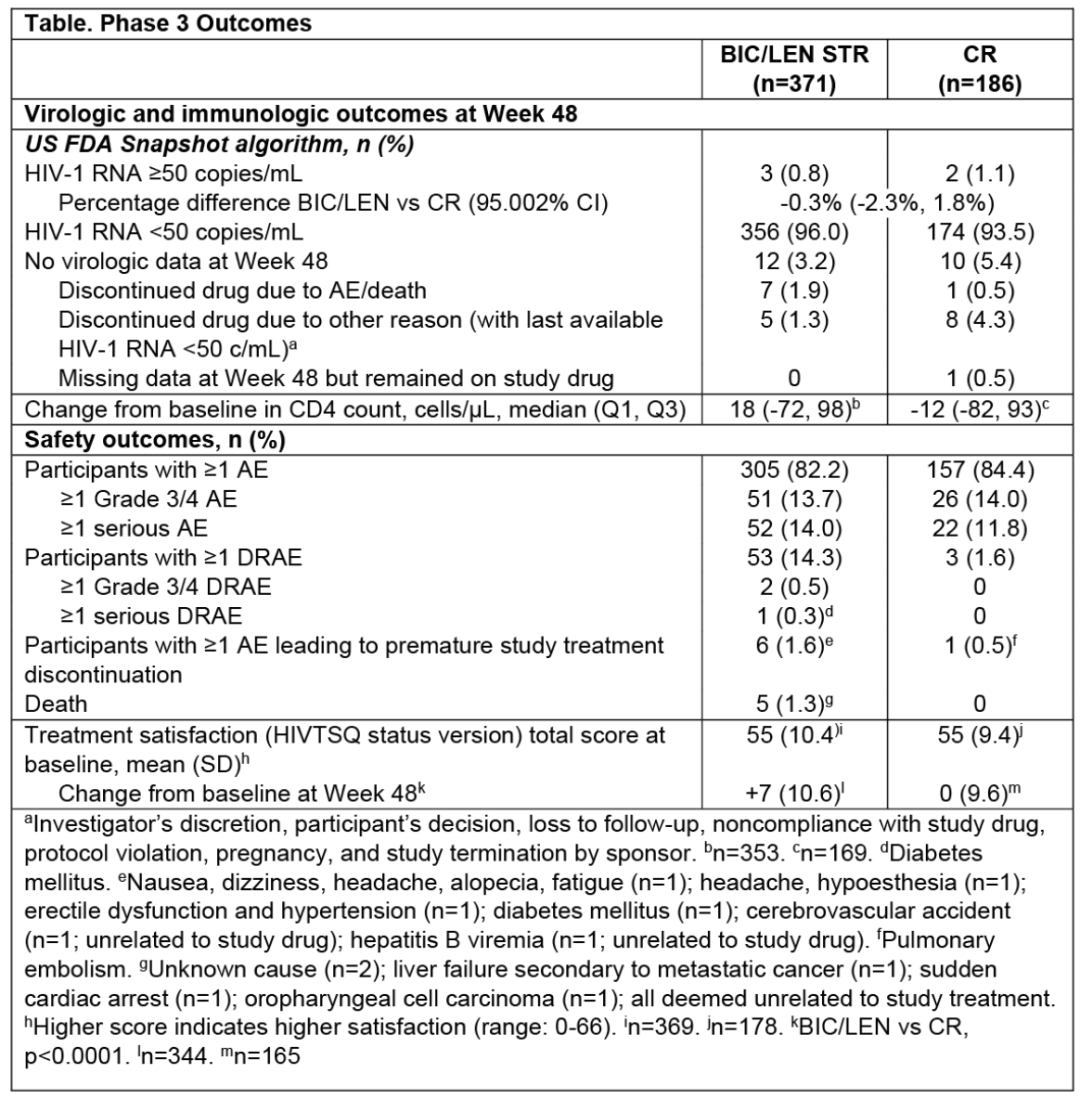
△Ⅲ期ARTISTRY-1研究的48周疗效和安全性结果
研究结论
BIC/LEN单片复方制剂维持了高比例的病毒学抑制,并在第48周时非劣效于复杂方案。BIC/LEN总体耐受性良好,并提高了治疗满意度。这些结果支持BIC/LEN单片复方制剂作为接受复杂方案治疗的HIV感染者的一种新的有效治疗选择。
专家点评
BIC作为新一代整合酶抑制剂、LEN作为新型衣壳抑制剂,前者的单片复方制剂BIC/FTC/TAF以及后者的长效制剂可谓当前临床实践中的“明星”ART方案。ARTISTRY-1研究提供了一种全新的简化单片复合制剂BIC/LEN,为那些因病毒耐药、不耐受或药物相互作用而无法使用现有单片方案的HIV感染者提供了新的治疗选择。研究结果显示,转换为BIC/LEN方案的参与者中,第48周病毒抑制率高达96.0%,非劣效于继续多片药物组,且无新发耐药病例,显示出强效且持久的抗病毒效果。
该研究证实了比克替拉韦与来那卡帕韦这两种不同作用机制药物的联合应用在单片复方制剂中的可行性,为多重耐药患者提供了新的治疗选择;其次,研究人群中位年龄60岁,80%存在合并症,代表了临床实践中常见的复杂患者群体,结果具有良好的外推性;第三,转换为单片复方制剂后,患者治疗满意度显著提高,这对于提高长期治疗依从性具有重要意义。
值得注意的是,研究中77%的患者基线时正在使用PIs方案,转换为BIC/LEN后,总体药物相关不良事件发生率虽高于继续多片方案组(14.3% vs. 1.6%),但多为轻中度,严重不良事件罕见,提示该方案具有良好的安全性。期待未来有更长随访的数据披露,以及有更多不同治疗场景、治疗人群的应用探索,包括如孕妇、青少年、合并肝炎病毒感染者中的安全性和有效性;以及与其他药物联合应用的潜力。
来源:《感染医线》
查看更多