查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





基于以上,来自南方医科大学南方医院肾内科的周丽丽/李晓龙团队于2026年2月在Kidney International杂志上发表了题为“Increased Smoothened signaling promotes kidney fibrosis through inhibiting autophagy in fibroblasts”的文章,该研究揭示肾脏成纤维细胞的Smoothened(Smo)信号在抑制细胞自噬、驱动CKD肾脏纤维化进程中的关键作用。该研究不仅为理解肾脏纤维化的演进机制提供了全新视角,也为慢性肾脏病的临床干预开辟了潜在的新靶点。

首先,研究人员通过分析人类肾脏snRNA-seq数据,将成纤维细胞划分为七个功能亚群,并发现:与健康对照组相比,在CKD样本中,Smo在皮质成纤维细胞多个亚群[FIB、dFIB(早期肌成纤维细胞)和aFIB(肌成纤维细胞潜在祖细胞)]中表达显著升高,在肌成纤维细胞(MYO)和髓质纤维细胞(M-FIB)中也有所增加,而在基质和ECM评分较低的髓质退化纤维细胞亚群(dM-FIB)中则表达下降。进一步在多种CKD模型及原代细胞中证实,Smo高表达的成纤维细胞呈现肌成纤维细胞活化表型,同时伴随自噬流受阻及自噬诱导反应性丧失。这些结果表明,Smo的高表达与成纤维细胞活化及细胞外基质产生密切相关,提示其在肾脏纤维化进程中可能发挥关键作用。(图1)
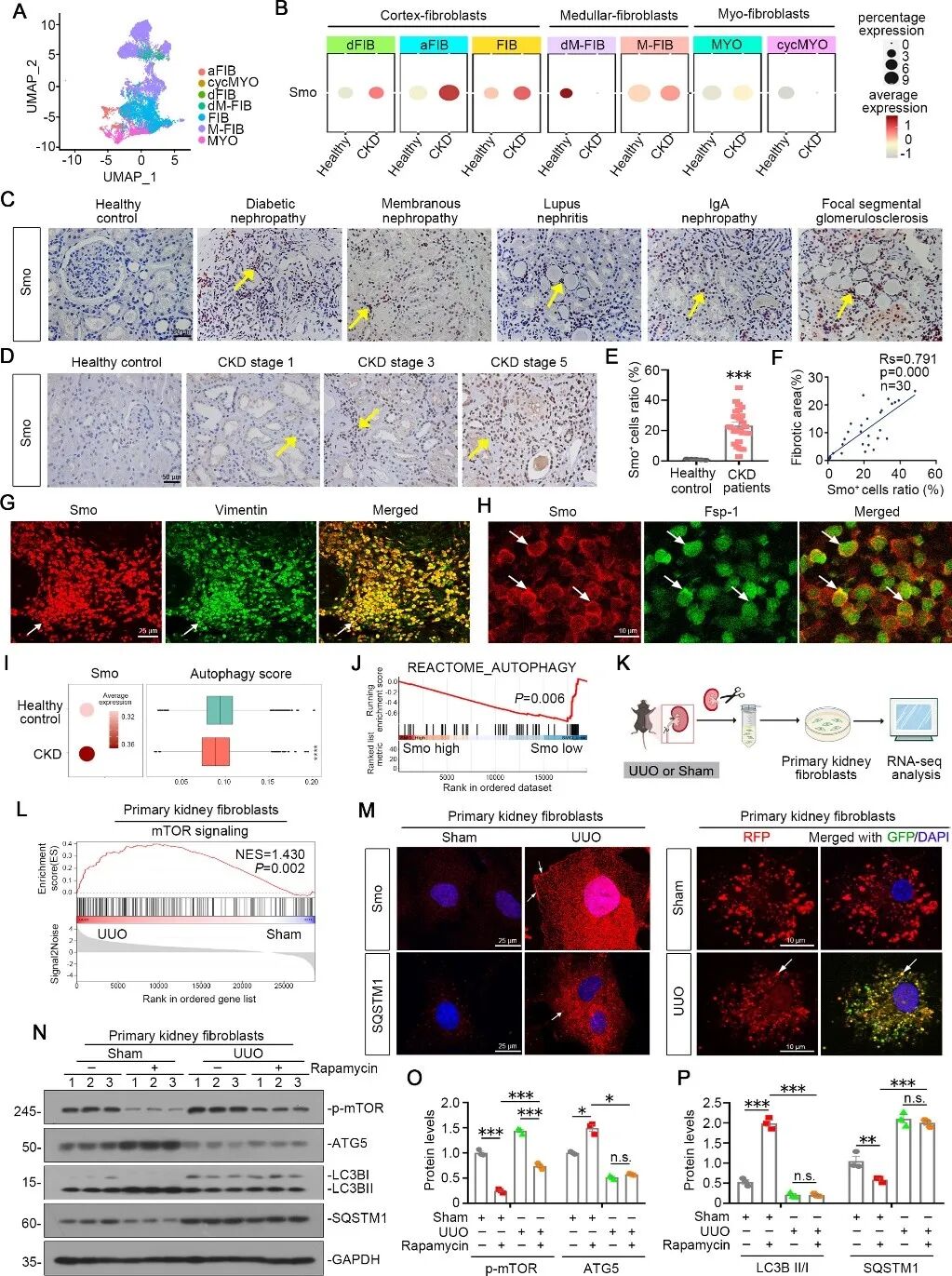
图1 Smo在活化肾成纤维细胞中上调,并与自噬能力缺陷相关
随后,研究人员通过分离原代成纤维细胞以及NRK-49F成纤维细胞系揭示:Shh刺激可上调Smo及纤连蛋白表达、促进细胞增殖,同时抑制自噬流并诱导SQSTM1积累;而使用Smo特异性拮抗剂NVP-LDE225或自噬诱导剂雷帕霉素则可逆转上述效应,抑制肌成纤维细胞活化。在ATG5敲除的成纤维细胞中,Shh对自噬的抑制作用及对肌成纤维细胞活化的促进作用进一步增强,而过表达ATG5则抵抗Shh的效应。这些结果表明,Shh/Smo信号通过抑制自噬驱动成纤维细胞向肌成纤维细胞转化,从而参与肾脏纤维化进程。(图2)
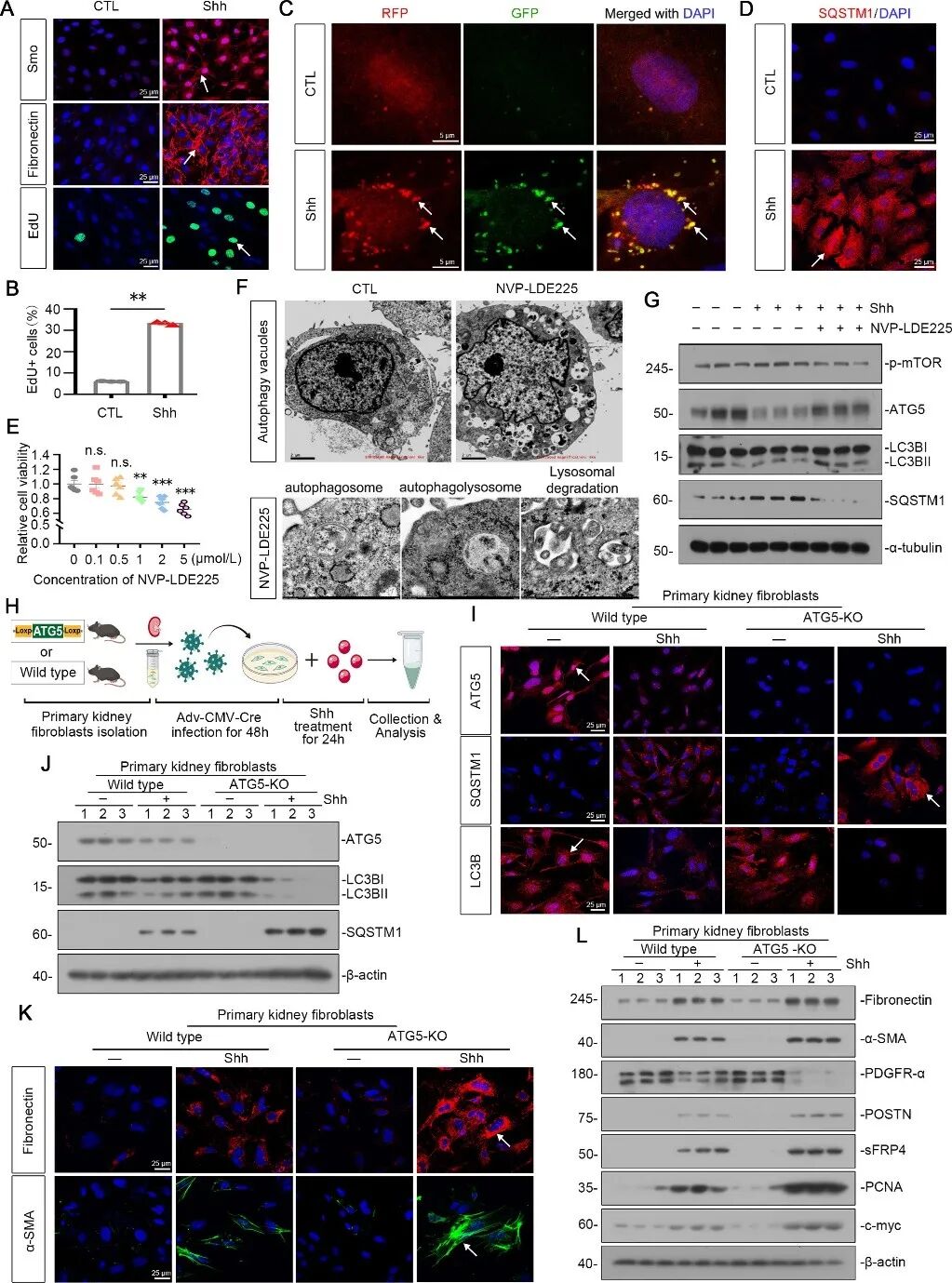
图2 Shh/Smo信号通过抑制自噬促进成纤维细胞活化
接下来,通过构建成纤维细胞特异性Smo敲除小鼠(SmoCKO)并实施UUO手术,研究人员发现:与对照组相比,SmoCKO小鼠来源的原代肾成纤维细胞中p-mTOR和SQSTM1表达下调,ATG5和LC3BII形成增加,自噬空泡增多,自噬能力得以恢复;同时,这些细胞的肌成纤维细胞活化标志物表达降低,增殖能力减弱,肾间质基质沉积和纤维化病变明显减轻。这些结果表明,成纤维细胞中的Smo通过抑制自噬促进肌成纤维细胞活化,从而驱动肾脏纤维化进展。(图3)
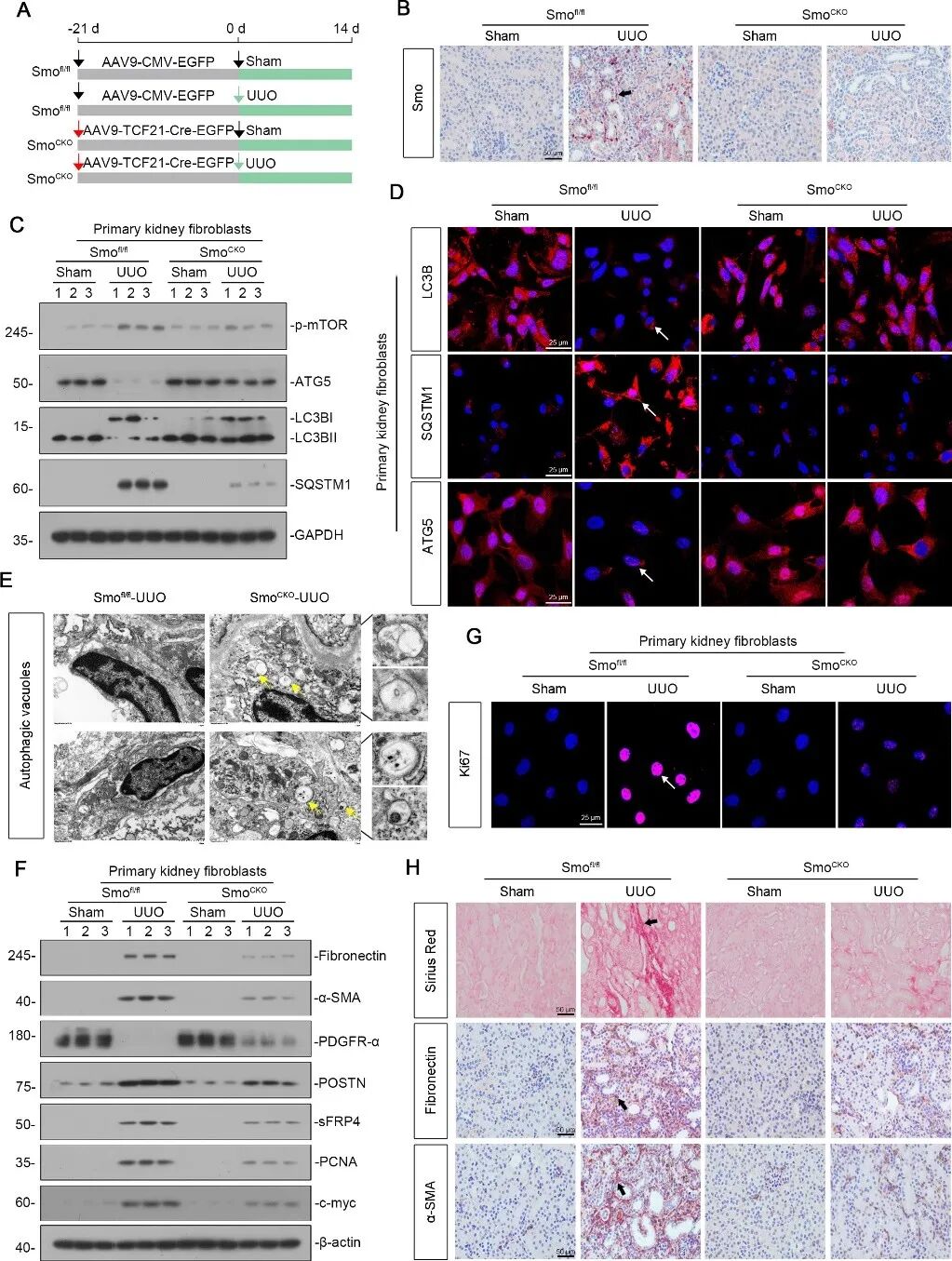
图3 特异性敲除成纤维细胞Smo可增强自噬并缓解肾纤维化
接下来,研究人员通过整合人类肾脏snRNA-seq数据分析及原代成纤维细胞GSEA验证,发现Smo正向调控细胞外基质形成、非经典Wnt信号及mTOR通路,同时抑制自噬;进一步机制研究表明,Smo通过β-arrestin 1/Src复合物促进β-catenin活化入核,而使用β-catenin降解剂KYA1797K或干扰β-arrestin 1可抑制p-mTOR、恢复自噬流并阻抑肌成纤维细胞活化。这些结果表明,Smo主要通过β-arrestin 1/Src/β-catenin调控成纤维细胞自噬与活化。(图4)
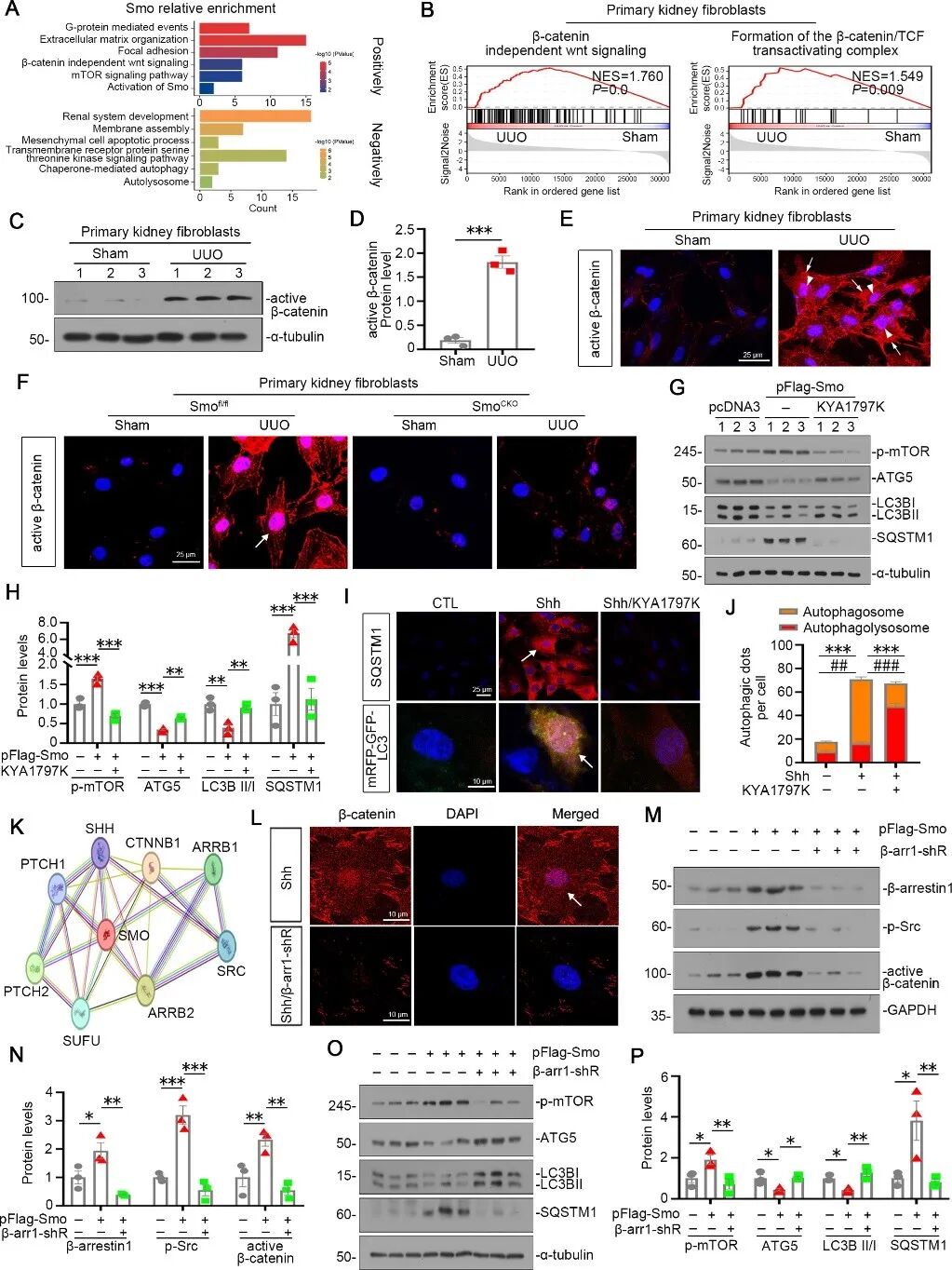
图4 Smo通过激活β-arrestin 1/Src/β-catenin途径抑制成纤维细胞的自噬
随后,生信预测与实验验证显示,β-catenin核效应分子TCF/LEF可直接结合 mTOR 启动子,Smo与β-catenin过表达可协同上调mTOR转录及蛋白磷酸化,而β-catenin降解剂KYA1797K可阻断这一过程。功能实验表明,β-catenin过表达通过激活mTOR抑制自噬流,雷帕霉素可逆转该效应并减轻肌成纤维细胞活化与基质沉积。上述结果揭示 Smo/β-catenin/TCF-LEF轴通过转录上调mTOR、抑制成纤维细胞自噬,进而驱动肾脏纤维化的新机制。(图5)
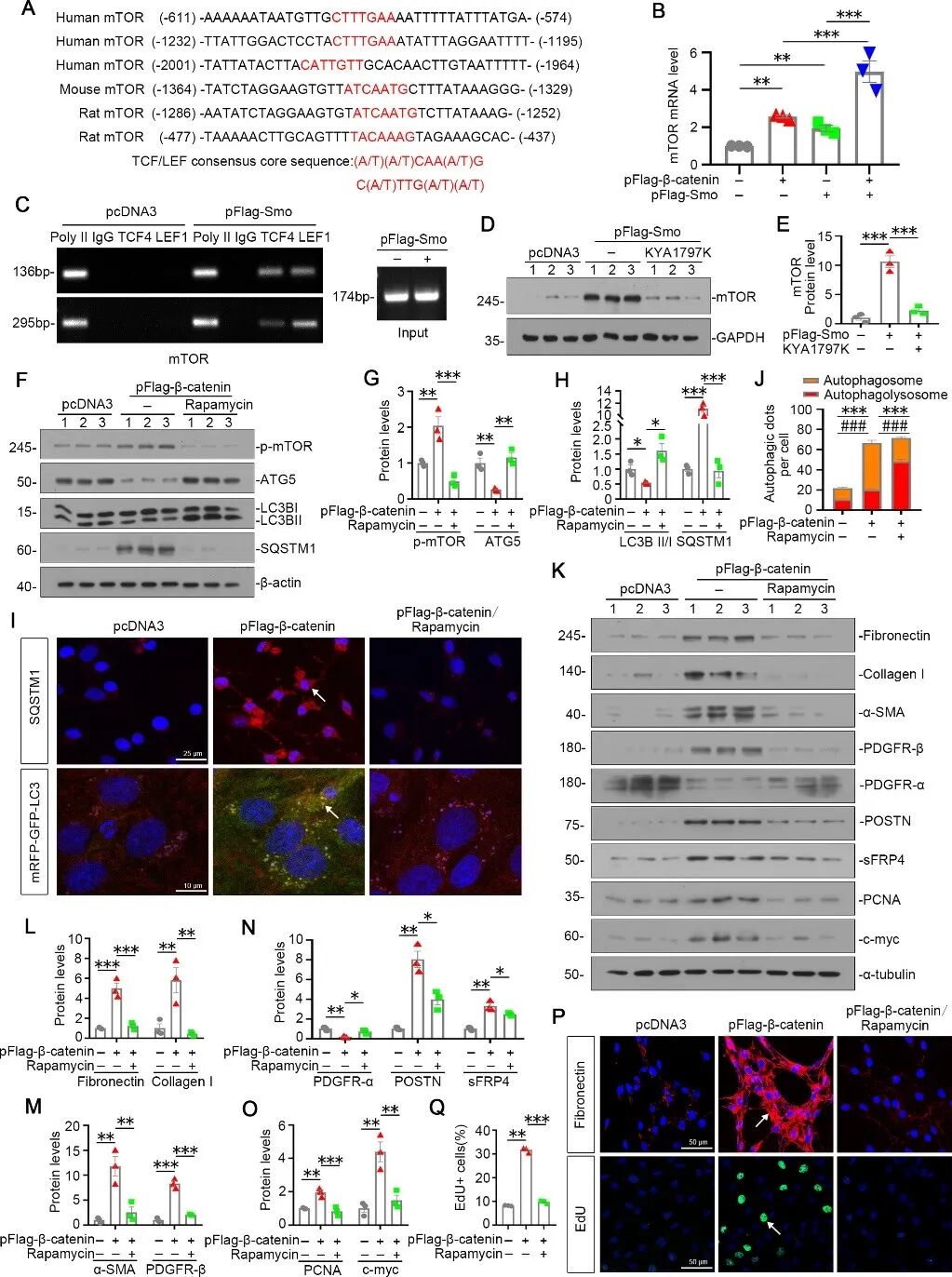
图5 Smo/β-catenin/ mTOR信号轴介导自噬缺陷,进而驱动肌成纤维细胞转化
随后,研究人员构建成纤维细胞特异性β-catenin敲除小鼠(β-catCKO)并进行 UUO 手术,发现敲β-catCKO小鼠肾间质纤维细胞β-catenin表达被有效抑制,肌成纤维细胞活化与肾间质纤维化显著减轻,相关纤维化标志物表达明显下调,提示成纤维细胞中β-catenin对肌成纤维细胞活化及肾脏纤维化至关重要。进一步单细胞测序及机制分析显示,β-catenin敲除可降低成纤维细胞与肌成纤维细胞比例、下调促纤维化通路,并通过抑制mTOR信号恢复细胞自噬,改变成纤维细胞分化轨迹,使其偏向肾脏结构修复,表明β-catenin可通过抑制自噬促进成纤维细胞向肌成纤维细胞转化,进而驱动肾脏纤维化。(图6)
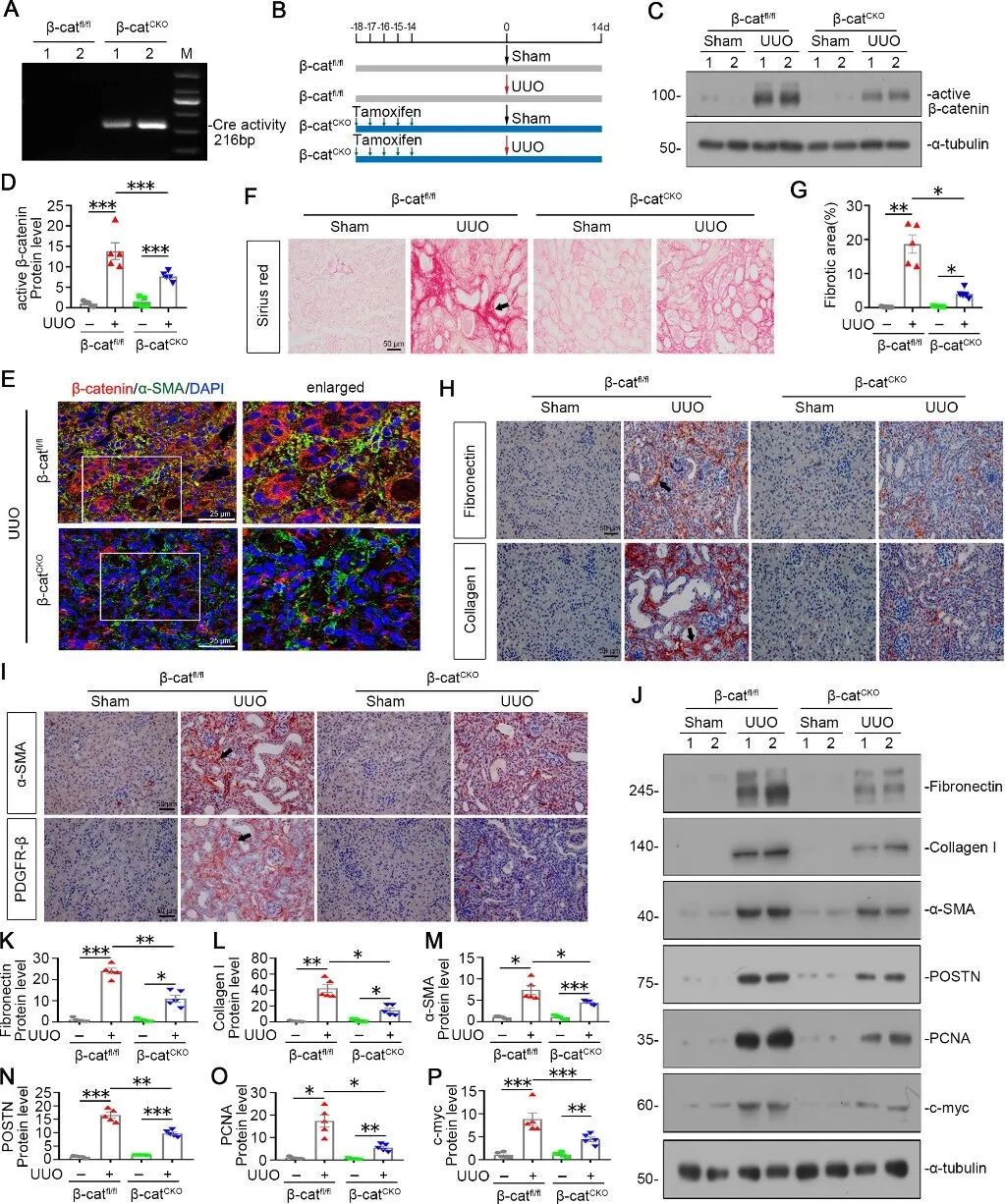
图6 成纤维细胞中敲除β-catenin可预防肾纤维化
最后,通过在已建立的UUO小鼠模型中给予Smo拮抗剂NVP-LDE225治疗,研究人员发现:NVP-LDE225可有效抑制肾间质成纤维细胞中Smo及活性β-catenin的表达,降低纤维细胞增殖;同时,该处理显著增强了成纤维细胞的自噬能力,表现为p-mTOR和SQSTM1表达下调、LC3B斑点增多、自噬空泡增加。RNA-seq及GSEA分析进一步证实,NVP-LDE225处理抑制了Hedgehog信号及非经典Wnt通路。这些结果表明,靶向Smo可通过抑制β-catenin、恢复自噬功能来阻断肌成纤维细胞活化,在已建立的纤维化模型中仍具有治疗潜力。(图7)
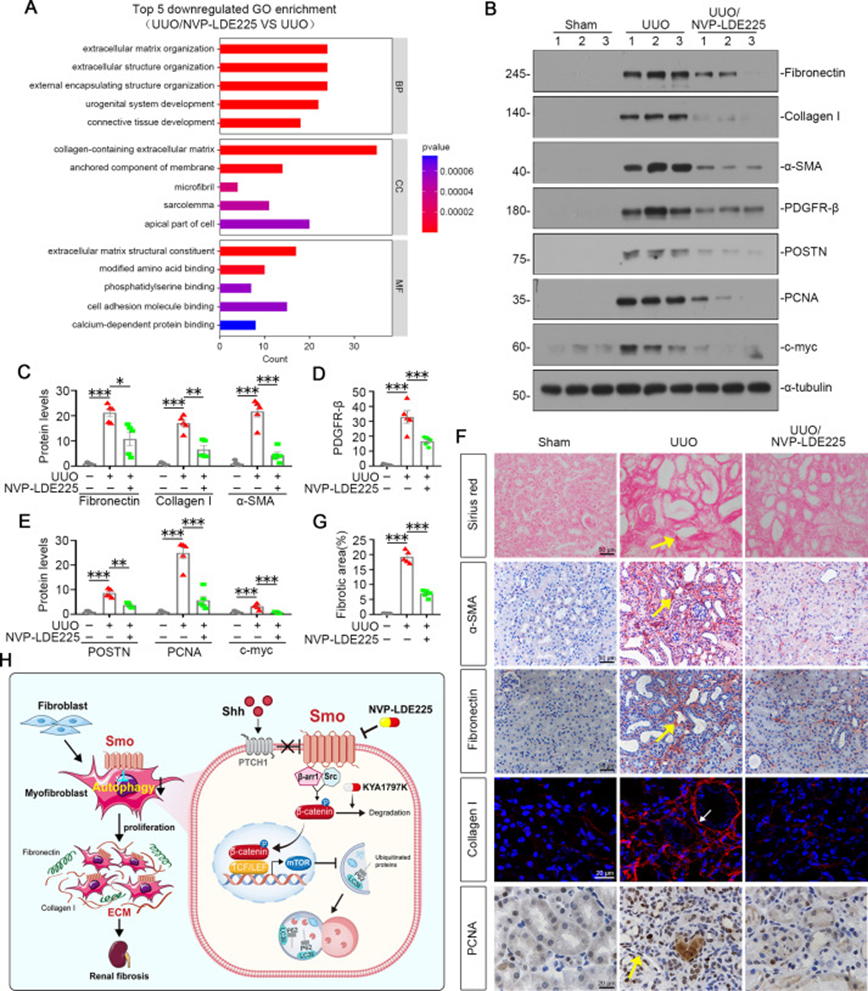
图7 NVP-LDE225显著改善UUO小鼠的肾纤维化
文章结论与展望
综上所述,本研究首次揭示了Smo通过β-arrestin 1/Src/β-catenin通路抑制成纤维细胞自噬,从而驱动肌成纤维细胞活化及肾纤维化的新机制。在多种CKD模型及原代细胞中证实了该通路的致病作用,并发现临床药物NVP-LDE225在已建立的纤维化模型中可通过恢复自噬有效延缓疾病进展。该研究为靶向成纤维细胞自噬治疗肾纤维化提供了新的理论基础和潜在干预策略。
来源:KidneyCode
查看更多