查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





71岁老年男性,主诉吞咽困难伴腹痛2月余。
2022年6月起无明显诱因出现吞咽困难,伴有恶心、呕吐、反酸及腹痛,服用胃药可缓解,2022年7月吞咽困难症状进行性加重。起病后精神、睡眠、食欲一般,二便基本正常,体重下降3kg。
2017年因“腰椎间盘”突出,行手术治疗。
哥哥67岁患“肿瘤”,具体不详。
查体:KPS 90分,全腹部轻压痛,无反跳痛,腹部可触及肝肿大,余无特殊。
肿瘤标志物:AFP 19656ng/mL,CEA 131ng/mL,CA19-9 38.7U/mL,CA125 正常范围。
胃镜(外院):食管、贲门见一不规则隆起,表面溃疡,占据管腔2/3。
胸腹盆CT:食管胃结合部管壁明显增厚并形成肿物,食管下段旁、胃小弯侧、胃左血管旁、肝门区多发淋巴结转移,肝内多发转移瘤。
病理:(食管贲门)镜下符合中分化腺癌,Lauren 分型:肠型。免疫组化:HER2(0),MLH1(+),PMS2(+),MSH2(+),MSH6(+),AFP(+)。
基因检测(肿瘤组织):TMB-L,MSS,检出AXIN1 c.1166C>A,TP53 c.828delCinsGT,NOTCH1 c.1070T>C突变。
食管胃结合部中分化腺癌多发肝转移,cT4N2M1 Ⅳb期;Lauren分型:肠型;HER2(-),MSS,TMB-L
(1)一线治疗
鉴于产AFP胃癌现有指南未单独列出个体化治疗方案,且既往小样本研究提示免疫联合化疗可能带来生存获益,结合现有指南和证据,为患者制定免疫联合化疗的姑息一线方案。
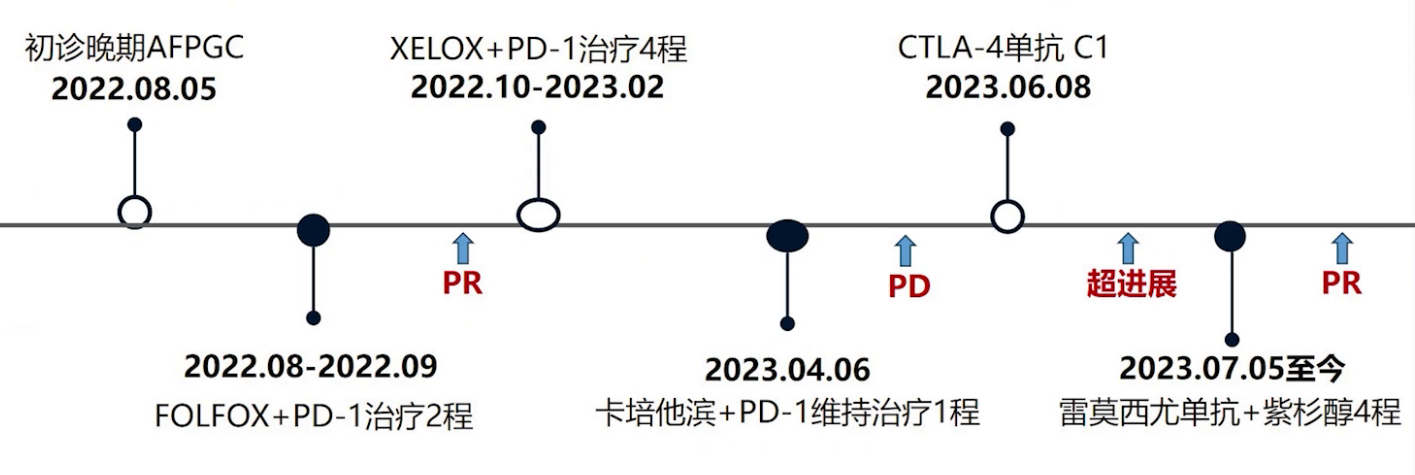
2022年8月-2023年2月,患者接受替吉奥+奥沙利铂+帕博利珠单抗治疗,期间因治疗方便,化疗方案从FOLFOX调整为XELOX。治疗期间患者耐受性良好,仅出现Ⅰ度周围神经损伤。影像学显示肝脏转移病灶缩小,吞咽困难及腹胀症状缓解,肿瘤标志物CA19-9从接近20000ng/mL降至293ng/mL。2023年4月,患者开始卡培他滨+帕博利珠单抗维持治疗。
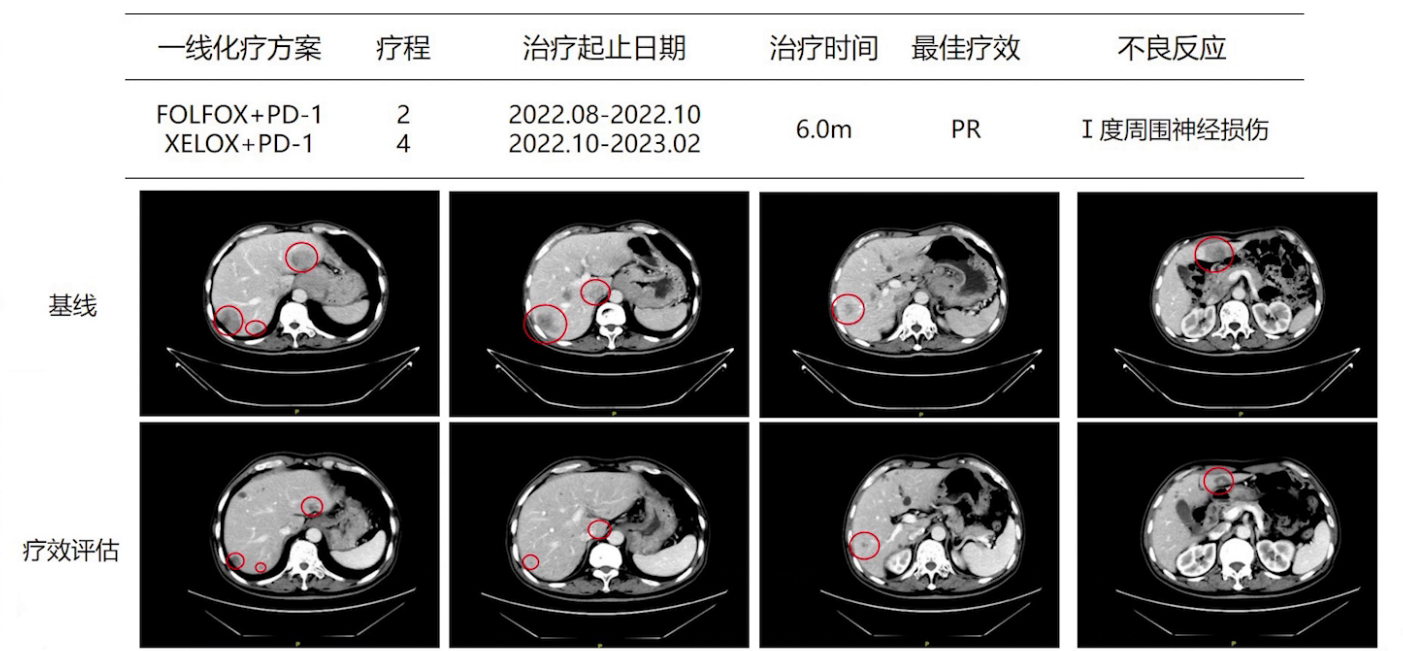
(2)二线治疗
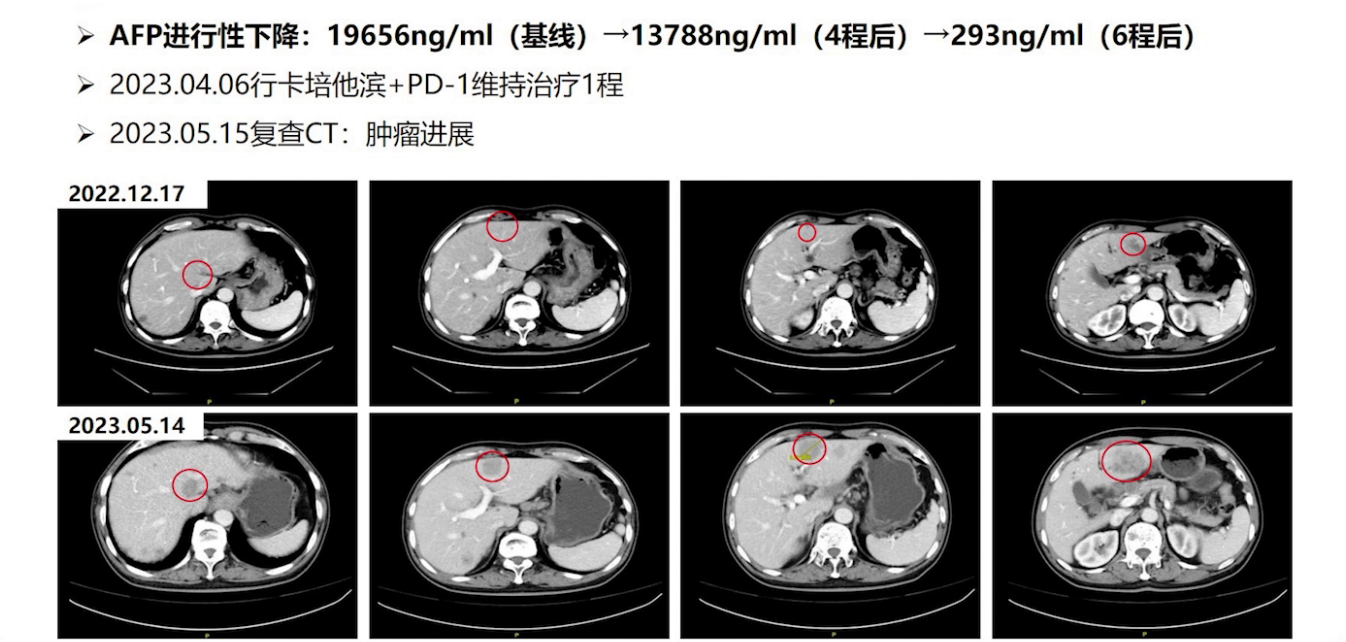
2023年5月,患者复查CT提示肝转移灶增大,评估为PD。经筛选,患者符合科室开展的CTLA-4单抗C392临床研究,于6月8日入组并接受治疗。3周左右,患者出现腹胀、纳差、乏力,当地医院检查示肝酶与胆红素轻度升高,返院检查发现肿瘤标志物明显升高,AFP>121000ng/mL,CA19-9与CEA也显著升高,CT显示肝内转移病灶增多增大,考虑出现免疫治疗超进展。

(3)三线治疗
针对免疫治疗超进展,经与家属沟通,结合指南和循证医学证据,选择化疗联合抗血管生成治疗策略,考虑患者体能状态及器官功能,采用周疗的紫杉醇联合雷莫芦单抗治疗。
从2023年7月起,患者接受4个疗程治疗,期间出现一过性痰中带血、鼻衄及Ⅲ度白细胞下降,但腹胀和纳差症状迅速缓解,复查CT显示肝脏转移病灶缩小减少。

查看更多
专家点评
本病例分享了一例AFP升高的胃癌肝转移患者的诊疗全程,其过程凸显了在免疫治疗时代下,对此类高度异质性、预后不良的晚期胃癌进行个体化全程管理的复杂性与关键决策点。
首先,该病例的诊断具有挑战性。AFP升高的胃癌是一个独特的亚群,涵盖肝样腺癌、伴肠母细胞分化的腺癌等多种少见病理类型,恶性程度高,异质性强。在诊断时需排除肝炎、肝硬化、妊娠及其他生殖细胞肿瘤等非胃癌疾病。
治疗层面,本例的核心启示在于免疫治疗时代的全程药物管理与策略布局。患者初始按照HER2阴性胃癌标准,接受了一线免疫联合化疗。当治疗失败后,临床面临的关键问题包括:免疫治疗进展后,能否进行“再挑战”。本例尝试了更换PD-1抑制剂的单药治疗,但患者迅速出现疾病暴发式进展,符合“超进展”特征。这提示,在胃癌中基于现有证据,免疫治疗单药再挑战疗效有限且风险高,应极为谨慎。
应对超进展,本例迅速转换策略,采用了以细胞毒药物联合抗血管生成治疗为主的方案。患者症状及影像学均获得快速、显著的改善。这一成功转折引出了另一个重要思考,即在一线免疫治疗暴露后,后线使用抗血管生成药物联合化疗,可能产生协同增效作用。一些真实世界研究也观察到此现象,其背后的机制值得深入探索,也为临床决策提供了正向提示。