查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





研究名称:替雷利珠单抗联合化疗新辅助治疗IB3/IIA2期宫颈癌(NATIC):一项前瞻性、单臂、Ⅱ期研究[Tislelizumab (anti-PD-1) plus chemotherapy as neoadjuvant therapy for patients with stage IB3/IIA2 cervical cancer (NATIC):a prospective, single-arm, phase II study]
发表期刊:《信号转导与靶向治疗》(Signal Transduction and Targeted Therapy, IF=52.7)
通讯作者:郝继辉 刘文欣
主要作者单位:天津医科大学肿瘤医院
宫颈癌是全球女性恶性肿瘤第四大发病和死亡原因,其中LACC患者(IB3和IIA2-IVA期宫颈癌)约占37%。尽管以顺铂为基础的同步放化疗(CCRT)已成为标准治疗,但仍有相当比例的患者出现复发或转移。NATIC研究展示了替雷利珠单抗联合化疗的新辅助治疗方案在IB3/IIA2期宫颈癌中显示出令人鼓舞的抗肿瘤活性、安全可控,这为局晚期宫颈癌(LACC)患者提供了一种新的治疗选择。
NATIC研究是一项前瞻性、单臂、Ⅱ期临床研究,该研究创新性地评估了抗PD-1抗体替雷利珠单抗联合化疗作为新辅助治疗方案,在初治IB3/IIA2期LACC患者中的疗效和安全性。
本研究共纳入30例患者(IB3期11例,IIA2期19例),所有患者均完成3周期新辅助免疫联合化疗并接受了根治性手术。对患者术后病理进行评估,研究结果显示:主要终点pCR(病理完全缓解)率为66.7%(20/30),另有4例(13.3%)达到主要病理缓解(MPR),合计满意病理缓解(OPR,定义为pCR+MPR)率为80.0%(24/30)。客观缓解率(ORR)达90.0%,其中56.7%为完全缓解(CR)。中位随访时间14.7个月时,18个月无病生存率(DFS)为90%。术后需要接受辅助治疗的不满意病理缓解(non-OPR)患者仅占20%。研究结果显示,替雷利珠单抗联合化疗新辅助治疗具有良好的抗肿瘤活性和安全性,大大降低了IB3/IIA2期LACC患者术后辅助治疗的应用(包括同步放化疗、放疗和化疗),降低了患者的经济负担及术后辅助治疗带来的并发症,有望为LACC的治疗提供新的选择。
患者的基线特征、肿瘤应答及病理应答情况
值得注意的是,影像学与病理评估一致性仅56.7%,7例影像学评估为PR的患者术后病理评估为pCR,5例影像学评估为CR的患者术后病理仍发现有残存肿瘤。pCR患者的PD-L1 CPS评分显著高于未达到pCR(non-pCR)的患者(中位数 77.5 vs 8.5,P < 0.001),但是1例PD-L1 CPS <1 的患者术后病理评估达到了pCR。接受延迟手术(手术时间间隔>6 周)的患者 pCR 率较高,达到 83.3%,该结果表明在新辅助免疫化疗后4-6周后进行手术可能会改善病理反应。
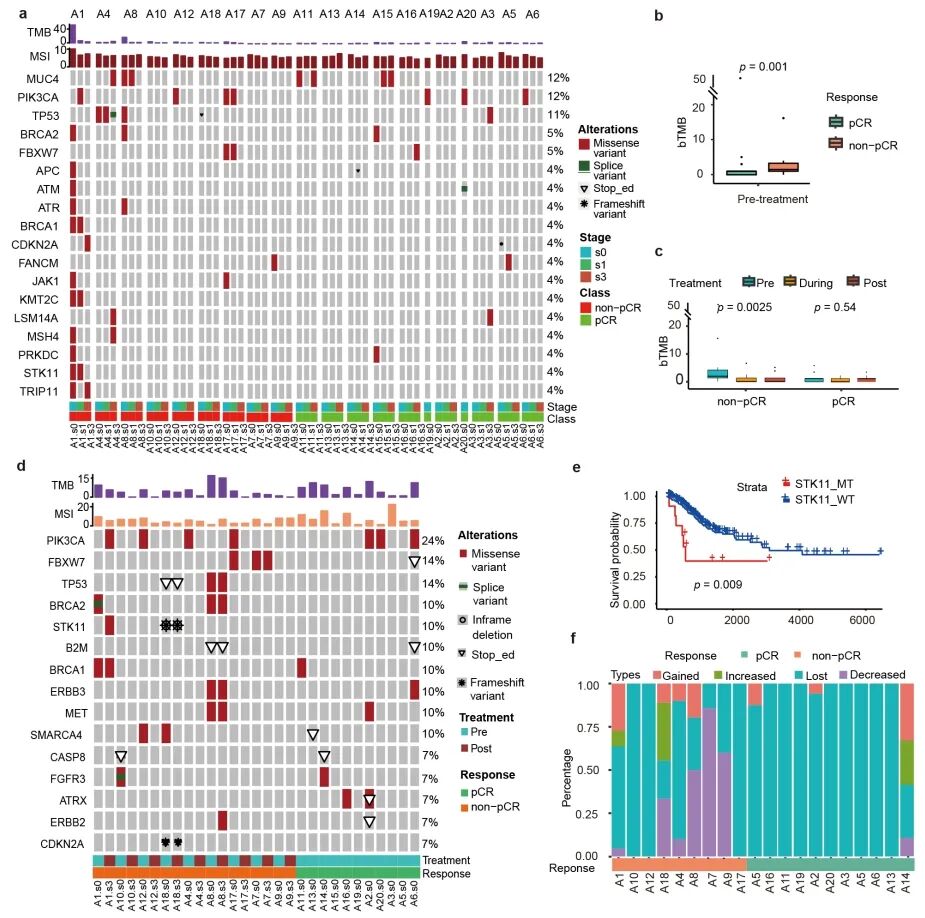
通过对血液(上)和肿瘤组织(下)样本的NGS测序分析,探究了基因组突变与新辅助治疗疗效之间的关系
探索性生物标志物分析显示,non-pCR 组的基线 bTMB 显著更高,表明 ctDNA 检测可以为预测治疗效果提供有价值的见解。进一步分析基线肿瘤组织中的免疫相关特征显示,pCR组具有更高水平的溶细胞特征、CD8+ T 细胞、T 细胞耗竭和 IFN-γ 特征,表明其肿瘤免疫微环境更“热”,而IFN-γ可能是影响新辅助免疫治疗疗效的生物标志物,并可能诱导有效且持久的抗肿瘤免疫反应。免疫细胞丰度分析显示,与non-pCR组相比,pCR组的B 细胞、CD8+ T 细胞、CD4+记忆T细胞和NK细胞水平显著更高。这一发现与在pCR组基线样本中观察到的更高免疫基因表达水平一致。从临床结果到实验室分析,分子层面的见解不仅验证了观察到的临床反应,而且揭示了新辅助免疫化疗后手术潜在获益的生物学机制。
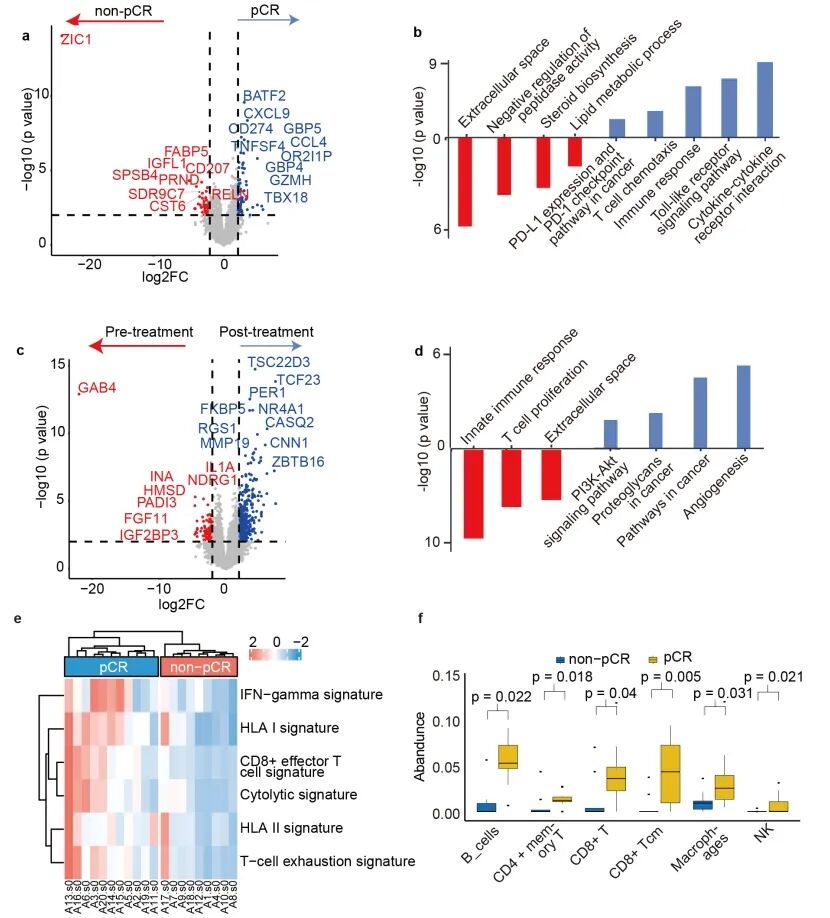
不同应答组之间差异基因、免疫信号及肿瘤微环境的比较
安全性方面,最常见的 TRAEs 是淋巴细胞减少(27/30,90.0%)、贫血(21/30,70.0%)和低白蛋白血症(21/30,70.0%),仅 1 例患者(3.3%)出现≥3 级免疫相关不良事件(irAE) ,该患者在术后 2 周出现周围神经病变(包括肢体麻木和腿部无力),进展为吞咽和呼吸困难,最终诊断为格林-巴利综合征,经大剂量皮质类固醇治疗后症状明显改善。
宫颈癌是全球女性恶性肿瘤第四大发病和死亡原因,其中LACC患者(IB3和IIA2-IVA期宫颈癌)约占37%。尽管以顺铂为基础的同步放化疗(CCRT)已成为标准治疗,但仍有相当比例的患者出现复发或转移。近年来,免疫检查点抑制剂(ICIs)联合治疗策略为LACC带来了新希望。KEYNOTE-A18研究推动了CCRT联合帕博利珠单抗用于新诊断的III-IVA期LACC患者的治疗模式改变,而新辅助免疫化疗后进行根治性手术能为IB3/IIA2期LACC带来多大程度的临床价值,仍需进一步的探讨。
NATIC是一项前瞻性、单臂、Ⅱ期临床研究,该研究创新性地评估了抗PD-1抗体替雷利珠单抗联合化疗作为新辅助治疗方案,在初治IB3/IIA2期LACC患者中的疗效和安全性。NATIC研究达到了预设终点,替雷利珠单抗联合化疗的新辅助治疗方案在IB3/IIA2期LACC患者中显示出令人鼓舞的抗肿瘤活性(pCR率高达66.7%),安全性可控,本研究数据支持该联合方案用于LACC新辅助治疗的可行性。本研究获得天津医科大学肿瘤医院“358计划”临床试验基金的支持,后续拓展队列研究目前仍在继续进行中,长期生存数据将在后续报告中更新。
天津医科大学肿瘤医院妇科肿瘤科
主任医师 肿瘤学博士 硕士生导师
中国抗癌协会卵巢癌专业委员会委员
中国抗癌协会中西整合宫颈癌专业委员会常务委员
中国医药教育协会妇科肿瘤医学教育委员会常务委员
天津市抗癌协会妇科肿瘤专业委员会副主任委员
天津医科大学党委副书记、校长
天津医科大学肿瘤医院党委副书记、院长
教授、主任医师、博士生导师
国家杰出青年科学基金获得者
科技部重点领域创新团队带头人
百千万人才工程国家级人选
国家卫生健康突出贡献中青年专家
国家恶性肿瘤临床医学研究中心执行副主任、药物成药性评价与系统转化全国重点实验室副主任、天津市消化系统肿瘤重点实验室主任
国家肿瘤质控中心胰腺癌质控专家委员会主任委员
中国抗癌协会副理事长、天津市抗癌协会理事长
中国抗癌协会肿瘤精准治疗专业委员会候任主委
中国抗癌协会胰腺癌专业委员会副主任委员
Cancer Biology & Medicine、《中国临床肿瘤》执行主编
以第一完成人获得教育部高等学校科学研究优秀成果奖(科学技术)一等奖、天津市自然科学特等奖、天津市科技进步奖一等奖、华夏医学科技奖科学技术一等奖、中国抗癌协会科技奖一等奖和中华医学科技奖医学科学技术奖、教育部霍英东教学成果奖等科技奖励10余项
主持国家重点研发计划、国自然重点项目等省部级以上课题10余项
以第一作者或通讯作者(含共同)在Cancer Cell、Cell Res.、Cancer Discov.、Gut、Gastroenterolog、Sci Adv.、Nat. Commun.、J. Exp. Med.等权威期刊发表论文百余篇
每一项临床研究都倾注着研究团队的心血结晶。学习过后,您是否有所收获?或有疑问想与主创团队分享?请在评论区留言,期待与您交流!

整理丨中国医学论坛报 胡岳
查看更多