查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





2024年9月13-17日,2024年欧洲肿瘤内科学会(ESMO)年会于西班牙巴塞罗那正式召开。作为肿瘤领域最具权威的年度盛会之一,本届年会再次云集全球肿瘤大咖、汇聚领域最新进展。
在当地时间9月13日的上消化道肿瘤优选论文专场中,由中国药科大学附属南京天印山医院秦叔逵教授和复旦大学附属中山医院樊嘉院士共同领衔的研究“A Phase Ib/II Study to Assess the Safety and Efficacy of PM8002/BNT327 in Combination with Nab-Paclitaxel for First Line Treatment of Locally Advanced or Metastatic Triple-Negative Breast Cancer”,由秦叔逵教授线上进行了口头报告。现将研究内容编译整理如下,以飨读者。
Abstract Title:Iparomlimab and tuvonralimab (QL1706) with bevacizumab and/or chemotherapy in first-line (1L) treatment of advanced hepatocellular carcinoma (aHCC): A randomized, open-label, phase II/III study (DUBHE-H-308)
研究标题:艾帕洛利单抗(Iparomlimab)和托沃瑞利单抗(QL1706)联合贝伐珠单抗和/或化疗作为晚期肝细胞癌(aHCC)的一线(1L)治疗:一项随机、开放标签、Ⅱ/Ⅲ期研究(DUBHE-H-308)
摘要号:LBA38
时间:2024年9月13日,CEST
专场:上消化道肿瘤优选论文专场
QL1706是一种双功能MabPair产品,由两种工程化单克隆抗体(抗PD-1和抗CTLA-4)组成。QL1706联合贝伐珠单抗(bev)作为aHCC的一线治疗在1b/2期研究中显示出有希望的抗肿瘤活性和良好的安全性。因此,DUBHE-H-308研究(NCT05976568)的Ⅱ期部分研究了QL1706与bev和/或化疗(chemo)治疗aHCC的一线治疗,此摘要展示了研究结果。
患者随机分配(1:1:1:1)至组1:QL1706(7.5 mg/kg,Q3W)+bev(15 mg/kg,Q3W)+化疗(aHCC方案,即奥沙利铂85 mg/m2加卡培他滨1000 mg/m2,Q3W,最多4个周期);组2:QL1706+bev;组3:QL1706+化疗,或组4:另一种PD-1抗体信迪利单抗(200mg,Q3W)+bev。主要研究终点是研究者根据RECIST v1.1评估的客观缓解率(ORR)和安全性。
共120例患者入组。截至2024年7月12日,中位随访时间为6.7个月。基线特征四组基本平衡。ORR和疾病控制率(DCR)见表。数据截止时无进展生存(PFS)期尚不成熟。上述4组患者6个月PFS率分别为78.5%、64.3%、53.8%和50.3%。4组患者中≥3级治疗相关不良事件发生率分别为46.7%、50.0%、46.7%和37.9%。只有组4中例患者死于与治疗相关的肝功能衰竭。
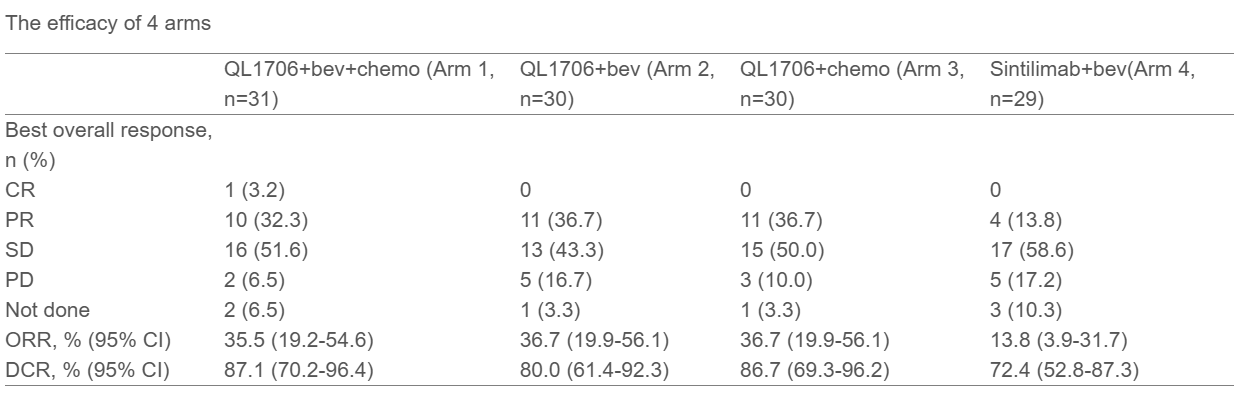
在DUBHE-H-308研究的2期部分中,QL1706 + bev联合化疗一线治疗aHCC显示出令人鼓舞的初步疗效和可管理的安全性。独立数据监测委员会选择QL1706 + bev + XELOX作为未来3期研究的研究组。
-----今日肿瘤编译整理自ESMO官网-----
(最新数据以大会现场报告为主)


查看更多