查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





林潮双 中山大学附属第三医院
目前世界上尚无治疗乙型肝炎(简称乙肝)病毒(HBV)感染相关疾病的特效药,接种乙肝疫苗仍是控制、预防乙肝最有效的方法。然而,自20世纪80年代应用乙肝疫苗以来,无论是血源性疫苗还是基因重组疫苗,在按照WHO推荐的0、1、6个月免疫程序进行全程免疫后,仍然有2%一15%的接种者HBV表面抗体(抗-HBs)始终阴性或达不到保护阈值(>10 mIU/ml),乙肝疫苗对此部分人群没有产生有效的保护作用,尤其是成年人免疫效果往往不如婴幼儿。为探索行之有效的乙肝疫苗再免疫方案,本研究对100例无或弱应答成年人采用3种不同方法进行再免疫,并对不同方法再免疫的效果进行比较,结果报告如下。
研究对象与方法
1.研究对象:2005年9月至2007年12月在中山大学附属第三医院感染科门诊体检,有详细记录2年内乙肝疫苗接种史(至少完成1个标准免疫接种程序)的健康人群,酶联免疫吸附法检查HBV标志物5项指标(HBsAg、抗-HBs、HBeAg、抗-HBe和抗-HBc)均为阴性,肝功能检查正常者为研究对象。同时调查其脂肪肝史。
2.研究方法及接种方案:采用随机(数字表法)、开放性的研究方法,对符合研究方案的研究对象随机(数字表法)分为3组,每组乙肝疫苗复种程序均为0、1、6个月共3针,均于上臂三角肌予肌内注射。A组:共34例,其中男20例,女14例,年龄18-64岁,平均(35.94 ±12.44)岁,先予粒细胞-巨噬细胞集落刺激因子(granulocyte macrophage colony stimulating factor,GM-CSF)300μg皮下注射,次日开始按常规程序予乙肝疫苗接种,每次剂量为10μg;B组:共33例,其中男17例,女16例,年龄22-58岁,平均(33.42±8.85)岁,单纯乙肝疫苗接种,每次剂量为20μg;C组:共33例,其中男20例,女13例,年龄19-63岁,平均(29.30±10.38)岁,单纯乙肝疫苗复种,每次剂量为10μg。该研究均已取得受试对象的知情同意。
3.疫苗来源:10μg基因重组酵母乙肝疫苗,深圳康泰生物制品有限公司生产,批号为20051131,每支剂量5 μg/O.5 ml装;20μg基因重组酵母乙肝疫苗,由上海葛兰素史克生物制品有限公司生产(商品名:安在时),批号为XHBVB270AA,每支剂量20μg/1 ml装。均在有效期内使用。
4.采血及检测方法:在复种首针乙肝疫苗前及复种首针后第1、2、8个月(T1、T2、T8)对所有复种对象采集静脉血5 ml,在同一实验室、用同一仪器和方法、使用同一厂家试剂、固定检测人员严格按试剂盒说明进行抗-HBs检测。抗-HBs的检测使用Abbot/AxSYM AUSAB标准试剂盒,Abbot Park,IL USA所生产。
5.判定标准:抗-HBs滴度<10 mIU/ml为阴性,抗-HBs滴度10-100 mIU/ml为弱阳性,抗-HBs滴度≥100 mIU/ml为阳性。
6.统计学处理:采用SAS统计软件包进行统计学处理。计数资料采用t检验和方差分析(ANOVA),计量资料采用x2检验。以P<0.05为差异有统计学意义。
结 果
1.三组研究对象基线比较:见表1。
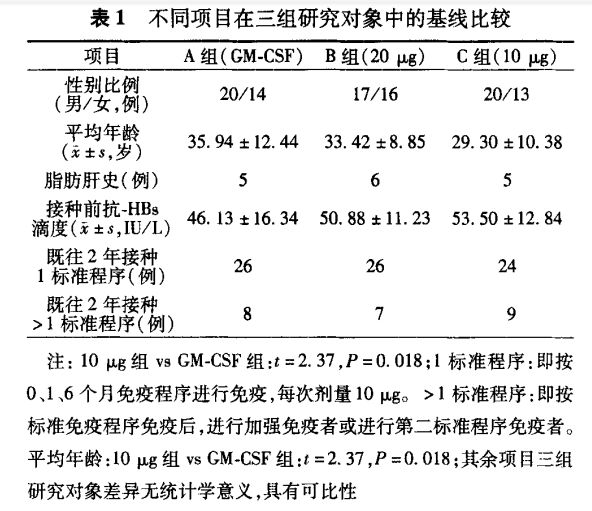
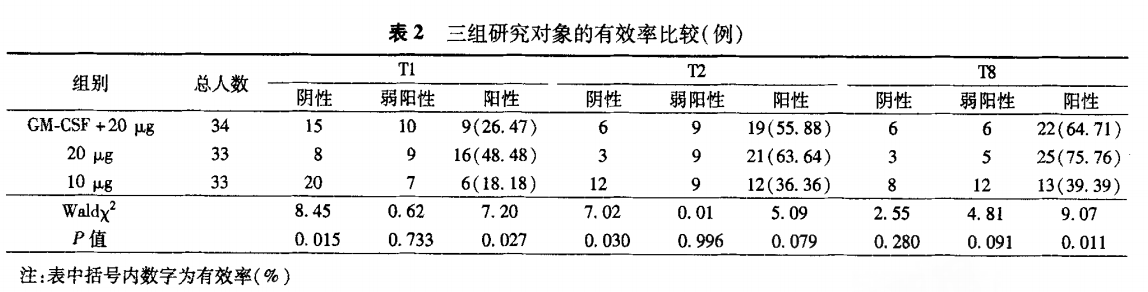
2.三组研究对象的有效率比较:见表2。
3.三组研究对象抗-HBs滴度比较:见表3。
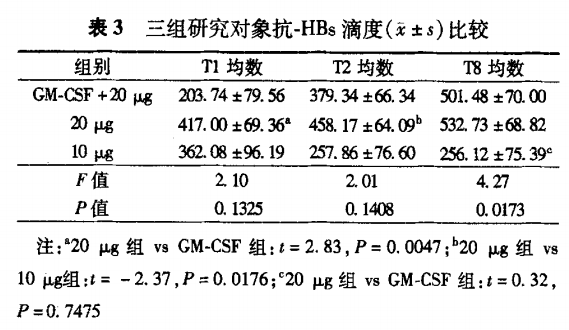
4.第3次免疫接种效果:对20μg组完成再免疫三剂后,抗-HBs仍呈阴性的3例研究对象,对其进行第4剂接种,剂量为40μg,仍使用20μg基因重组酵母乙肝疫苗(安在时),1个月后检测抗-HBs全部阳转抗-HBs滴度分别为1000、1000、962。
讨 论
鉴于目前对乙肝疫苗接种后无(弱)应答者,尤其那些顽固的无(弱)应答者,尚元确实有效的对策,国内外学者作了许多尝试。近年来,调节机体免疫机能的免疫调节剂正逐渐用于乙肝疫苗的研究中,许多研究者通过辅以某些免疫调节剂以期提高机体对乙肝疫苗免疫应答能力。但对无(弱)应答者在加强接种乙肝疫苗时联合使用免疫调节剂,其作用尚不明确。因此,有必要继续探索乙肝疫苗免疫接种的最佳方案。
乙肝疫苗接种后的免疫应答表明,免疫应答效果与年龄有关,年龄越小时接种,其免疫效果越好,成年人乙肝疫苗接种效果往往不理想。有学者认为不能把乙肝疫苗初种无应答者全部看作是完全无应答者,部分人可能是免疫应答迟缓者。另外,全程免疫接种抗体阳性者,5年内抗-HBs维持在较好的水平,5年后高水平抗-HBs应答率有所下降。因此,本研究选择2年内至少完成1个标准乙肝疫苗免疫接种程序,检查抗-HBs为无(弱)应答的健康人群为研究对象,以避免免疫应答迟缓者及随时间推移抗-HBs下降者。研究结果提示,复种(仍使用原标准剂量)、增加疫苗剂量、联合GM-CSF 3种方案再免疫均可提高部分无(弱)应答成年人的抗-HBs应答率,而增加疫苗剂量组和联合GM-CSF组方案免疫效果优于复种组,在完成再免疫三剂后,20μg组抗-HBs阳性率达75.76%,联合GM-CSF组达64.71%,均高于10μg组的39.39%(P=0.011)。三组研究对象的抗-HBs滴度显示,20μg组在T1时高于联合GM-CSF组,在T2时高于复种组,T8时20μg组和联合GM-CSF组均显著高于10μg组(P=0.0173)。进一步提示,增加疫苗剂量和联合GM-CSF方案抗体免疫水平均优于复种。
细胞集落刺激因子(CSF)是一组多潜能的造血细胞生长因子,临床上已广泛应用于促进化疗、放疗或骨髓移植后机体造血功能恢复的治疗。近年来研究发现,GM-CSF还具有促进免疫应答、调节免疫反应的作用。Sedegah等的实验研究表明用DNA疫苗与质粒GM-CSF共同注射与单独用DNA疫苗注射比较,前者抗体水平、IFN-ʏ分泌水平及CTL活性均较后者高,表明编码GM-CSF的质粒能增强DNA疫苗的免疫效果。周景仰等用G—CSF(粒细胞集落刺激因子)注射小鼠,发现rhG-CSF能明显增加外周血树实状细胞(DC)2型细胞的数量,从而介导以Th2为主的免疫应答。Singh等对慢性肾功能衰竭患者采用首次乙肝疫苗注射前先予rhGM-CSF注射,结果抗-HBs在3个月时为90.9%,在7个月时达100%,而且抗-HBs滴度也较不使用rhGM-CSF组高。但Hasan等以其同乙肝疫苗合用于健康人群免疫,却没表现出明显的佐剂效应。国内用CSF作为乙肝疫苗的佐剂应用于人体的研究鲜有报道。GM-CSF发挥免疫调节、促进免疫应答的机制尚未完全清楚,可能是通过作用于抗原提呈细胞,包括上调MHC lI和共刺激分子如B7的表达,并促使DC分化成熟。成熟DC具有丰富MHC、共刺激信号及其他黏附分子表达,有利于DC与其他免疫细胞信号的传递;同时DC分泌多种细胞因子,有利于激活其他免疫细胞,诱导出高效的免疫应答。至于CSF是促进以Th1介导的细胞免疫为主还是促进以Th2介导的体液免疫为主,目前还未有定论,仍需进行大量的研究加以探讨和验证。
对乙肝疫苗无应答者进行加强免疫是有效的措施,但仍不能完全消除无应答状态。本研究经过再免疫,20μg组仍有3例没有产生抗体应答,笔者对其进行了第4剂接种,剂量为40μg,仍使用重组乙肝疫苗,结果1个月后检测抗-HBs全部阳转,且抗体滴度很高。由此推测,若再免疫后没有出现抗体应答,是否应加大剂量继续免疫,有待进一步临床研究。
无(弱)应答者复种后抗体能否持续存在是评价复种效果的关键,通过提高免疫应答者的应答水平,可能会延长免疫保护期。本研究67例健康无(弱)应答者接受高剂量乙肝疫苗或标准剂量HBV疫苗加GM-CSF复种,2种方案在诱导无(弱)应答者抗体水平方面的作用是一样的。但抗体能持续多久,与原应答良好者相比,其保护率有无差别,关于无(弱)应答者复种后的远期效果有待于进一步的研究和验证。
查看更多