查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





基本资料
性别:男
年龄:47岁
主诉:“排便次数增多、便血3月余”于2015.12.31就诊于我院肛肠外科
现病史:3月余前无明显诱因出现排便次数增多、便血,呈鲜红色,遂于郑州市中心医院就诊,做电子纤维结肠镜检查,提示:距肛门14cm有一肿物,病理提示为“乙状结肠腺癌”。为求进一步诊治就诊于我院。
既往史/个人史/婚育史:无特殊
家族史:父母及一兄患有高血压
辅助检查
体格检查:
ps1评分:1分
实验室检查:
CEA1.65ng/mL
病理:
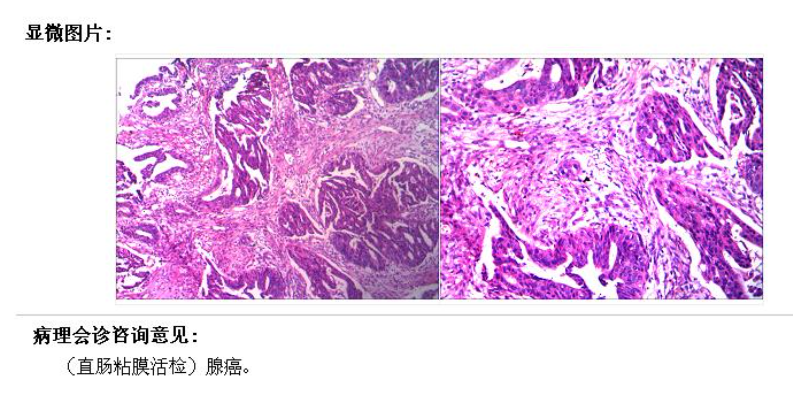
肠镜: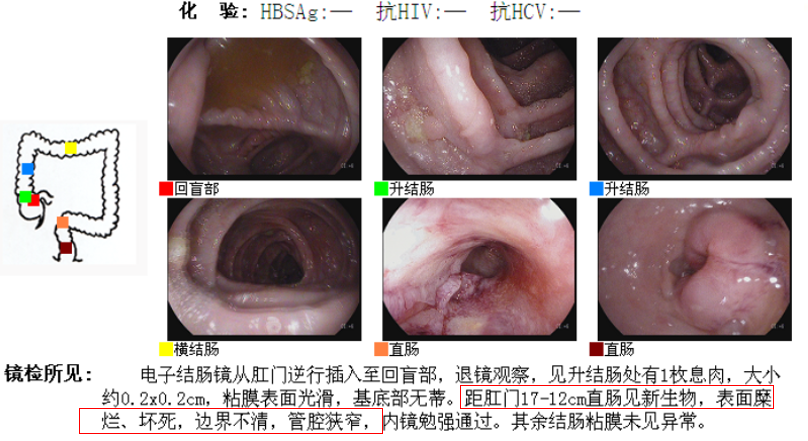
肠镜活检病理:
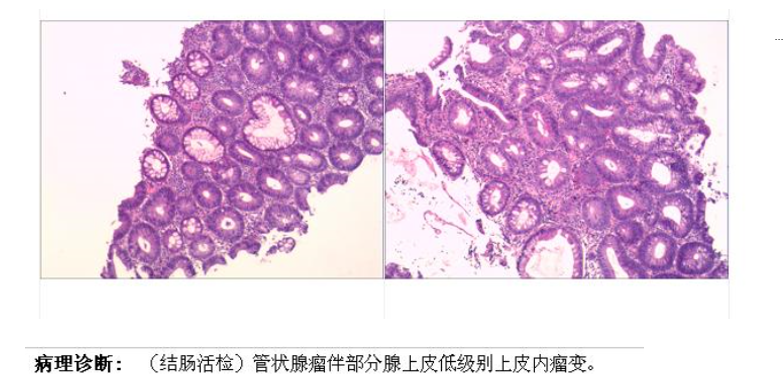
影像学检查:
术前盆腔增强MRI:
2016.01.01: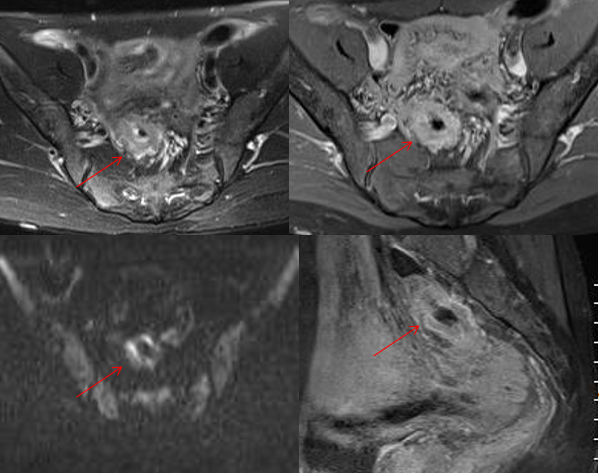
2016.01.02术前胸腹部增强CT: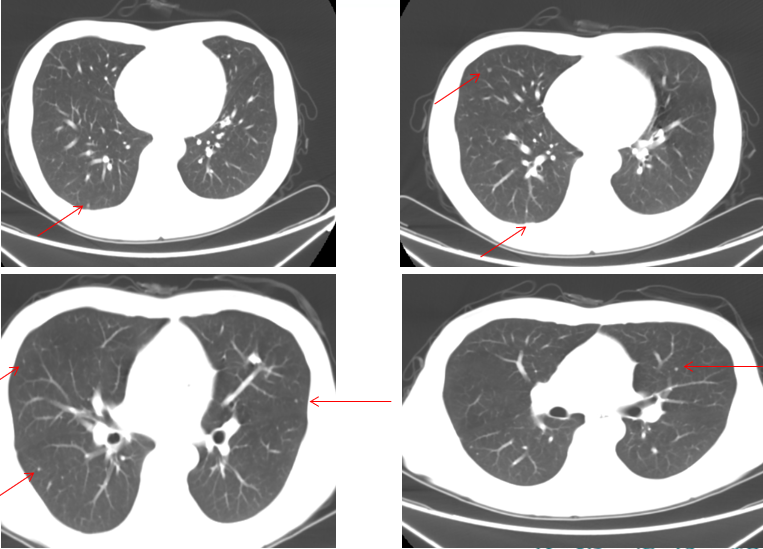
术前胸腹部增强CT:
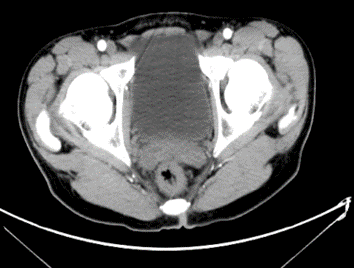
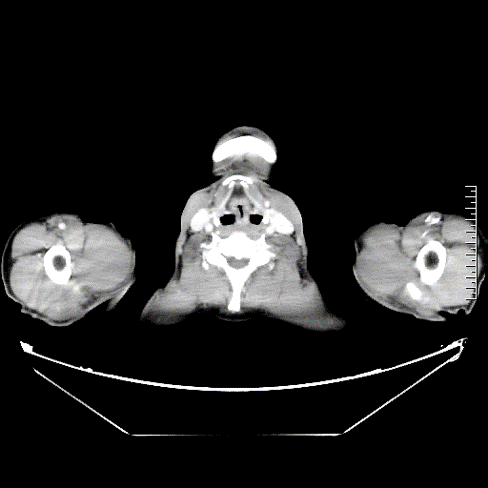
2016.01.08 PET-CT:
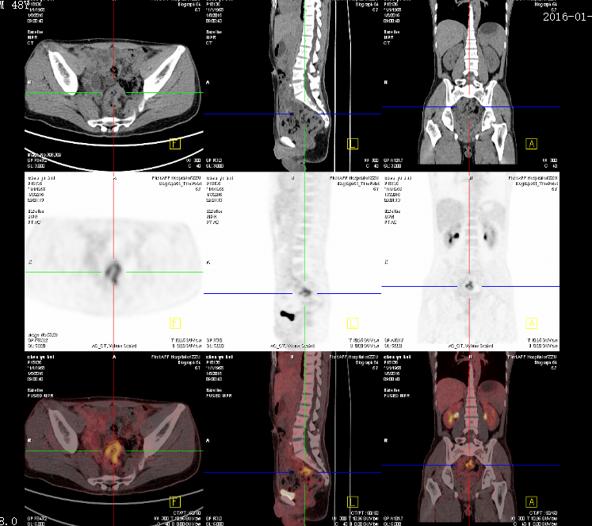
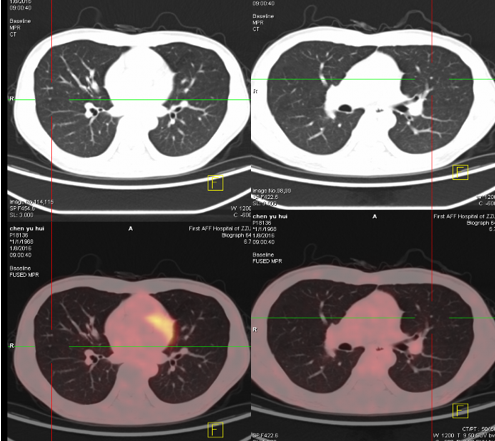

治疗过程:
外科治疗:
2016.01.11行“机器人辅助下直肠癌根治术+肠粘连松解术+扩肛术”
术后病理:
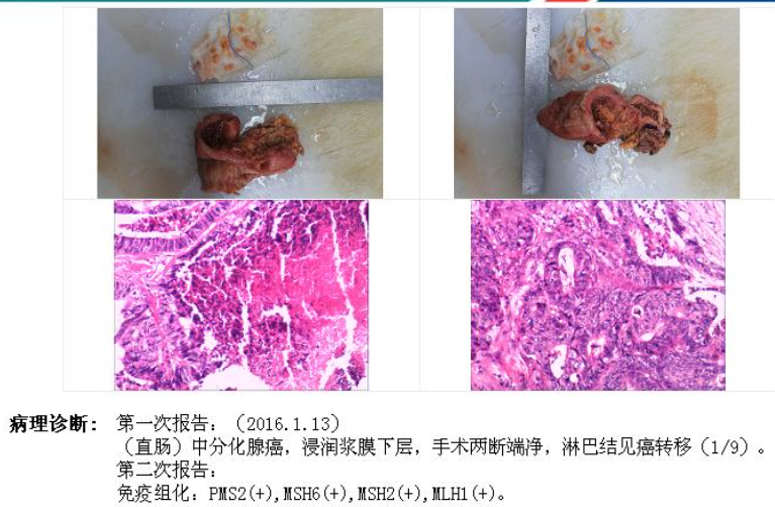
诊断:
直肠中分化腺癌术后 (pT3N1aM0,ⅢB期)
术后2016.01.23肠梗阻:
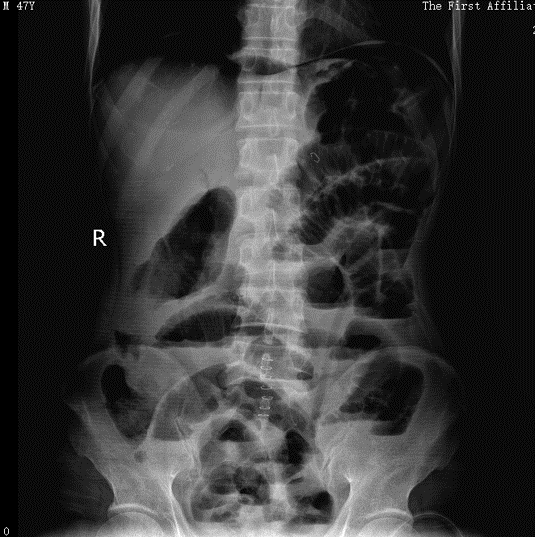
辅助化疗:
2016.02.25始给予“奥沙利铂+卡培他滨”1个周期。
2016.03.21始给予“奥沙利铂+替吉奥”6个周期,末次2019.08.03。
2016.08.29CT提示肺部转移 :
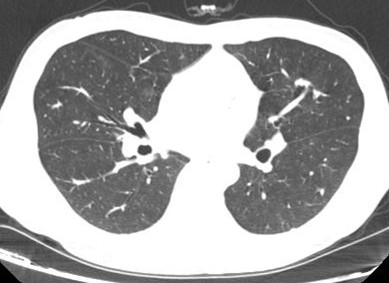
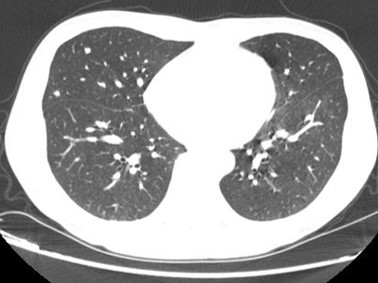
2016.09.05 PET-CT提示肺部多发转移
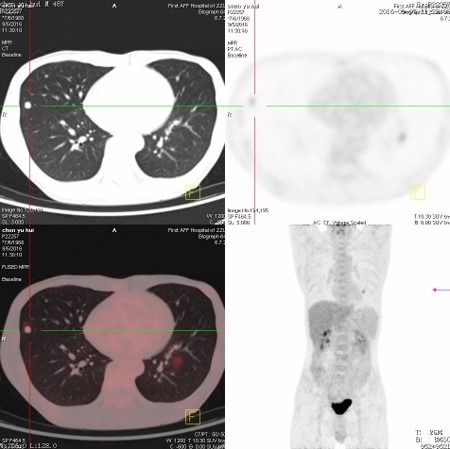
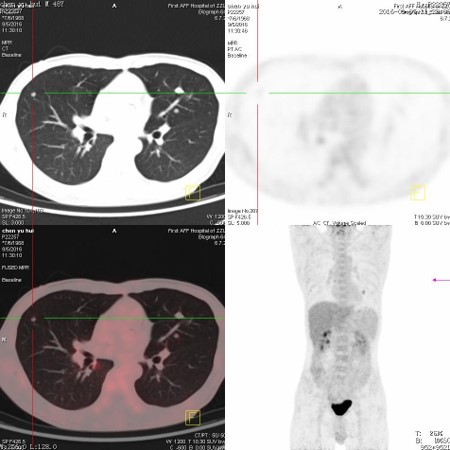
术后肠镜2016.09.07: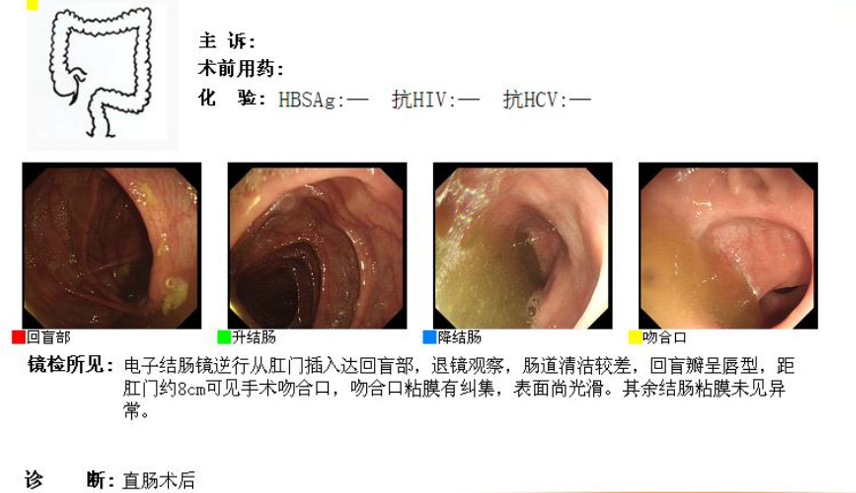
基因检测: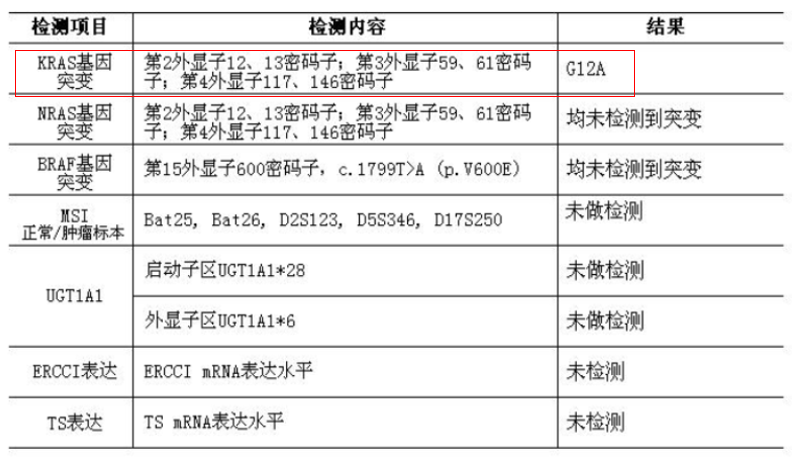 mCRC一线治疗:AVF2107g 研究
mCRC一线治疗:AVF2107g 研究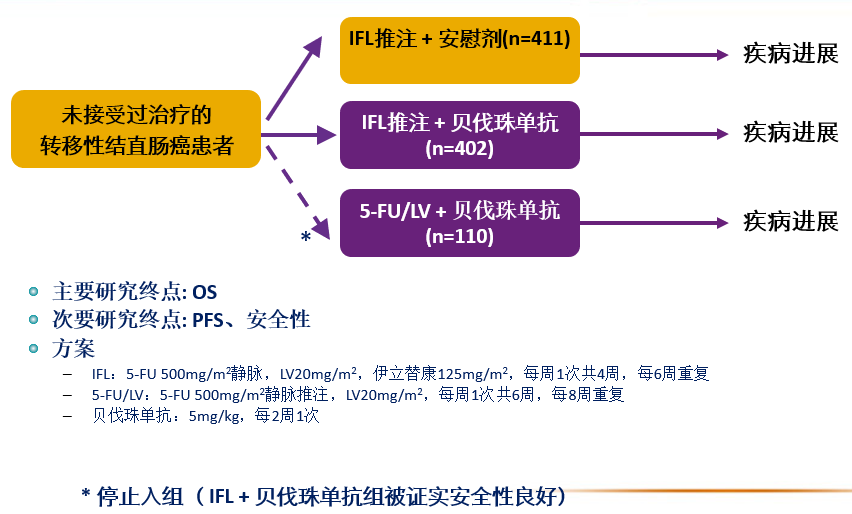
与单用化疗比较,贝伐珠单抗组显著改善PFS和OS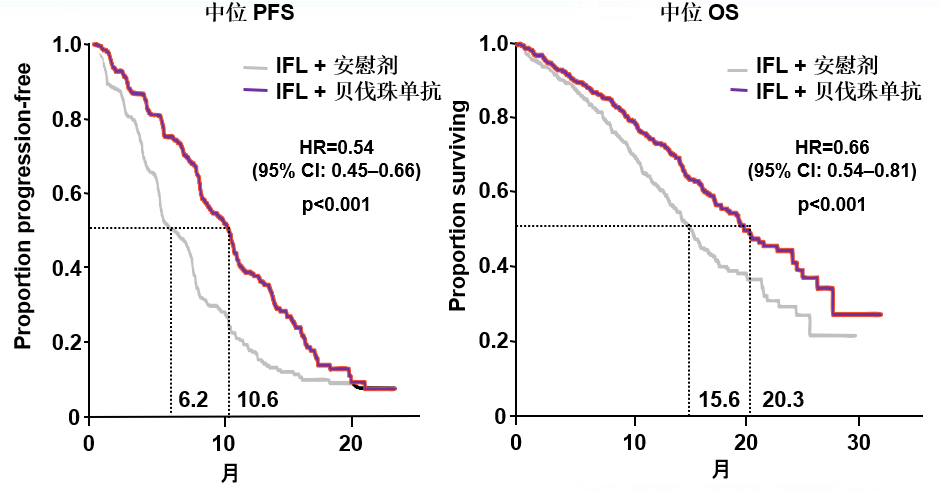 贝伐珠单抗组显著提高缓解率:
贝伐珠单抗组显著提高缓解率: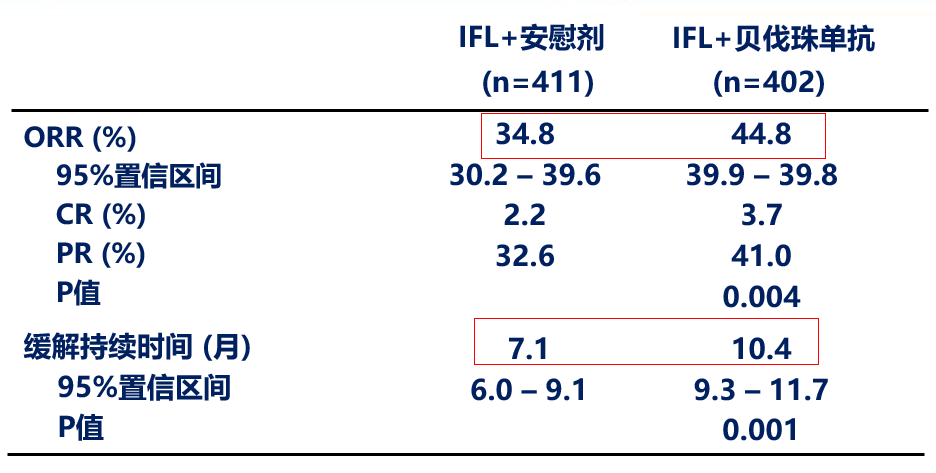
不论K-RAS状态,贝伐珠单抗治疗均可显著获得PFS的延长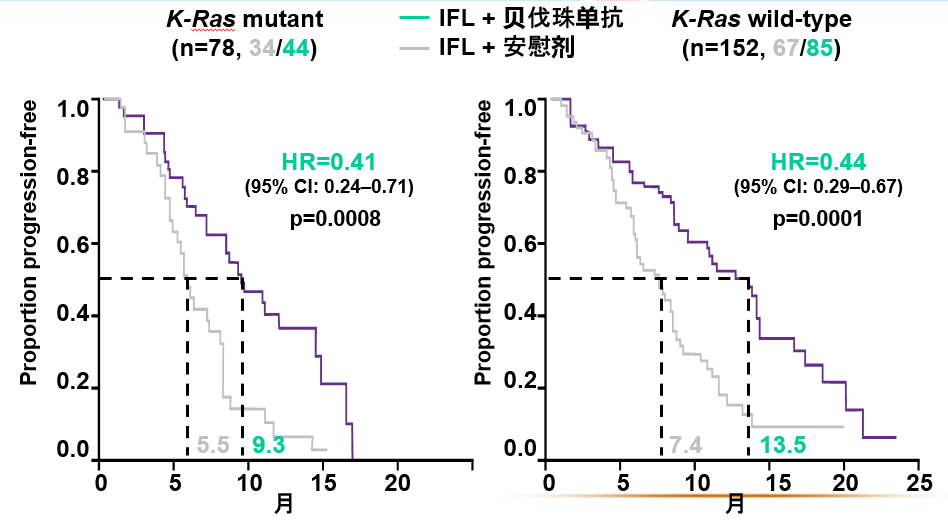
不论K-RAS状态,贝伐珠单抗均有OS的获益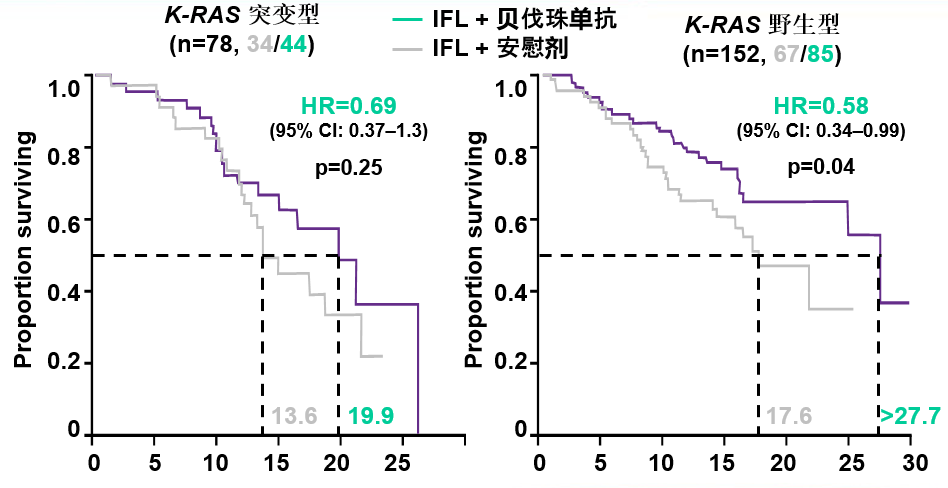 中国注册研究:ARTIST (BO20696)
中国注册研究:ARTIST (BO20696)
多中心、2:1随机对照、开放性临床研究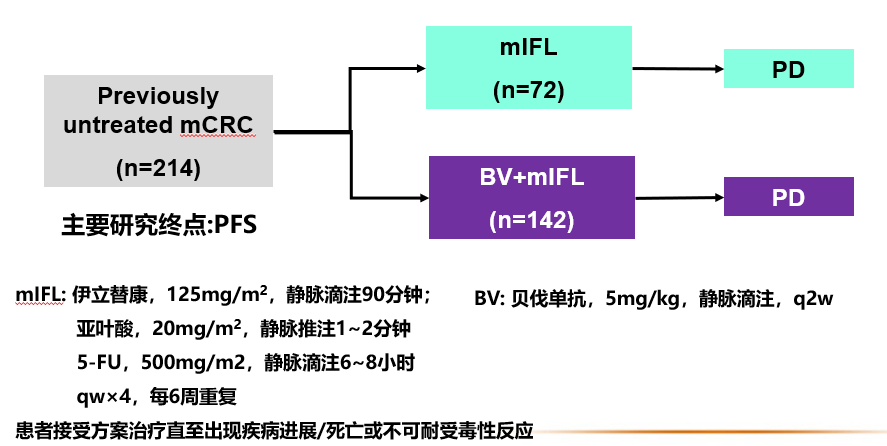 主要研究终点:无进展生存期
主要研究终点:无进展生存期
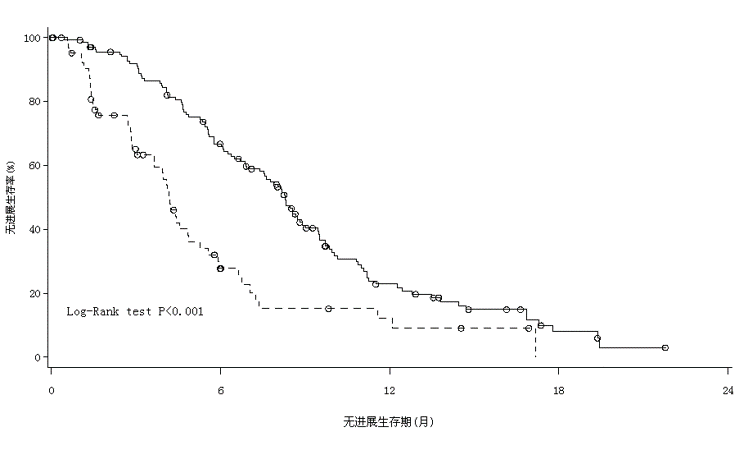
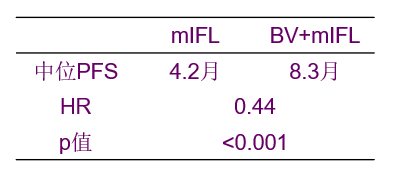 次要研究终点:总生存期
次要研究终点:总生存期
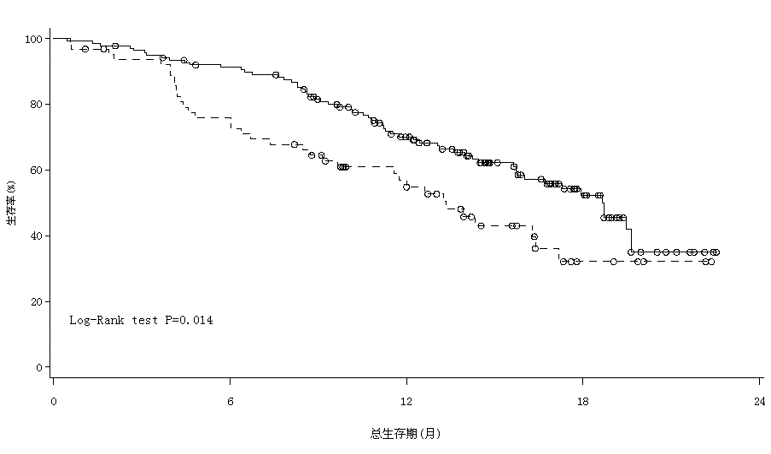
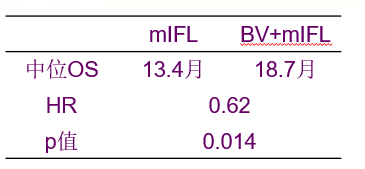
次要研究终点:客观缓解率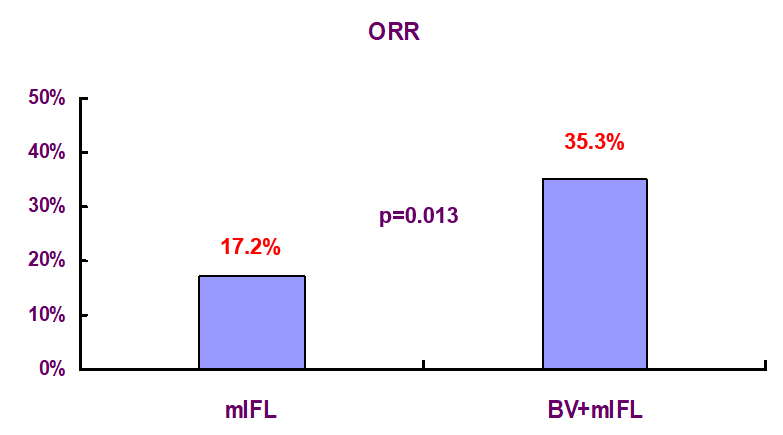
ARTIST疗效总结: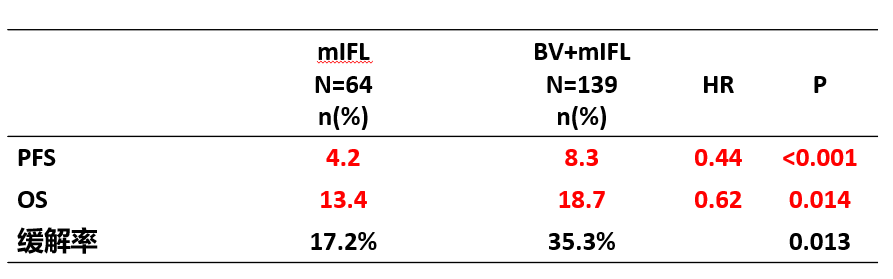 NCCN指南:
NCCN指南: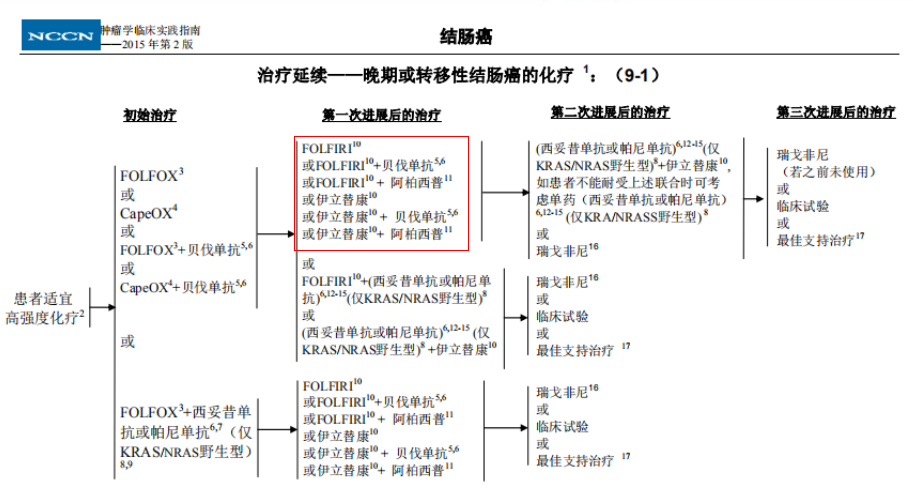
二线治疗:
2016.09.12始给予“贝伐珠单抗+FOLFIRI”化疗12周期,末次化疗时间为2017.03.09.
化疗4周期后疗效评估PR
2016.11.08 CT:

化疗8/12周期疗效评估维持PR:
2017.01.03 CT:
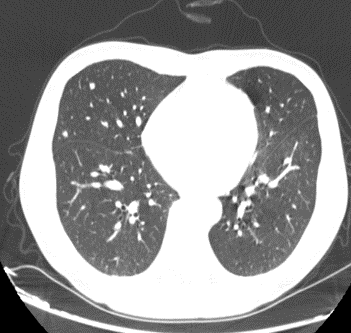
2017.03.08 CT:
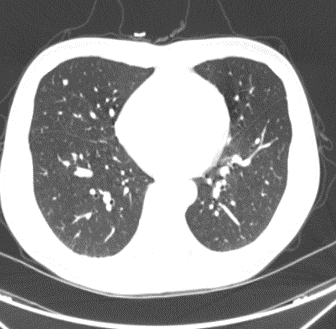
CAIRO3 和 AIO 0207: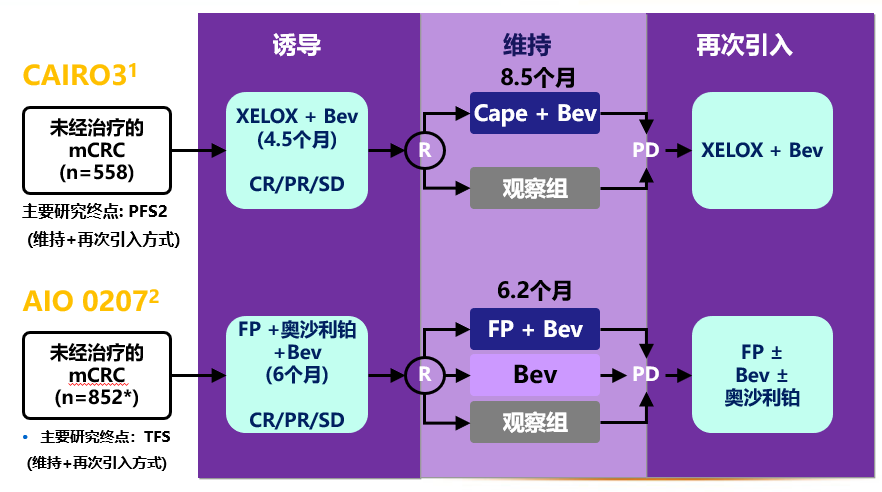 CAIRO3:研究设计
CAIRO3:研究设计
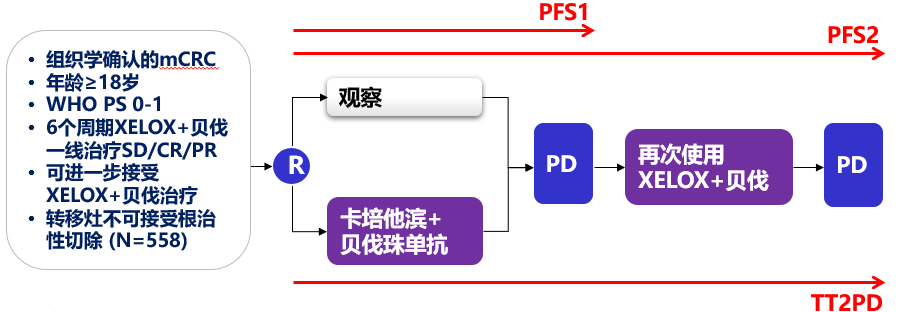
主要研究终点:
研究前诱导治疗:XELOX+贝伐 q3w x 6
–卡培他滨 1000 mg/m2 bid, op. d1-14 –奥沙利铂 130 mg/m2 iv, d1 –贝伐珠单抗 7.5 mg/kg iv, d1
维持治疗:
卡培他滨 625 mg/m2 bid, 连续
贝伐珠单抗 7.5 mg/kg iv, d1, q3w
CAIRO3:PFS1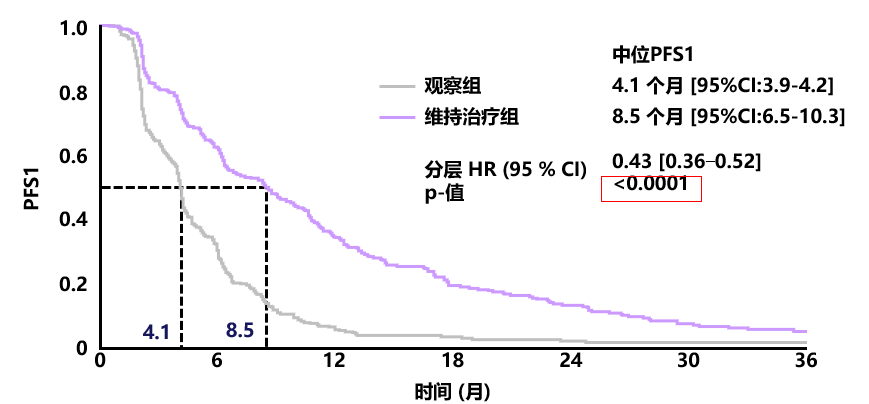 CAIRO3主要终点:PFS2
CAIRO3主要终点:PFS2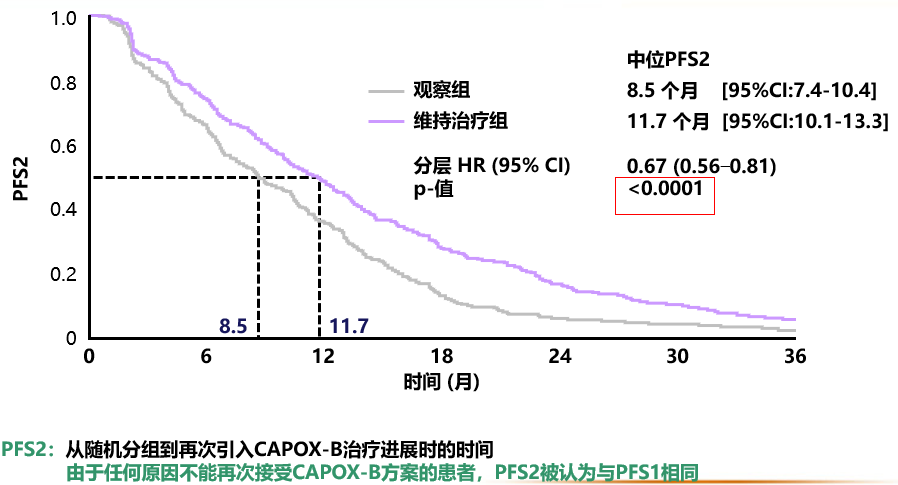
CAIRO3:TT2PD
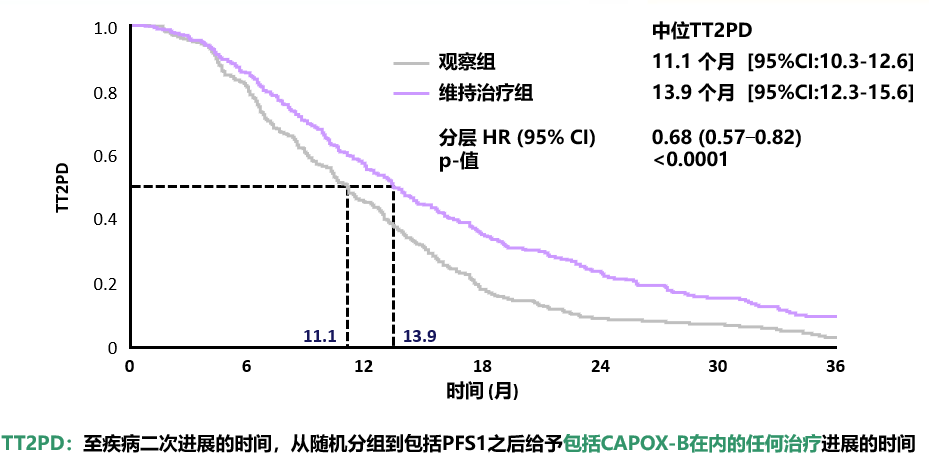 CAIRO3:OS
CAIRO3:OS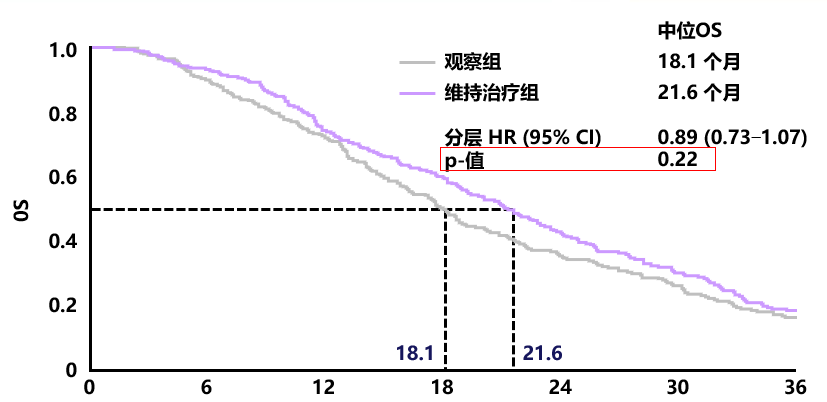 AIO 0207 研究设计:
AIO 0207 研究设计: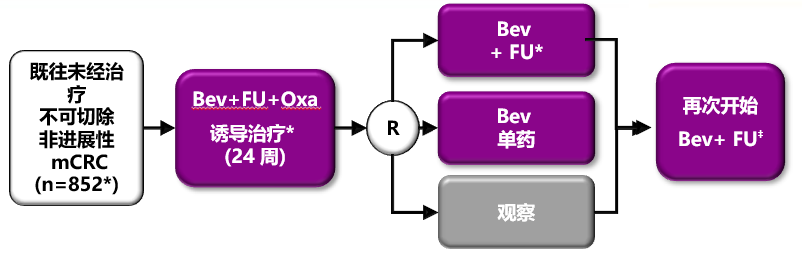
主要终点:至治疗失败时间(TFS)
定义:自随机(开始维持治疗)至维持治疗和再次用回原方案后的二次进展时间
–(如无再次治疗的情况下)TFS为至第一次进展时间 –非劣效性定义为TFS的HR 95%CI上限不超过1.43自维持治疗开始后的PFS1
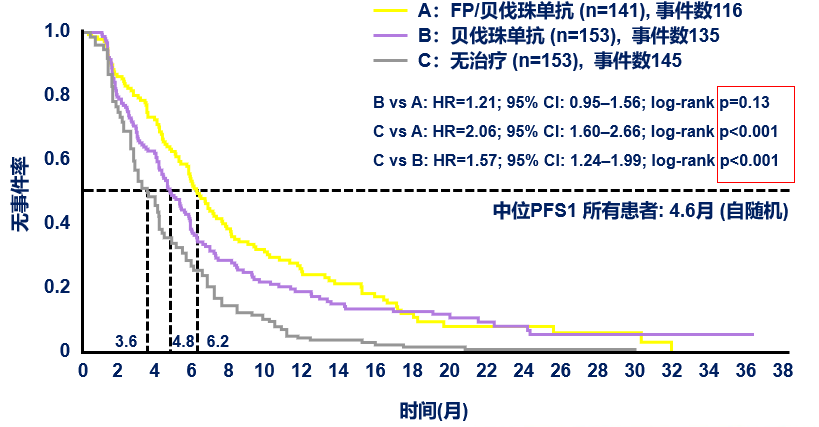 自维持治疗起的OS
自维持治疗起的OS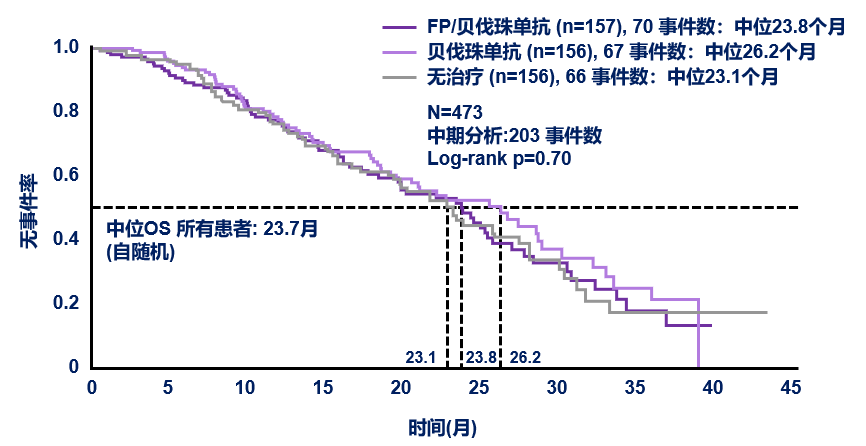
维持治疗:
2017.03.22始给予“贝伐珠单抗” 维持治疗5周期,末次给药时间2017.06.15。
2017.07.05胸腹部增强CT评估病情PD
2017.03.08 CT:
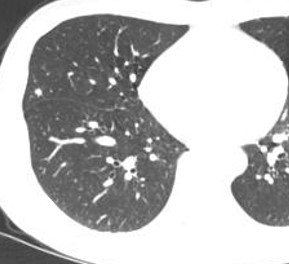
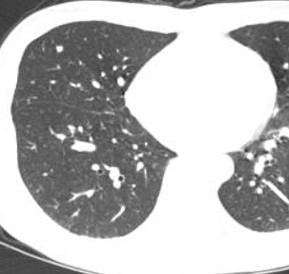
2017.07.05 CT:
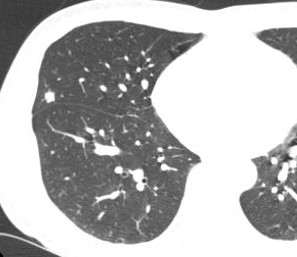
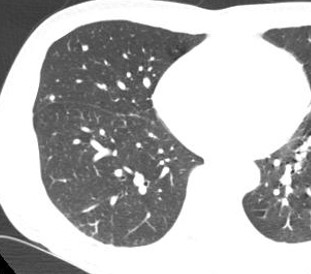
再次引入5-FU类药物:
2017.07.06始给予“贝伐珠单抗+替吉奥胶囊”化疗15周期,末次化疗时间为2018.4.26。
2018.05.16胸腹部增强CT评估病情PD: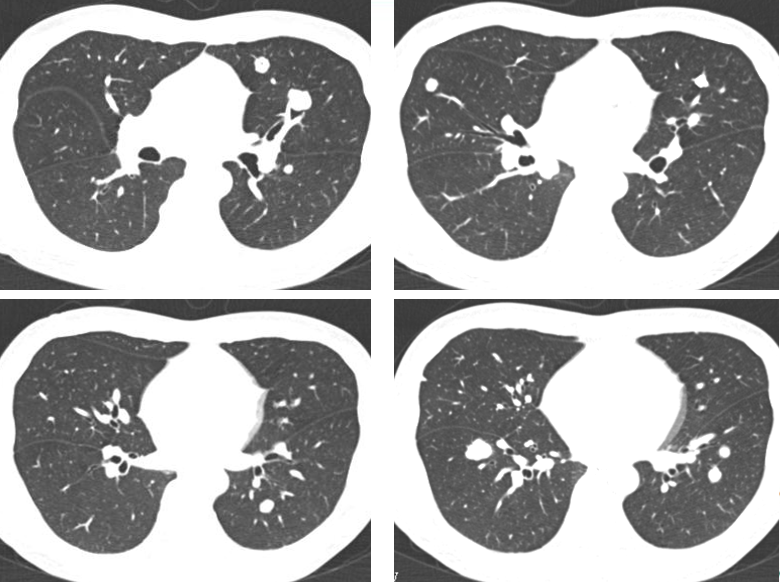 贝伐珠单抗跨线治疗III期临床研究:TML(ML18147)
贝伐珠单抗跨线治疗III期临床研究:TML(ML18147)
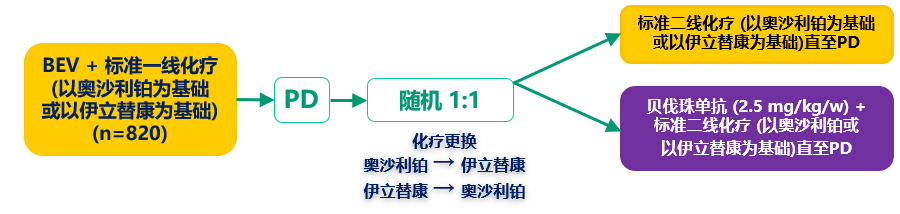
主要终点 | 自随机起的总生存 (OS) |
次要终点 | 无进展生存期 (PFS) 最佳ORR 安全性 |
分层因素 | 一线化疗 (以奥沙利铂为基础,以伊立替康为基础) 一线PFS (≤9个月, >9个月) 自末次贝伐珠单抗给药时间 (≤42天, >42天) 自基线的ECOG PS (0/1, 2) |
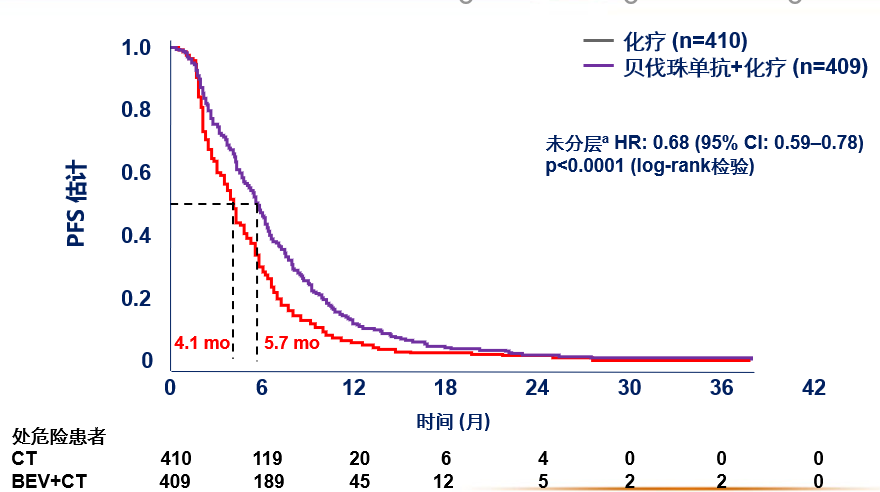
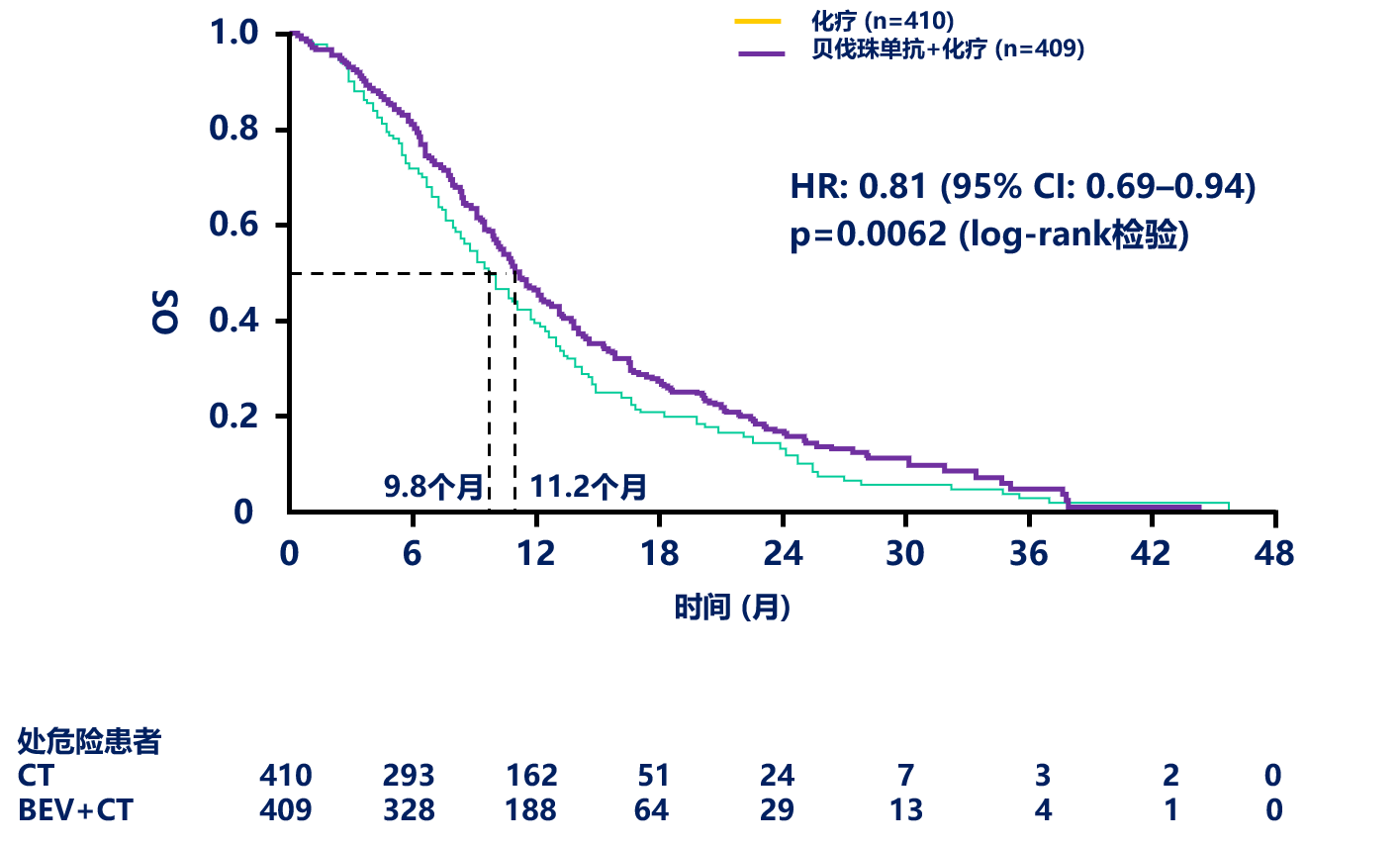
TML:贝伐珠单抗联合标准化疗方案一线治疗进展后,二线更换化疗方案,继续贝伐珠单抗治疗,显著延长总生存。
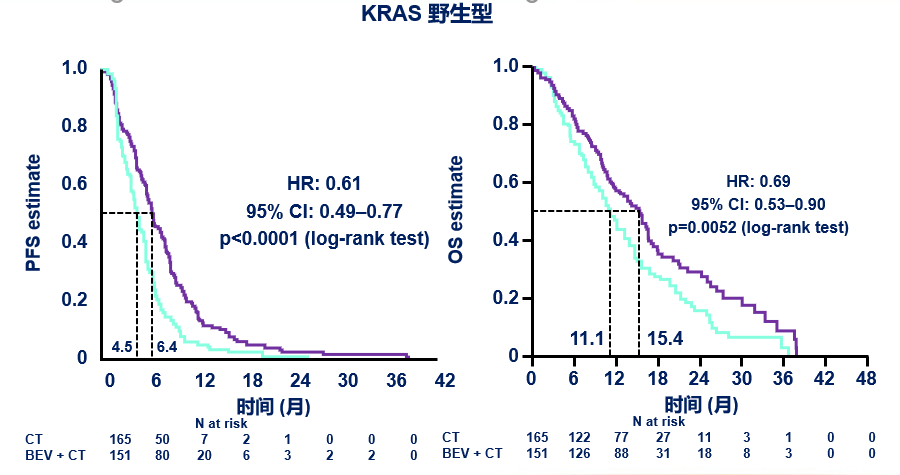
 TML研究中KRAS野生型亚组:PFS & OS获益显著
TML研究中KRAS野生型亚组:PFS & OS获益显著
 时机选择:贝伐珠单抗治疗快速进展患者
时机选择:贝伐珠单抗治疗快速进展患者

ML18147研究排除了快速进展患者(PFS<3个月),研究结论后续使用贝伐珠单抗跨线治疗有明显生存获益,较单用化疗延长OS 1.4个月(HR 0.81,95% CI 0.69-0.94;P=0.062)
对贝伐珠单抗快速进展患者,后续治疗不建议使用贝伐珠单抗继续跨线。
2019CSCO结直肠癌诊疗指南: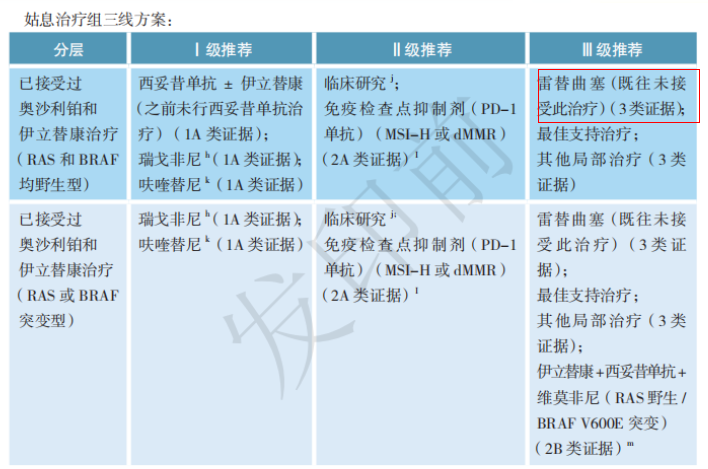
三线治疗:
2018.05.16始给予“贝伐珠单抗+奥沙利铂+雷替曲塞”化疗6周期,末次化疗时间为2018.09.13. 2018.10.11始“贝伐珠单抗+雷替曲塞”维持治疗4个周期,末次化疗时间为2018.12.13。
2019.01.23胸腹部增强CT评估病情PD: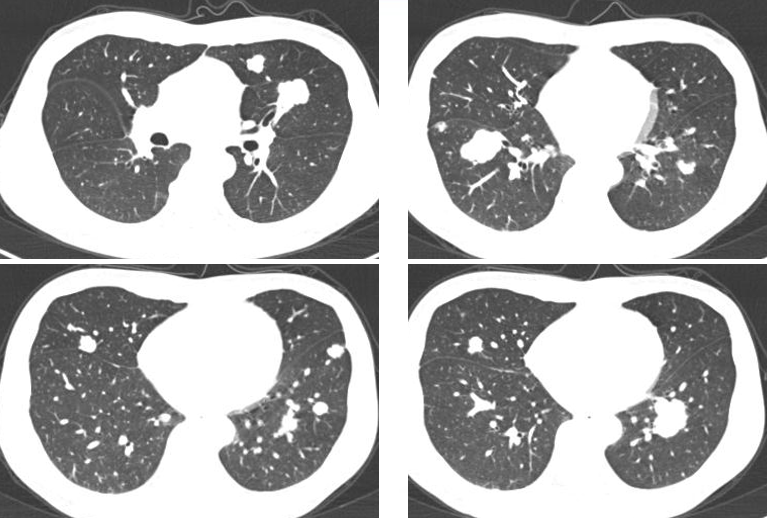
NCCN指南:
既往贝伐珠抗血管治疗后多项研究证实继续瑞戈非尼治疗生存获益显著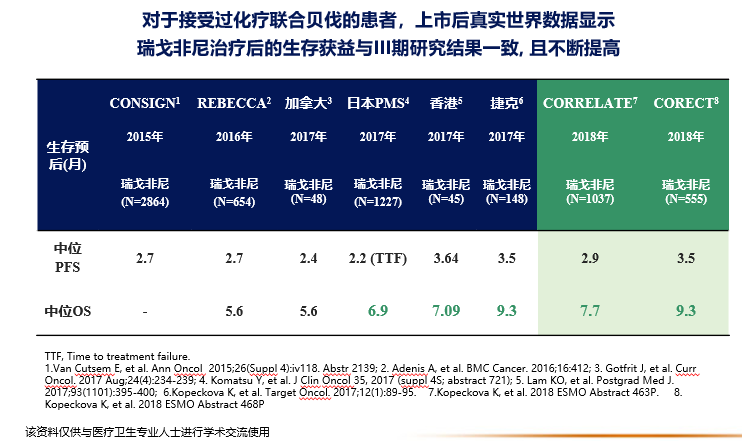
四线治疗:
2019.01.23始给予“瑞戈非尼 80mg起始,连服3周,停药1周”化疗6周期。
不良反应:手足综合征、口腔黏膜炎、阴囊水肿/溃疡。
2019.07.03胸腹部增强CT评估病情PD: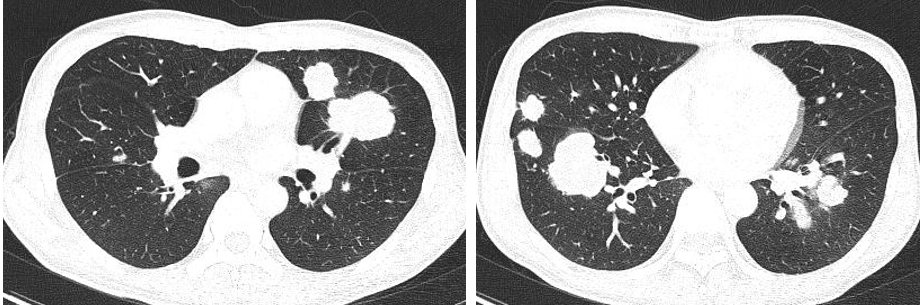
2019.07.04始给予“安罗替尼12mg,连服2周,停药1周”4周期。
2019.10.11胸腹部增强CT评估病情PD: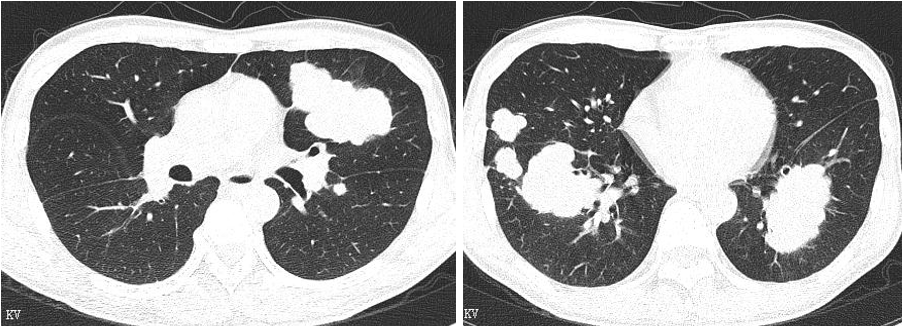
2019.10.15肺穿刺: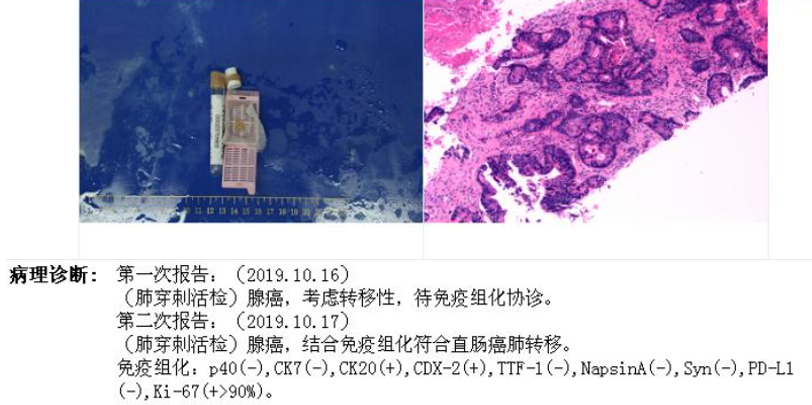 再次NGS检测:
再次NGS检测: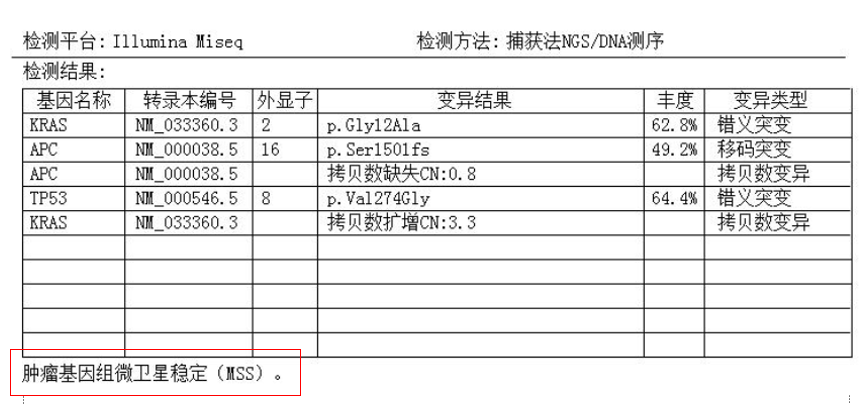
REGONIVO 研究2019ASCO结直肠癌新突破: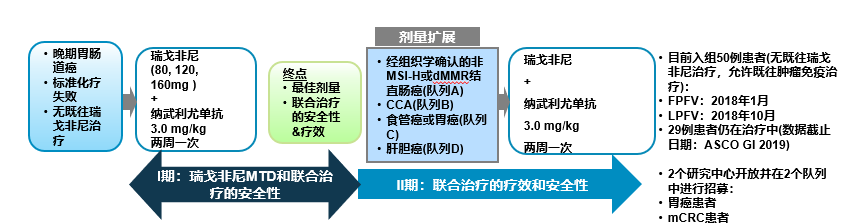
I期&II期剂量总结:
3+3设计和剂量递增直到160mg
160mg组全部3例患者因AEs而中断治疗
瑞戈非尼 MTD=120mg
患者#15-32接受初始120mg剂量治疗,但全部患者(除了1例患者)减量至80mg (患者#18在接受瑞戈非尼120mg+纳武利尤单抗联合治疗6个周期后仍在治疗中)
由于皮肤毒性(≠延迟发生且需要高剂量糖皮质激素治疗的HFSR),主要研究者决定在以下患者(#33-50)中使用瑞戈非尼80mg——参见安全性页
仅1例初始接受80mg治疗的患者(#38)现在接受瑞戈非尼40mg治疗(第3个周期正在进行中,C2观察到肿瘤缓解)
研究设计和目的(2019 ASCO现场公布)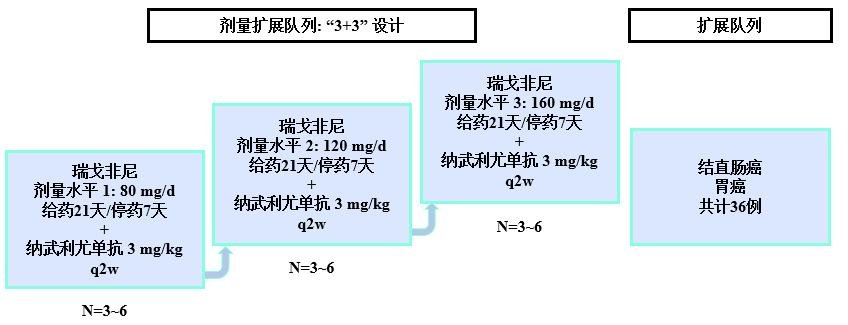 主要目的:周期1的剂量限制性毒性(DLT)以研究最大耐受剂量(MTD)和推荐剂量(RD)
主要目的:周期1的剂量限制性毒性(DLT)以研究最大耐受剂量(MTD)和推荐剂量(RD)
次要目的:ORR、PFS、OS、DCR
最佳肿瘤缩小的瀑布图 (2019 ASCO现场公布)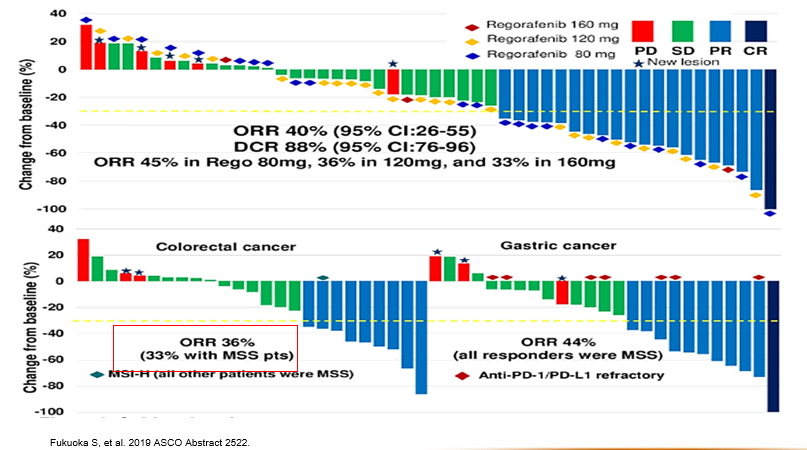 其他疗效数据 (2019 ASCO现场公布)
其他疗效数据 (2019 ASCO现场公布)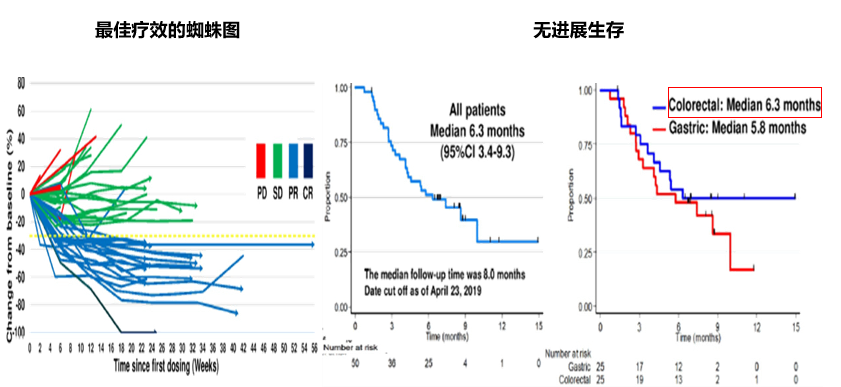 2019.11.1始给予“卡瑞利珠单抗200mg ivgtt+瑞戈非尼80mg 连服2周,停药1周” 化疗2周期,末次化疗时间2019.11.21。
2019.11.1始给予“卡瑞利珠单抗200mg ivgtt+瑞戈非尼80mg 连服2周,停药1周” 化疗2周期,末次化疗时间2019.11.21。
病史回顾:
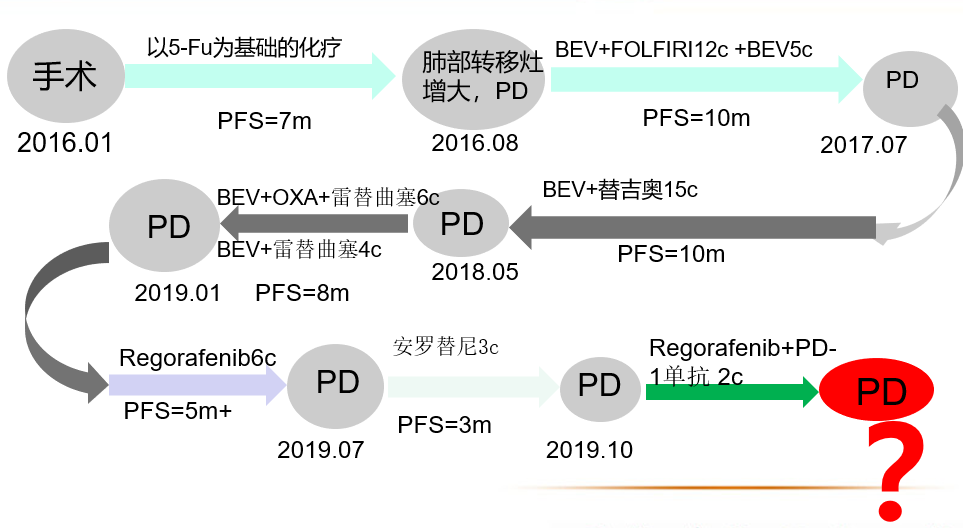 病例总结:
病例总结:
1.贝伐珠单抗跨线治疗的重要性
2.瑞戈非尼的应用?
3.PD-1在MSS人群中的应用时机?
查看更多