查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





2026年1月1日,新年的钟声余音尚在,中国科学院杭州医学研究所(以下简称“杭州医学所”)迎来里程碑时刻:谭蔚泓院士与吴芩研究员团队合作,在国际知名学术期刊Science发表重磅研究成果。研究团队成功构建了全球首个能够在单细胞分辨率下,同步实现细胞膜表面标志物发现与靶向核酸适体探针获取的一体化平台——SPARK-seq。该技术为分子识别、原创靶点发现及精准医学研究提供了全新的强大工具,有望为众多因靶点不明而缺乏有效疗法的疾病(如三阴性乳腺癌)开辟全新的治疗途径。
细胞表面蛋白是细胞的“门户”和“通信接口”,承载了约60%的药物靶点。然而,在浩如烟海的膜蛋白质组中锁定真正的癌症标志物,就像在黑夜中试钥匙。传统方法往往要先筛出上万个候选分子,再耗时数月甚至数年去验证它们“到底抓住了谁”。并且许多关键靶点表达量极低,且一旦离开活细胞就会“变样”,导致研发效率低、误差大,大量临床价值极高的靶点长期处于“隐身”状态。

针对这一制约精准医疗的瓶颈,医学所团队提出了一个精妙的构思:如果在同一个细胞里,既能“拿掉”靶点,又能实时读取分子的反应呢?
SPARK-seq 应运而生。它在单细胞水平上,巧妙地将三类顶尖技术融合:(1)CRISPR基因编辑: 像一把“分子剪刀”,精准剪掉特定的膜蛋白;(2)核酸适体组学: 投放海量“分子猎手”(适体)寻找目标;(3)单细胞多组学: 在同一个细胞里同步读取“谁被剪掉了”、“细胞变了吗”、“谁结合上去了”。
这种“三位一体”的逻辑,让靶点的确认从“推测”变成了“直观可见”的数字信号。
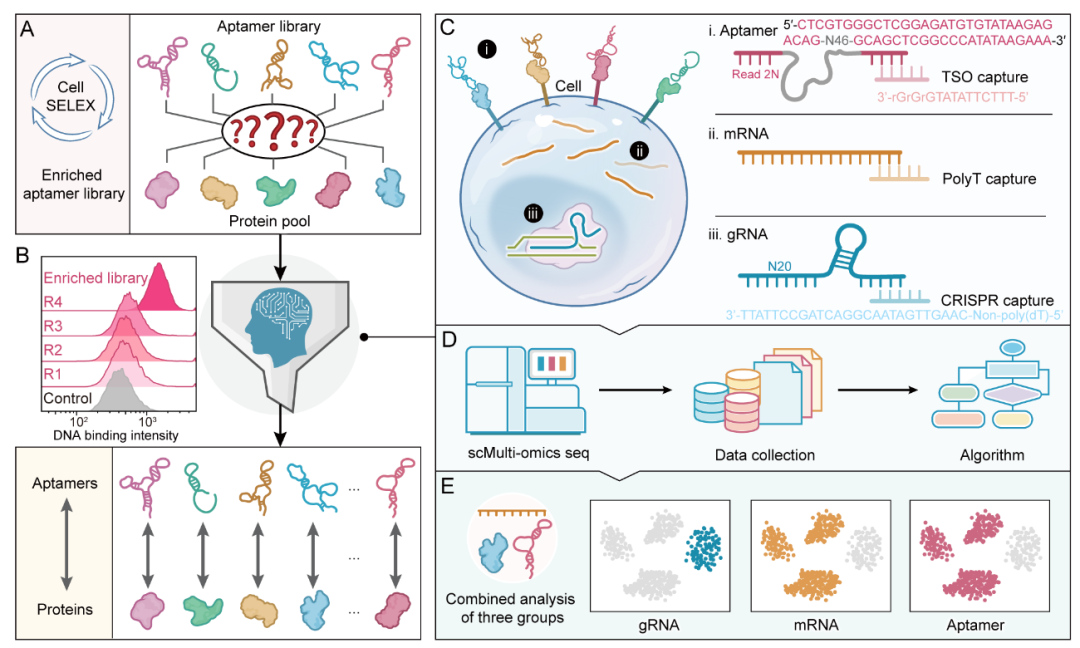
SPARK-seq原理与设计
利用SPARK-seq,研究团队在单次实验中深度分析了8000多个单细胞,从5000多条序列中精准锁定了8种肿瘤关键膜蛋白的特异性探针。该技术实现了即使是表面丰度相差上百倍的极低丰度靶点,也能被同时识别。并且首次实现了在天然细胞环境中,通过基因扰动直接建立适体与靶点的“因果关系”,有效克服了传统实验中因膜蛋白构象失真导致靶标鉴定难的问题。
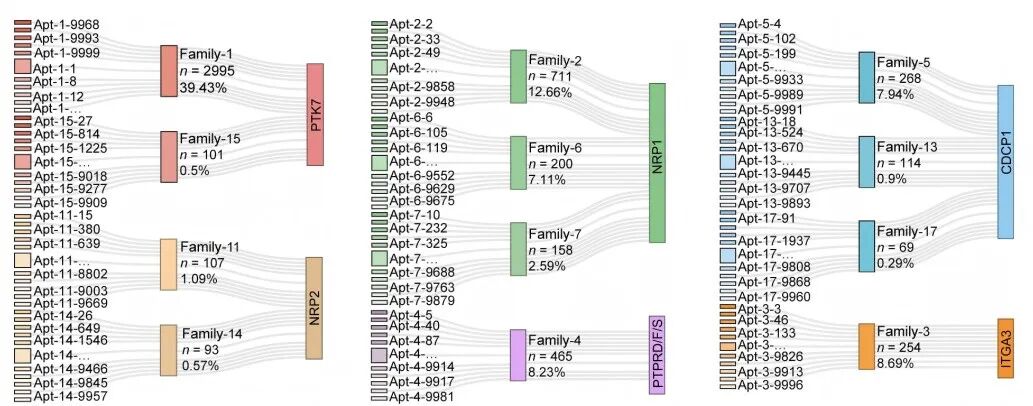
SPARK-seq带来的另一个惊喜是:它能自动筛选出“解离慢”的靶向核酸适体探针。 这种慢解离的稳定性在未来临床应用上至关重要——它意味着获取的靶向适体探针能使肿瘤成像信号更强、药物递送更精准、剂量需求更低。此外,通过自主研发的 SPARTA 深度学习框架,团队实现了高达 97% 的核酸识别探针预测准确率,让分子探针从“人工筛选”跨越到“理性设计”。
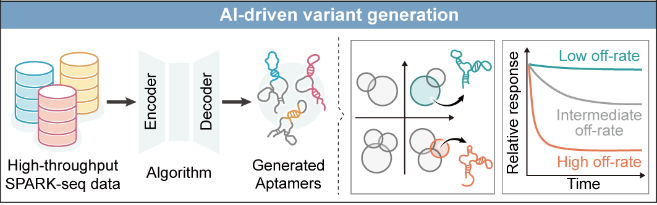
这项研究不仅实现了底层技术的颠覆性突破,更是对化学生物学与分子医学领域长期未解核心问题的系统性回应。它标志着细胞膜表面分子发现从“随机筛选”走向了“逻辑驱动”,为精准医学提供了深度的底层支撑。
在发现维度上,SPARK-seq 首次实现了对常规质谱难以触达的低丰度膜蛋白的系统性覆盖,使大量处于“盲区”的肿瘤微量标志物进入视野;
在识别精度上,SPARK-seq 彻底解决了构象敏感靶点在体外回溯中的失真难题,确保探针在原生细胞环境中通过“实战检验”,极大提升了分子药物在复杂生理环境下的转化成功率;
在性能评价上,团队前瞻性地确立了以“解离速率”为核心的新标杆,让探针开发从单纯的“识别”进化为对“有效作用时间”的精准控制;
在研发范式上,SPARK-seq 将海量实验数据沉淀为数字化训练集,构建了“发现-验证-优化”的 AI 驱动闭环,使分子设计正式迈入“数字化、可设计”的理性时代。
总结而言,SPARK-seq 不仅是一款高效工具,更是一套完整的“分子导航系统”,它让分子医学的每一个决策都建立在真实、高通量且可计算的生物数据之上,为细胞表面标志物的精准挖掘开创了新的范式。

通讯作者 谭蔚泓院士:
“这篇Science是医学所2026年的‘开门红’,更是我们核酸适体组学与分子医学的重要突破。科研的魅力在于从无到有的突破,也在于长时间的积淀。我们始终坚持做‘有用的研究’,更执着于‘原始的创新’。希望这第一个突破能激励所里更多的年轻人,仰望星空,脚踏实地,在医学科学与临床实践这片沃土上种出更多改变未来的医学科学之果。”
通讯作者 吴芩研究员:
“SPARK-seq 的诞生,是团队跨学科协作、集体攻关的胜利。我们不仅是在研发一个工具,更是在尝试构建一种可数字化的标志物挖掘新范式。回想2022年,这个想法刚诞生时我也曾有过忐忑,但在与学生们并肩作战、共克难关的日日夜夜里,这份不确定逐渐转化为前行的动力。衷心感谢每一位合作伙伴的倾力配合,科学的道路永无止境,我们将继续在‘探寻生命标志物’的征途中砥砺前行。”
第一作者 罗国焰、宋佳:“SPARK-seq 项目的顺利完成,离不开团队每个成员的努力与支持。过去四年的探索之路,走得并不容易。很多时候,实验进展缓慢,数据分析面临困难,但正是这些曲折让我更加坚信:只有团队的默契合作和彼此信任,才能让我们的科研工作不断突破和前行。此刻,能将这项成果作为新年礼物献给医学所,是对我们所有努力与坚持的最好回应。医学所世界一流的实验平台和自由创新的土壤,赋予了我们挑战未知的勇气与底气。未来,我们仍将步履不停,向着科学深处的光亮,继续前行。”
供稿 | 浙江省肿瘤医院
查看更多