查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





通讯作者:解放军总医院 韩为东 同济大学附属同济医院 梁爱斌 浙江大学医学院附属第二医院 钱文斌
CAR-T细胞治疗这一革命性创新疗法从实验室走到临床应用阶段,浙大二院血液科已经完成了3例难治/复发淋巴瘤患者,取得了良好的疗效。与传统化疗等方法不一样的是CAR-T细胞是“活的”药物,并具有细胞因子风暴和神经毒性等特殊的副作用,如何进行并做好细胞治疗的全程管理是安全、有效CAR-T疗法的关键。

最新一期《细胞&分子免疫》(Cellular & Molecular Immunology)杂志(IF:11.530)发表了中国专家的重磅述评:如何优化中国CAR-T治疗的全流程管理?
CAR-T细胞治疗为血液肿瘤,尤其是B细胞淋巴瘤治疗带来了革命性的改变。复发/难治的B细胞淋巴瘤患者常规化疗疗效差,中位生存期不足1年,目前应用CAR-T细胞治疗B细胞淋巴瘤,患者完全缓解率可以达到50%以上,这部分患者有望获得长期生存。
截至2021年4月16日,全球共有2073种在研活细胞治疗药物,比2020年同期增加了572种,增长率为38%。其中CAR-T疗法达到1164种,占据主导地位,对比去年同期增加299种,增幅达到35%。截至2019年底,已有593项注册的CAR-T细胞临床研究,其中48%的试验来自中国。
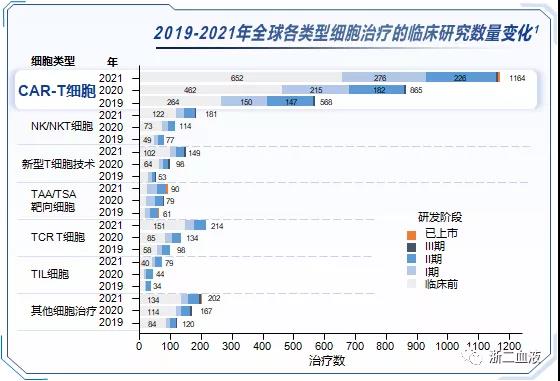

为了优化CAR-T治疗的全过程管理,建议:
(1)确保CAR-T产品的安全性和有效性,产品制备的透明化和标准化,设定CAR-T产品的标准;
(2) 自动化、标准化和规模生产以降低成本,最终实现个性化治疗的亲民价格;(3) 鉴于CAR-T前期的临床试验仅在部分医学中心进行,后续广泛应用于各个临床机构具有挑战性,迫切需要建立统一的CAR-T治疗指南;
(4)安全有效并系统性的收集临床数据,资源共享,并加强监管机构、CAR-T公司、医疗机构和患者之间的沟通。
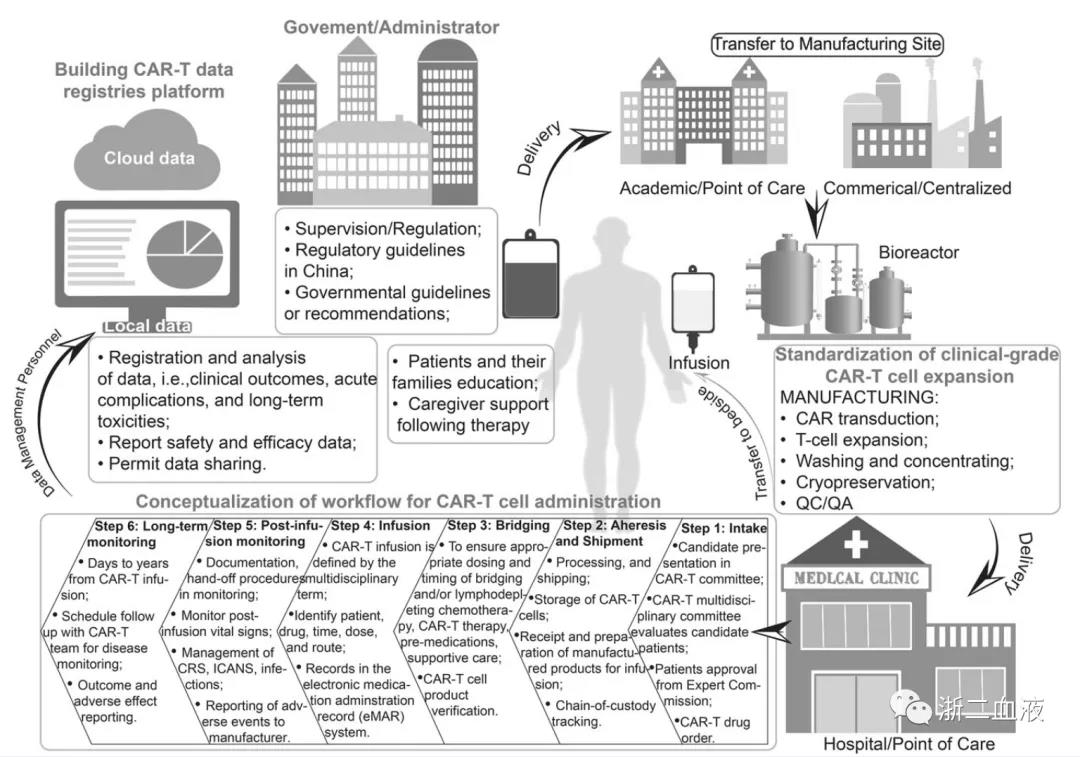
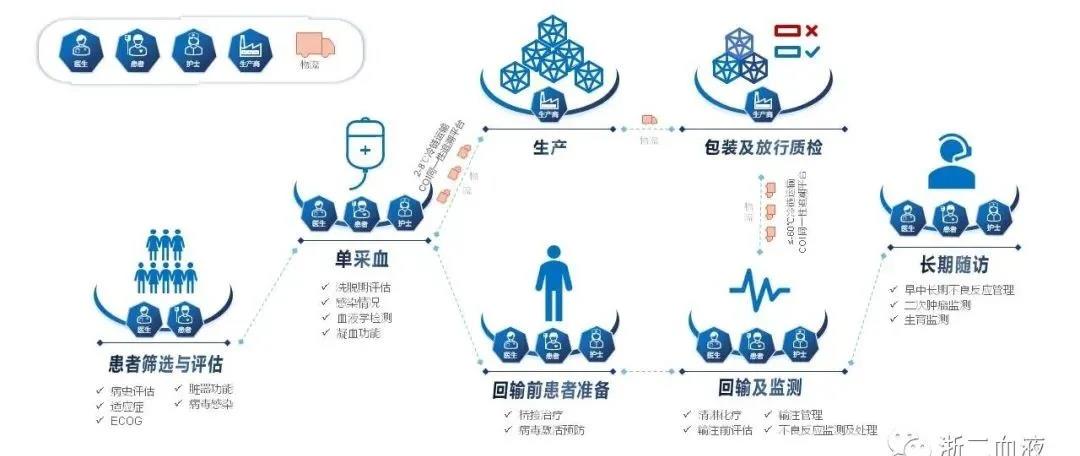
作为一种"活"的药品,CAR-T细胞治疗体系非常特殊,除了个体化定制之外,还涉及多个环节,环环相扣。
多环节相连
& 患者筛选及基线评估
& 单采前评估指标推荐
& 桥接治疗的选择
& 淋巴细胞清除化疗
& CAR-T细胞输注(输注前评估,输注管理)
& CAR-T细胞输注后不良反应管理
& 后续中长期随访
同时,CAR-T细胞治疗仍有其局限性:
一是治疗B细胞淋巴瘤患者的完全缓解率仍有待进一步提升,且部分患者完全缓解后出现疾病复发的现象亟待解决;
二是CAR-T细胞治疗相关副作用,如10%~30%患者治疗后会出现较严重的细胞因子风暴及神经系统毒性等,这也迫切需要更优化的CAR-T细胞结构和更规范的治疗管理加以改善。
CAR-T高危病例认定
& ECOG≥3
& 高肿瘤负荷:病灶最大直径乘积之和(SPD)≥100 cm2
& 巨块型病灶:单个病灶直径≥10 cm
& 病灶位于咽部、气管旁且存在压迫症状
& 病灶临近胃肠、胆管等重要空腔脏器,如病灶增大可压迫或侵犯周边脏器并影响其功能
& 浆膜腔受累存在浆膜腔积液(如胸腔积液、腹腔积液)
& Ki67≥90%
& 乙型肝炎病毒HBsAg+、HBV DNA<103或处于乙型肝炎病毒活动期,且无抗病毒治疗
& 重要脏器(如肺、胰腺、肾脏、肾上腺等)受累
患者回输后建议检测指标

早期发现CAR-T细胞相关副作用,早期处理、积极治疗,可使患者有良好的临床转归。《CAR-T 细胞治疗NHL毒副作用临床管理专家共识》的发布也为提高CAR-T细胞治疗的安全性提供了指导。
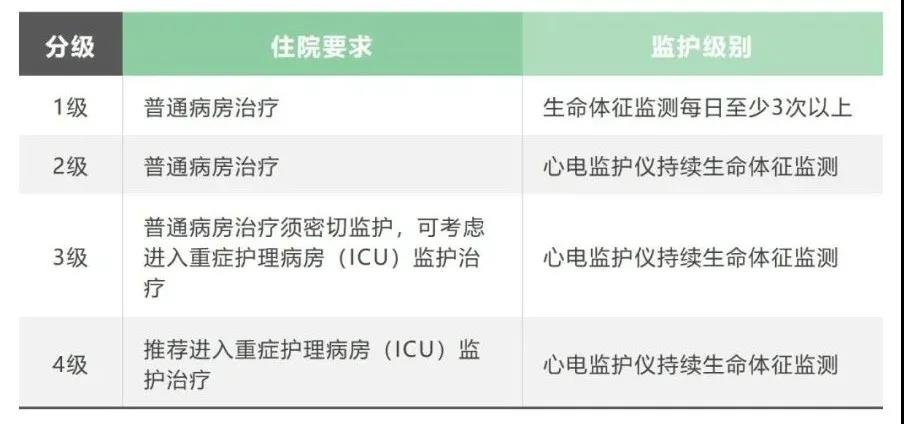
不良事件按4级区分及对应住院及监护要求
由免疫治疗引起的内源性或输注的T细胞以及体内其他免疫细胞激活所产生的一种超生理反应。CAR T细胞治疗相关CRS在淋巴瘤病例中发生率为30-95%,严重CRS(≥G3)发生率为10%~30%。与ALL不同,淋巴瘤中CAR T治疗相关CRS在发生机制、临床表现上具有特殊性。
CRS的分期与分型
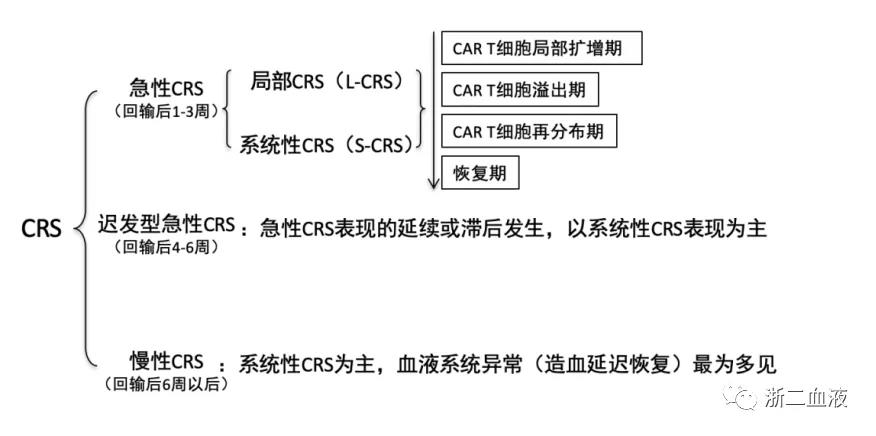
淋巴瘤CAR-T细胞治疗相关CRS分级标准

急性CRS的常规临床处置策略

1. 托珠单抗单次治疗最大剂量为800 mg;
2.治疗措施实施后观察24小时CRS症状无改善或加重,应升级至下一级处置;
3. 高危病例治疗后观察12小时CRS症状无改善或加重,应升级至下一级处置;
4. 高危病例如无β受体阻滞剂治疗禁忌,推荐CART细胞回输后即给予β受体阻滞剂(酒石酸美托洛尔片12.5-25mg 口服 2次/日).
指CAR T细胞治疗后出现的神经系统功能失调及相关病理性变化。免疫效应细胞相关神经毒性综合征(ICANS)是指免疫治疗后或继发于输注T细胞或内源性免疫效应细胞激活或应答所导致的中枢神经系统的病理过程和功能失调。
相对于CRES,ICANS的定义更为广泛,还包括其他免疫治疗继发的神经系统异常。
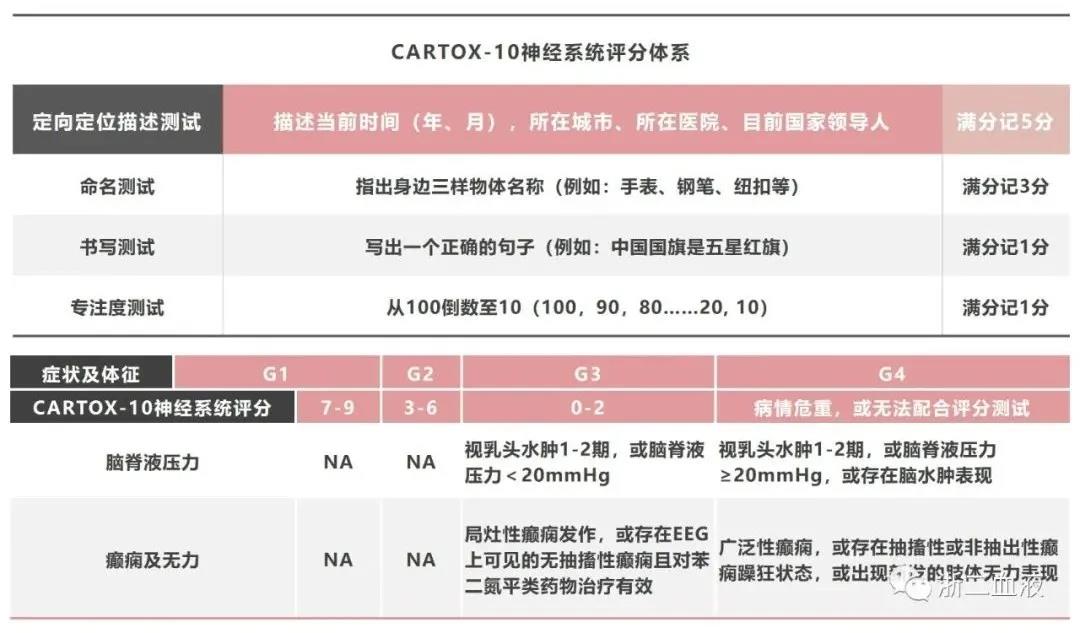
CRES的发病机制尚不明确,高细胞因子水平、高肿瘤负荷、血脑屏障功能异常、CAR T的结构以及颅内血管组织表达CD19等因素可能与CRES发生有关。
淋巴瘤患者中CRES发生率为20-60%,主要发生于CAR T回输后的8周内,中位持续时间为4-6天。临床表现包括头痛、谵妄、认知障碍、肌震颤、共济失调、语言障碍、神经麻痹、感觉障碍、嗜睡、癫痫发作等。继发脑水肿是神经毒性致死的重要原因。

HLH/MAS是一种涵盖了多种严重免疫功能异常的症候群,特征性表现为巨噬细胞和淋巴细胞的活化,炎性细胞因子升高,淋巴细胞的组织浸润以及免疫介导的多器官功能衰竭。多见于CRS恢复期或伴发与CRS过程中。
与经典的系统性CRS比较,除了常见的发热,HLH/MAS存在相对特征性的临床表现:肝脾肿大,骨髓穿刺嗜血细胞、嗜血现象,外周血血象三系或两系减少,甘油三酯及血清铁蛋白异常增高,多种细胞因子异常增高,sCD25升高等。HLH/MAS可以导致患者长期处于白细胞减少,严重者有粒细胞缺乏,并发感染存在致死风险。
出现以下情况高度提示HLH-MAS:
外周血中CAR-T持续高水平存在,超过2周以上,甚至2周后再次升高;再度发热,伴有血象三系下降,肝脾肿大等;转铁蛋白持续升高。
CAR-T治疗长期随访临床指标

最后,CAR-T治疗的全程管理势必是多学科协作(MDT)的过程,涉及病理科、神经内科医生、影像科、重症医学、呼吸科、外科及护理团队等等的通力合作,确保患者安全和治疗疗效。
浙二血液 平台发布
查看更多