查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





近年来,新辅助和围术期免疫治疗是可手术非小细胞肺癌(NSCLC)领域的热点。其中,纳武利尤单抗作为率先在该领域开展探索、且目前唯一III期证据覆盖新辅助和围术期的免疫治疗药物,持续扮演着“奠基者”和“领航者”的角色。近期举行的2024年ESMO ASIA大会上,纳武利尤单抗方案用于NSCLC围术期治疗的III期CheckMate-77T研究中国亚组亮眼数据重磅公布[1],进一步填补了该模式用于中国患者的临床证据。借此契机,我们特邀上海交通大学医学院附属胸科医院储天晴教授围绕CheckMate-77T最新数据、纳武利尤单抗既往相关重要成果及其临床意义作简要点评,以飨读者。
数值亮眼,围术模式用于中国人群获益喜人
CheckMate-77T是一项探索纳武利尤单抗围术期方案(术前4周期纳武利尤单抗+化疗、术后1年纳武利尤单抗辅助治疗)用于可手术IIA-IIIB期NSCLC患者的III期研究,本次ESMO ASIA大会公布了该研究的中国亚组数据。
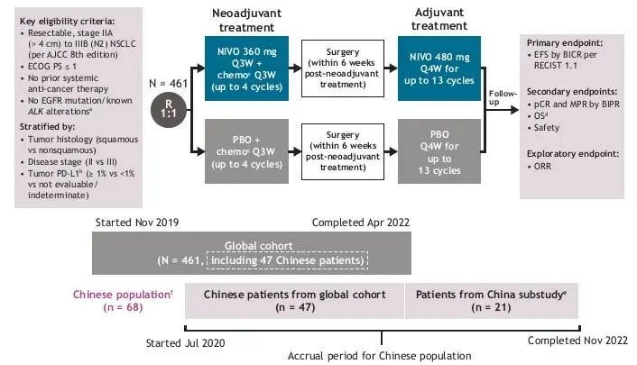
CheckMate-77T及中国亚组研究设计
主要终点方面,中国亚组的无事件生存期(EFS)的风险比(HR)低至0.40,纳武利尤单抗方案可降低60%疾病复发、进展或死亡风险,HR数值在全球人群[2](EFS HR 0.59)的高水准基础上仍观察到进一步下降,令人惊喜。次要终点方面,中国亚组的病理完全缓解(pCR)率相较对照组为35.1% vs. 3.2%,主要病理缓解(MPR)率为51.4% vs. 6.5%,数值上也均高于全球人群(pCR率:25.3% vs. 4.7%,MPR率:35.4% vs. 12.1%)。
本次还公布了中国亚组客观缓解率(ORR),相较化疗组为78.4% vs. 32.3%。手术结局方面,根治性手术率、临床降期率相较对照组分别为81.1% vs. 61.3%、54.1% vs. 19.4%。安全性方面,中国亚组的3~4级治疗相关不良事件(TRAEs)发生率相较化疗组为54.1% vs. 40.0%,未发现新的安全性信号,且大多数(84%)患者完成了新辅助免疫+规定的四个疗程,比例与全球人群近似(83%)。以上数据提示,术前4周期纳武利尤单抗+化疗相较单纯化疗可实现更佳的缩瘤、降期效果,且安全可行、不影响手术进行,进一步印证了此前CheckMate-816研究的相关结论。
人群基线特征方面,相较全球人群,中国入组患者的鳞癌占比较高,且更多患者的ECOG PS评分=1,同时PD-L1表达≥1%的患者比例也更高,与我国整体NSCLC患者特点一致,高度符合实践,为临床用药提供了坚实的参考依据。以上数据进一步支持了CheckMate-77T模式作为中国可手术NSCLC患者的优选方案之一。
首开先河,纳武利尤单抗奠定围术诊疗基石
CheckMate-77T的意义不仅在于证实了纳武利尤单抗围术期模式的价值,也继CheckMate-816研究开创了纳武利尤单抗+化疗新辅助治疗的模式后,于III期研究中“复现”了该模式在全球和中国人群中的获益,进一步明确了新辅助免疫+化疗在围术期的基石地位,在此也对CheckMate-816现有的长随访数据作简要回顾。
CheckMate-816全球人群3年数据[3]显示,纳武利尤单抗新辅助治疗患者EFS HR 0.68,3年EFS率相较化疗组提高14%(HR 0.68)。而中国亚组[4]EFS改善幅度在数值上更大,提升达24%,HR数值也更低(HR 0.47)。pCR方面,全球结果改善超过11倍,而中国亚组改善超12倍(25% vs. 1.9%)。安全性方面,不论全球还是中国数据,3级以上TRAE发生率均与安慰剂组相似。
今年ASCO大会公布了研究4年随访数据[5],进一步明确了纳武利尤单抗新辅助治疗的长期获益优势:4年EFS率为49%,4年OS率达71%(化疗组分别为38%、58%),且随时间推移能够持续保持EFS与OS曲线分离。此外,在达pCR的患者中,4年OS率高达95%。
综上,凭借CheckMate-816与CheckMate-77T两大III期研究的EFS、pCR等数据,纳武利尤单抗确立了自身在NSCLC围术期治疗领域的关键性地位,其长期随访获益也为后续的临床设定了新的标准。鉴于仅新辅助治疗的CheckMate-816长期获益已十分优秀,我们也十分期待CheckMate-77T后续能揭示更卓越的长生存结果。不仅如此,两项研究的中国亚组分析与全球结果保持高度一致,且在部分关键指标上数值更为突出,这无疑为上述方案用于国内临床进一步夯实了证据。也期待该领域的热点问题(如:不同细分人群的精准治疗等)后续能有更多结果的出炉,为临床提供进一步的指导,帮助患者取得更好的疗效。
参考文献
[1]. Wu, L., et al. (2024). Perioperative nivolumab (NIVO) in patients (pts) with resectable stage II–IIIB NSCLC: CheckMate 77T Chinese population analysis. ESMO Aisa 2024, 277P.
[2]. Pulla, M. Provencio, et al. (2024). LBA50 Perioperative nivolumab (NIVO) v placebo (PBO) in patients (pts) with resectable NSCLC: Clinical update from the phase III CheckMate 77T study. Annals of Oncology, 35(Supplement_1), S1239-S1240.
[3]. Spicer, J., et al. (2023). Clinical outcomes with neoadjuvant nivolumab (N) + chemotherapy (C) vs C by definitive surgery in patients (pts) with resectable NSCLC: 3-y results from the phase 3 CheckMate 816 trial. Journal of Clinical Oncology, 41(16 Suppl), 8521-8521. doi:10.1200/JCO.2023.41.16_suppl.8521.
[4]. Wang, C., Chen, K. N., Chen, Q., Wu, L., Wang, Q., Li, X., Ying, K., Wang, W., Zhao, J., Liu, L., Fu, J., Zhang, C., Liu, J., Hu, Y., Ntambwe, I., Cai, J., Bushong, J., Tran, P., Lu, S. (2023). Neoadjuvant nivolumab plus chemotherapy versus chemotherapy for resectable NSCLC: subpopulation analysis of Chinese patients in CheckMate 816. ESMO Open, 8(6), 102040. doi:10.1016/j.esmoop.2023.102040. PMCID: PMC10774966.
[5]. Spicer, J., et al. (2024). Neoadjuvant nivolumab (NIVO) + chemotherapy (chemo) vs chemo in patients (pts) with resectable NSCLC: 4-year update from CheckMate 816. Journal of Clinical Oncology, 42(LBA8010-LBA8010).
转载自医学界肿瘤频道
查看更多