查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





(通讯员 陈勤奋)近日,复旦大学附属华山医院感染科张继明教授团队、布朗大学肝病研究中心Shuping Tong、Jisu Li教授团队和厦门大学夏宁邵、袁权教授团队鉴定出一株高感染性C基因型乙型肝炎病毒(HBV)临床分离株,并进一步研究高感染性机制,探索其临床意义。相关成果以“Naturally occurring 5′ preS1 deletions markedly enhance replication and infectivity of HBV genotype B and genotype C”为题在线发表于国际著名期刊《GUT》。

高效的HBV体外感染模型对于研究HBV与宿主的相互作用等至关重要。现有体外感染细胞模型主要有人原代肝细胞、分化的HepaRG细胞、外源性表达NTCP的肝癌细胞系等,被广泛应用于HBV感染实验,但不足之处是感染效率均较低。在病毒来源方面,用于体外感染的病毒主要来自于HepG2.2.15、HepAD38和HepDE19等稳定转染细胞系产生的D基因型HBV,而中国以B和C基因型毒株流行为主。目前尚缺乏可体外高效感染的B或C基因型模型毒株。
正文实验图摘录:

图1:5’端preS1区缺失或插入对HBV感染性的影响
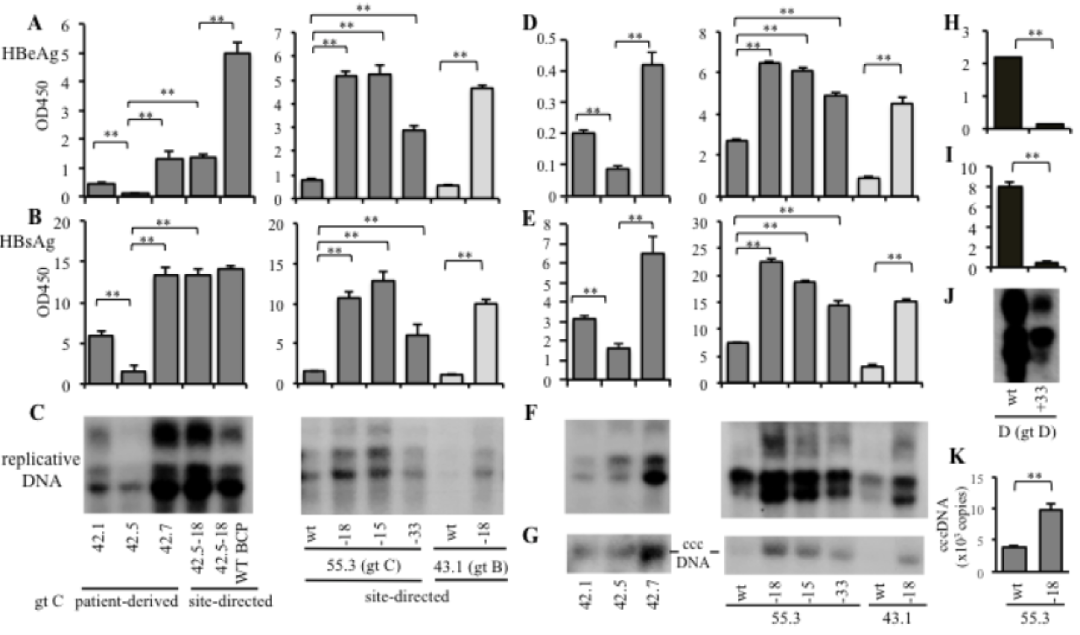
图2:野生型和N端截短型preS1多肽抑制HBV感染及与HepG2/NTCP细胞结合能力的比较
该研究从一例“免疫耐受期”的C基因型HBV慢性感染者血清中分离出5’端preS1区15 nt和18 nt缺失突变株,分析该患者2012年、2017年和2019年的系列血清标本后发现缺失株比例逐渐增加。用相同拷贝数病毒感染HepG2/NTCP和HepaRG两种细胞,发现缺失株感染性强于野生株;相反,另外两株自然发生5’端preS1区缺失的C基因型毒株(分离于慢乙肝肝癌患者)中重新插入该区18 nt片段、以及D基因型克隆该区插入33 nt片段后,感染性均明显下降。随后,研究者发现仅突变C基因型preS1区第一个起始密码子,使之翻译产生类似于D基因型、截短了11个氨基酸的L蛋白足以增强感染性。为验证截短型L蛋白与感染性增强有关,研究者合成野生型和缺失型两种豆蔻酰化修饰的preS1多肽,发现缺失型多肽体外抑制HBV感染及与HepG2/NTCP细胞结合能力更强。同时,缺失株感染后早期胞内cccDNA水平明显增强。以上结果提示缺失型病毒感染进入细胞的能力更强,其机制与截短型L蛋白结合细胞的能力更强有关。此外,研究者用HBV 1.1倍体转染HepG2细胞,发现18 nt缺失株转染后胞内HBV RNA、HBV DNA以及胞外病毒颗粒释放水平均明显强于野生株。
进一步追踪该患者长达九年的临床资料随访情况,发现其为持续高HBV DNA载量、高表面抗原以及正常丙氨酸转氨酶(ALT)水平,可判断为“免疫耐受期”,但随后肝组织学活检结果为中重度肝脏炎症及纤维化(G2S2),提示已经进入“免疫清除期”。研究者认为该患者长期高病毒载量状态与病毒突变导致的病毒感染性和复制能力增强有关,并不能代表真正的免疫耐受状态。同时,病毒与宿主在相互选择中不断进化,HBV方面可通过改变感染性等维持其慢性持续感染。该研究也提示可通过在5’端preS1区引入突变以提高体外感染性,构建B和C基因型HBV感染模型毒株,用于HBV与宿主的相互作用、cccDNA的形成和降解及抗HBV药物的筛选等相关研究。
布朗大学/复旦大学基础医学院童舒平教授、布朗大学李纪速教授和华山医院张继明教授为本文共同通讯作者。感染科博士研究生李菁为论文第一作者。
(审核 张文宏 编辑 李发红)
查看更多