查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





食管癌是我国五大恶性肿瘤之一,在全国新发恶性肿瘤中位居男性第三位,女性第五位,其致死率在所有恶性肿瘤致死率中位于第四位。
早期食管癌的手术切除率为100%,5年生存率可达90%以上。然而,我国近75%的食管癌患者在确诊时已发展为局部晚期或伴有远处转移;局部晚期的食管癌患者在手术治疗后也仍有近50%的患者会复发,而晚期患者的治疗手段有限,以化疗为主、中位生存期在一年左右。上述因素导致我国食管癌的总体五年生存率不到30%,食管癌治疗存在巨大未被满足的需求,治疗水准也迫切需要提升。
首个PD-1或将改变食管癌治疗临床实践
免疫治疗不可切除的局部晚期和转移性食管癌近两年发展迅猛,三个PD-1免疫检查点抑制剂单药治疗局部晚期或晚期食管癌的III期临床研究结果在2019年公布(图1)[1-3]。
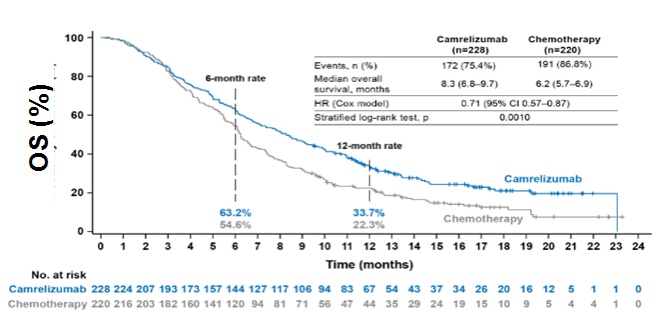
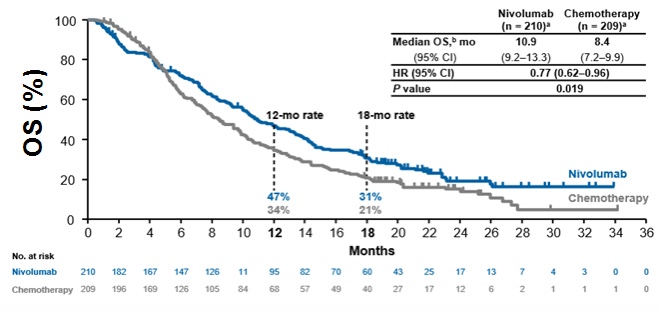
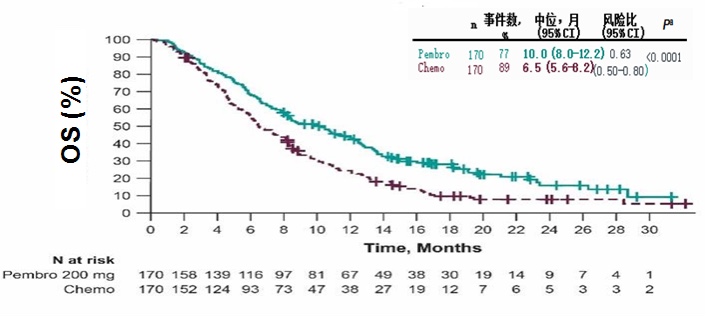 图一、卡瑞利珠单抗、纳武利尤单抗以及帕博利珠单抗单药治疗食管癌的三个III临床研究(ESCORT, ATTRACTION-3和KEYNOTE-181)的OS曲线图
图一、卡瑞利珠单抗、纳武利尤单抗以及帕博利珠单抗单药治疗食管癌的三个III临床研究(ESCORT, ATTRACTION-3和KEYNOTE-181)的OS曲线图
美国FDA基于KEYNOTE-181研究的OS阳性结果于2019年7月31日批准帕博利珠单抗治疗PD-L1阳性(CPS≥10)、经一线或多线全身治疗后进展的局部晚期或转移性食管鳞状细胞癌, 而日本厚生省也于2020年2月22日基于2019年ESMO公布的ATTRACTION-3研究结果批准纳武利尤单抗治疗在化疗后疾病依然进展无法切除的晚期/复发性食管癌患者。
KEYNOTE-181研究结果显示帕博利珠单抗治疗中国食管癌人群所带来的OS获益相比给欧美人群带来的获益更显著,死亡风险降低45%, 是整体研究人群的3倍: 中国人群45%(HR, 0.55[0.36-0.82],95%CI)相比整体人群仅有的15%(HR, 0.85[0.72-1.01],95%CI,P=0.031)[4]。 这一“偏向性”在食管鳞癌和PD-L1表达阳性(CPS≥10)人群都有体现(表1)。
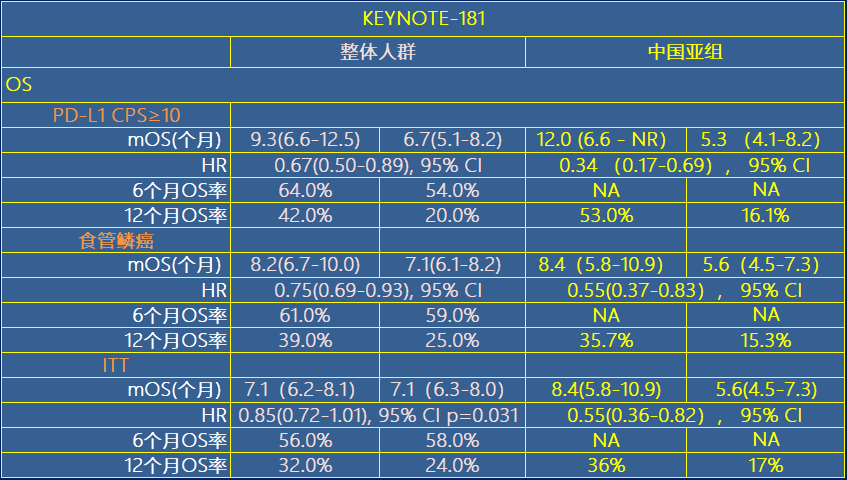 表一、KEYNOTE-181研究中帕博利珠单抗治疗整体人群和中国亚组人群的OS数据对比
表一、KEYNOTE-181研究中帕博利珠单抗治疗整体人群和中国亚组人群的OS数据对比
据悉,帕博利珠单抗治疗食管癌的适应证有望在近期正式获批。
“在过去几十年,晚期食管癌一线治疗只有5-FU和顺铂这两种化疗一线治疗药物,而且带来的中位OS不到一年,出现疾病进展后也缺乏标准治疗方案。在这样的背景下,免疫治疗的到来必将为晚期食管癌治疗带来革命性的改变,助力提升我国局部晚期和转移性食管癌患者的总生存率“, 复旦大学附属肿瘤医院放射治疗中心胸部专科主任赵快乐教授认为。
在晚期非小细胞肺癌取得巨大成功的免疫联合化疗方案也在晚期食管癌治疗中显示出巨大的潜力。据悉,当前有多个PD-1联合化疗的III期临床研究已在国内开展之中,其中帕博利珠单抗联合化疗一线治疗复发转移性食管癌患者(鳞癌、腺癌和胃食管结合部腺癌)的III期临床研究KEYNOTE-590的中国扩展研究已在国内20个中心启动,并于2019年6月完成所有受试者的入组[5]。
术后复发食管癌的免疫治疗
国家癌症中心2019年1月发布的最新一期的全国癌症统计数据[6]显示, 2015年食管癌发病人数约25万,这其中约有四分之三的患者在被初诊时已是局部晚期食管癌或发生远端转移。
对于可手术切除的局部晚期患者,同步放化疗配合手术治疗是局部晚期食管癌的标准治疗方案,但是术后仍有50%的复发率。免疫治疗作为放化疗后的维持治疗,在III期不可切除的非小细胞肺癌治疗领域已经显示能带来显著的疗效和长期生存获益[7],这令业界对于免疫治疗用于食管癌术后维持治疗充满期待。
据赵快乐教授介绍,当前有多个食管癌术后放化疗联合免疫的临床研究正在国内开展之中,但是放化疗联合免疫治疗,或序贯免疫维持治疗必须考虑不良反应的管理。食管癌患者因为进食有困难,所以一般身体状况都较差,PS评分比较高,对于放化疗的耐受程度较弱;而且放化疗本身有一定的副作用,比如放疗可能导致的放射性肺炎等。
顺铂和氟尿嘧啶化疗方案联合根治性放疗是不可切除的局部晚期食管癌的标准治疗方案。然而,这一根治性方案的治疗毒性较大:42%的患者出现3级急性毒性、25%的患者出现3级远期毒性,而5年生存率仅26%[8]。
2019年3月28日,《临床肿瘤学杂志》(Journal of Clinical Oncology)在线发表了由复旦大学附属肿瘤医院赵快乐教授领衔的一项多中心、随机对照、Ⅲ期临床研究(ESO-Shanghai 1),结果显示紫杉醇联合氟尿嘧啶的同步放化疗治疗局部晚期食管鳞癌,五年的OS率达到43%,但相比顺铂+氟尿嘧啶联合根治性放疗方案,虽然急性3级或以上的贫血、血小板减少、厌食、恶心、呕吐和乏力发生率显著更低,但白细胞减少、放射性皮炎、肺炎的发生率却更高[9]。
“因此,免疫联合放化疗,无论是同步还是序贯维持,必须关注严重不良反应的发生,跟踪和管理患者,以早期发现苗头并给予及时的处理”, 赵快乐教授提醒,“稍有疏忽,就会有严重的后果。”
不同PD-1显示不同不良反应谱
在KEYNOTE-181研究中,帕博利珠单抗(K药)治疗中国食管癌患者的相关的不良反应发生率低于化疗(帕博利珠单抗组75.8%, 化疗组83.1%), 3-5级不良反应的发生率更是仅有化疗组的一半(帕博利珠单抗组21.0%, 化疗组42.4%)(表2)[4]。
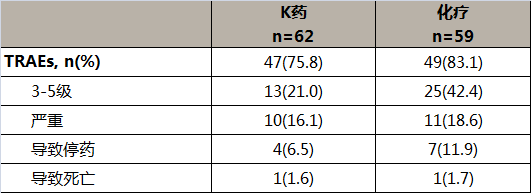 表二、帕博利珠单抗治疗(中位随访15.1个月)中国食管癌的3-5级TRAE发生率仅有化疗组(中位随访14.7个月)的一半
表二、帕博利珠单抗治疗(中位随访15.1个月)中国食管癌的3-5级TRAE发生率仅有化疗组(中位随访14.7个月)的一半
主要的TRAE为甲状腺功能减退,肝功能ALT和AST指标升高,便秘,恶心,肺炎,皮疹。与整体人群的不良反应一致,未显示有明显的东西方人种差异(表3)。
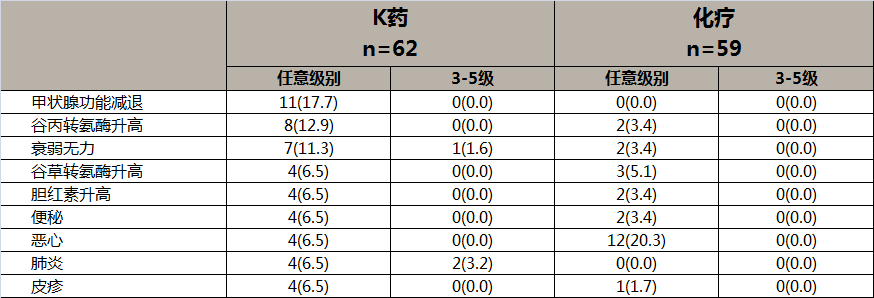 表三、帕博利珠单抗单药治疗中国食管癌患者的主要TRAEs[4]
表三、帕博利珠单抗单药治疗中国食管癌患者的主要TRAEs[4]
在所有PD-1/PD-L1免疫检查点抑制剂的研究中,围绕帕博利珠单抗开展的临床研究的数量是目前最多的,达到1050个[10]。 在已公布的多项III期临床研究中,帕博利珠单抗单药治疗不同瘤种的不良反应谱基本相同,没有出现新的不良反应;而且其治疗晚期非小细胞肺癌3年和5年不良反应谱也基本相同,5年随访没有出现新的不良反应[8]。
“但是,这并不代表免疫治疗食管癌,我们可以掉以轻心,也不代表其它PD-1的不良反应也有相同可靠性和可预测性,因为不同PD-1的疗效和安全性可能都不同”,赵教授指出。
当前在国内获批的四个国产PD-1单抗中,卡瑞利珠单抗是目前唯一已正式发布III期临床结果的PD-1单抗。卡瑞利珠单抗单药二线治疗食管癌的III期临床研究ESCORT于2019年世界食管癌大会上发布,该研究共入组457例中国患者,随机接受卡瑞利珠单抗(228例)或化疗(229例)。
与化疗相比,除了反应性毛细血管增生症(RCCEP)之外,几乎在其它所有不良反应发生率上,卡瑞利珠单抗组都要低于化疗组。 唯独RCCEP的发生率高达79.6%[1]; 而在已发布的K药或O药的III期临床研究中,都没有报道RCCEP的发生。
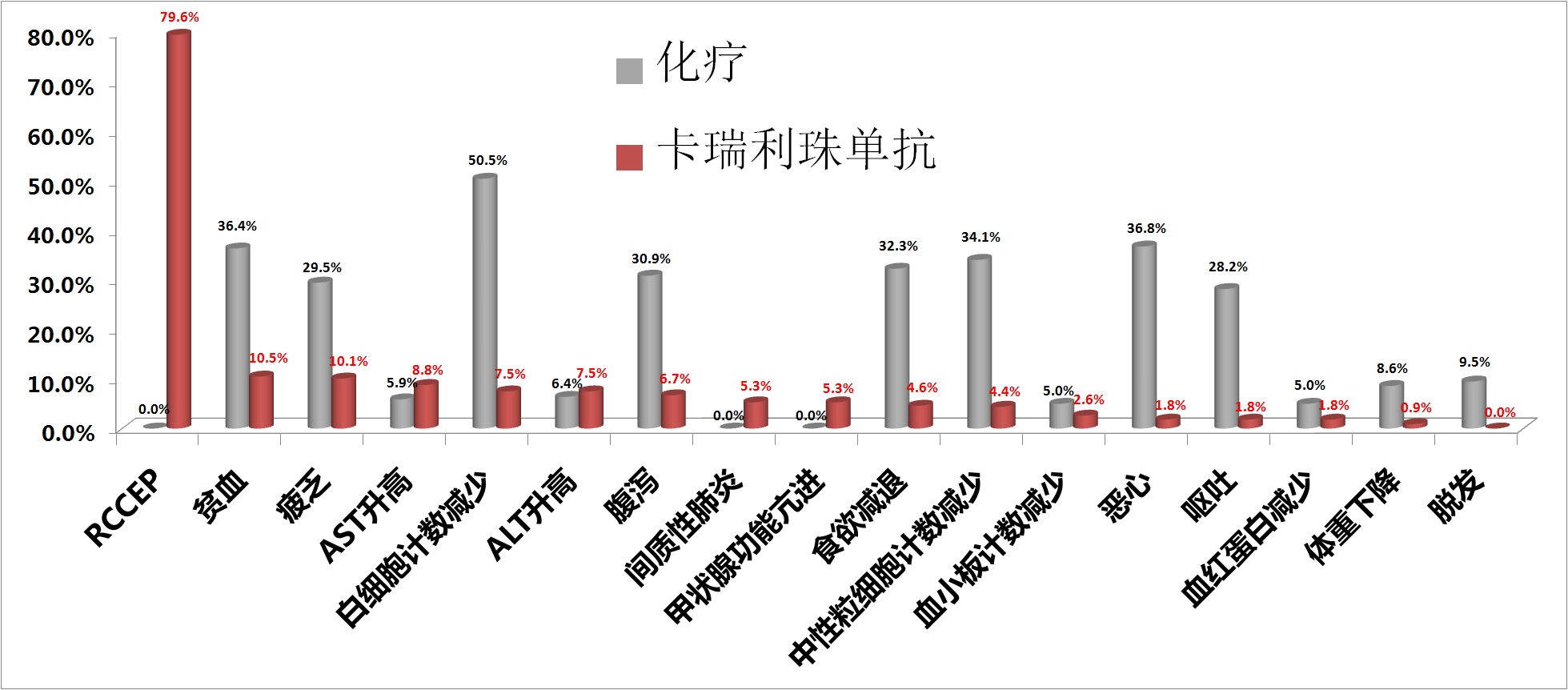 图二、卡瑞利珠单抗治疗组的RCCEP(反应性毛细血管增生)的发生率高达79.6%[1]
图二、卡瑞利珠单抗治疗组的RCCEP(反应性毛细血管增生)的发生率高达79.6%[1]
赵快乐教授指出,食管癌免疫治疗的临床应用仍处于早期,多数放疗、放化疗或外科医生对其临床应用仍缺乏实践经验,因此在临床应用时必须参考国内外指南推荐,依据可靠的临床研究数据结果,这样才能做出最佳的临床抉择。“同时,在临床实践中也要与患者保持沟通,充分说明各类PD-1的疗效和潜在的不良反应,供患者在综合考虑各方因素后做出最明智的选择”,赵教授补充道。
参考文献:
[1] Huang J et al., Phase 3 study of camrelizumab vs chemotherapy for locally advanced/metastatic esophageal cancer: The ESCORT Study, Oral Presentation at the 15th OESO World Conference for Esophaeal Diseases, Nov. 7-9th, 2019
[2] Cho BC et al., Nivolumab Versus Chemotherapy in Advanced Esophageal Squamous Cell Carcinoma: The ATTRACTION-3 Study. Oral Presentation, ESMO Congress, September 27-October 1st, 2019
[3] Shen L et al., 帕博利珠单抗对比化疗二线治疗晚期/转移性食管腺癌或鳞状细胞癌: KEYNOTE-181亚洲亚组分析, 口头报告, 2019 CSCO, 9月18日-9月22日
[4] Chen J et al., Pembrolizumab Versus Chemotherapy in Patients with Advanced/Metastatic Adenocarcinoma or Squamous Cell Carcinoma of Esophagus as Second-line Therapy: Analysis of the Chinese Sub-group in KEYNOTE-181, Abstract Presentation, ESMO, September 27th, 2019
[5] www.clinicaltrials.com
[6] 中华肿瘤杂志 2019 年 1 月第 41 卷第 1 期 Chin J Oncol, January 2019, Vol.41, No.1
[7] Antonia SJ, Villegas A, Daniel D, et al.Overall Survival with Durvalumab after Chemoradiotherapy in Stage III NSCLC[J].N Engl J Med. 2018;379(24):2342-2350
[8] 2019 年 CSCO 食管癌诊疗指南
[9] Yun Chen et al., Comparing Paclitaxel Plus Fluorouracil Versus Cisplatin Plus Fluorouracil in Chemoradiotherapy for Locally Advanced Esophageal Squamous Cell Cancer: A Randomized, Multicenter, Phase III Clinical Trial. J Clin Oncol, 2019, .
[10] www.merck.com
查看更多