查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





艾伯维(AbbVie)近日宣布,欧盟委员会(EC)已批准Rinvoq(upadacitinib,15mg)用于2个新的风湿适应证:(1)用于治疗对一种或多种疾病修饰抗风湿药物(DMARD)应答不足或不耐受的活动性银屑病关节炎(PsA)成人患者;(2)用于治疗对常规疗法应答不足的活动性强直性脊柱炎(AS)成人患者。
欧盟之前已批准Rinvoq用于治疗中度至重度类风湿性关节炎(RA)成人患者。此次最新批准,Rinvoq成了欧盟批准的第一个可用于治疗3种风湿适应证(RA、PsA、AS)的口服、每日一次、选择性、可逆性JAK抑制剂。
此次批准基于3项关键临床试验SELECT-PsA 1、SELECT-PsA 2、SELECT-AXIS的数据,这些试验在多种疾病活动评价指标方面均证实了Rinvoq的疗效。
艾伯维研发部高级副总裁、首席科学官Tom Hudson医学博士表示:“银屑病关节炎和强直性脊柱炎对患者生活的许多方面都有重大影响。我们很自豪,Rinvoq作为PsA患者一种新的治疗选择,为AS患者提供同类首个(first-in-class)治疗选择。这些批准是我们致力于开发一系列解决方案的重要里程碑,这些解决方案将提高风湿病患者的护理标准。”
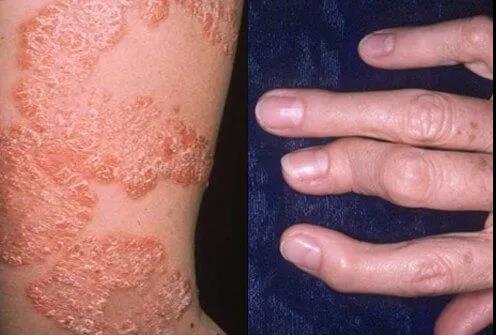
银屑病关节炎(图片来源:onhealth.com)
银屑病关节炎(PsA)是一种复杂的异质性疾病,表现跨越多个领域,包括关节和皮肤,导致日常疼痛、疲劳和僵硬。强直性脊柱炎(AS)是一种慢性、进行性、炎症性的肌肉骨骼疾病,主要引起脊柱疼痛和僵硬。PsA和AS的各种症状会给患者带来重大的生理、心理和经济负担。
Rinvoq治疗PsA的新适应证,基于2项III期临床研究SELECT-PsA-1(NCT03104400)和SELECT-PsA-2(NCT03104374)的数据支持。这2项研究入组了超过2000例活动性PsA患者,结果显示,与安慰剂相比,Rinvoq均达到了ACR20应答的主要终点。此外,15mg剂量Rinvoq与阿达木单抗在治疗第12周ACR20应答方面显示出非劣效性。接受Rinvoq治疗的患者在身体功能(HAQ-DI)和皮肤症状(PASI 75)方面也有更大的改善,并且有更大比例的患者达到了最低疾病活动度。
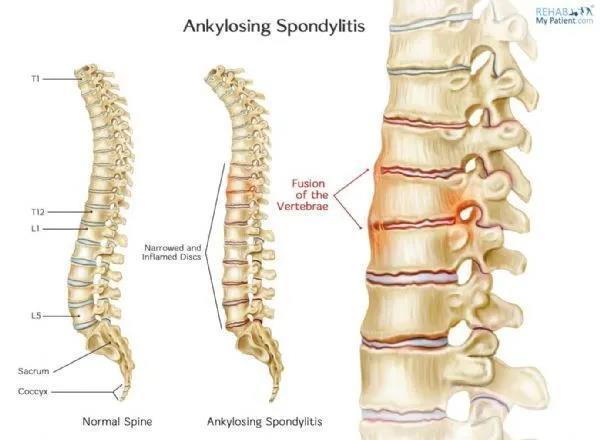
强直性脊柱炎(图片来源:rehabmypatient.com)
Rinvoq治疗AS的新适应证,基于2/3期SELECT-AXIS 1研究(NCT03178487)的数据支持。结果显示,与安慰剂相比,Rinvoq显著改善了活动性AS成人患者的症状和体征,治疗第14周达到ASAS40(国际脊柱关节炎学会评估改善40%)的患者比例提高一倍(52% vs 26%,p<0.001)。
在上述3项临床研究中,Rinvoq的安全性与之前报道的类风湿性关节炎临床试验结果一致,没有发现新的重大安全风险。
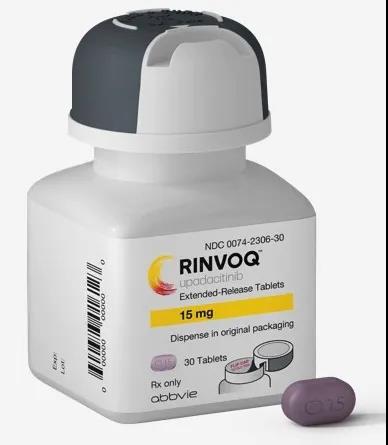
Rinvoq的活性药物成分为upadacitinib,这是由艾伯维发现和开发的一种口服选择性和可逆的JAK1抑制剂,正被开发治疗数种免疫介导的炎症性疾病。JAK1是一种激酶,在多种炎症性疾病的病理生理过程中发挥了关键作用。
2019年8月,Rinvoq在美国获得全球首批,用于治疗对氨甲蝶呤(MTX)应答不足或不耐受的中度至重度活动性类风湿性关节炎(RA)成人患者。2019年12月,Rinvoq获得欧盟批准,用于治疗对一种或多种疾病修饰抗风湿药物(DMARD)应答不足或不耐受的中度至重度RA成人患者。在RA中,Rinvoq批准的剂量为15mg。
目前,艾伯维正在开发Rinvoq用于治疗多种炎症性疾病,包括银屑病关节炎(PsA)、RA、中轴型脊柱关节炎(axSpA)、克罗恩病(CD)、特应性皮炎(AD)、溃疡性结肠炎(UC)、巨细胞动脉炎(GCA)。
本文首发于生物谷公众号,账号主体系上海春谷生物医药科技有限公司
查看更多