查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





3月18日,Kiniksa公司宣布,美国食品和药物管理局(FDA)已批准该公司开发的重组融合蛋白ARCALYST (rilonacept) 上市,每周皮下注射1次,用于治疗12岁及以上儿童和成人复发性心包炎,并降低心包炎复发风险。rilonacept是FDA批准的首个治疗复发性心包炎的药物。

复发性心包炎是一种疼痛性自身炎症性心血管疾病,典型表现为胸痛,通常与心电传导改变和心脏周围积液有关。复发性心包炎严重影响患者生活质量,限制机体活动,并导致频繁急诊和住院。数据显示,美国每年约有4万名复发性心包炎患者寻求并接受治疗。受长期基础性疾病或对传统治疗[如非甾体抗炎药(NSAID)、秋水仙碱和皮质类固醇]反应不足的影响,这些患者中大约有14000名经历了2次及以上复发。
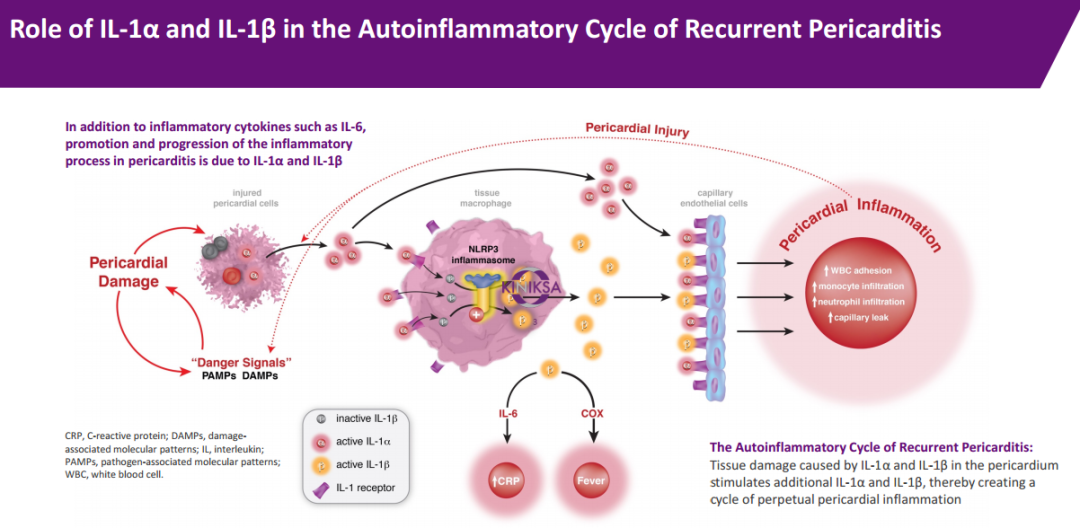
心包炎炎症过程的促进和进展除了与IL-6等炎症因子有关外,还与IL-1α和IL-1β相关,rilonacept是一款IL-1抑制剂,可同时阻断IL-1α 和IL-1β 通路,抑制由IL-1α 和IL-1β导致的心包炎症的循环。
FDA此次批准是基于rilonacept治疗复发性心包炎患者的关键Ⅲ期RHAPSODY研究结果。患者在接受首剂注射后,疼痛和炎症症状都有快速、持续的缓解,治疗应答的中位时间为5天,应答率为97%。随机接受rilonacept治疗患者发生心包炎复发事件的风险降低了96% (HR =0.04, p<0.0001),试验期间,rilonacept组患者92%时间无疼痛或仅经历轻微疼痛,而安慰剂组这一比例为40%(p<0.0001)。最常见的不良反应是注射部位反应和上呼吸道感染。该研究数据已发表于《新英格兰医学杂志》上。

Rilonacept最初由Regeneron发现,并于2008年2月获FDA批准用于治疗周期性综合征(CAPS),包括家族性寒冷型自身炎症综合征(FCAS)、穆-韦二氏综合征(MWS) ,2020年12月,rilonacept获FDA批准用于IL-1受体拮抗剂缺乏症(DIRA)患者的维持缓解治疗 。
首发于医药魔方Info公众号
作者:拾贝
查看更多