查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





人工智能赋能乳腺癌个体化治疗专刊
Cancer Biology & Medicine
据统计,乳腺癌已成为全球女性发病率最高的恶性肿瘤,每年新发病例超过230万。面对这一沉重的疾病负担,乳腺癌诊疗领域正以前所未有的速度演进——精准医学不断深入临床实践,人工智能逐步赋能诊疗决策,国内外学者的研究步伐也在持续加快。在这一背景下,Cancer Biology & Medicine与中国人民解放军总医院江泽飞教授联合打造“人工智能赋能乳腺癌个体化治疗”专刊,旨在汇聚顶尖专家的智慧,系统呈现乳腺癌诊疗领域的新进展、新思考和新突破。
准确检测PIK3CA突变对于指导乳腺癌PI3K靶向治疗至关重要,但测序技术尚未普及,且单一模态的预测模型性能有限。针对这一临床挑战,河北医科大学第四医院刘月平教授联合首都医科大学宣武医院滕梁红教授及四川大学生物医学工程学院韩骁教授团队成功构建了一种整合病理全切片图像与临床数据的多模态深度学习框架,通过利用多模态信息的互补性,评估其在提升突变预测准确性、稳健性及跨数据集泛化能力方面的潜力。同时,结合可解释性分析观察模型关注的病理与临床特征,为进一步优化乳腺癌精准诊疗策略提供了新的研究思路和参考依据。该研究成果发表在本期专刊中。

Cite

Miao J, Liu Q, Zhao J, Fan S, Wang S, Ye F, et al. Multimodalartificial intelligence predicts PIK3CA mutation in breast cancer from digitalpathology and clinical data: a multicenter study. Cancer Biol Med. 2026; 23:430-450. doi: 10.20892/j.issn.2095-3941.2025.0771
内容介绍
本研究成功构建并验证了一种基于多模态人工智能的融合框架——多模态PIK3CA模型(MPM),用于预测乳腺癌PIK3CA突变状态。研究纳入了来自癌症基因组图谱(TCGA)数据集的1047例患者,以及来自河北医科大学第四医院(HBMU)、首都医科大学宣武医院(CMU)和四川大学华西医院(SCU)三家独立医疗中心的166例患者作为外部验证队列,构建了覆盖不同人群、不同医疗机构的多样化数据集。所有病例均经过标准化组织处理、组织学扫描及基因检测,确保数据质量与一致性。
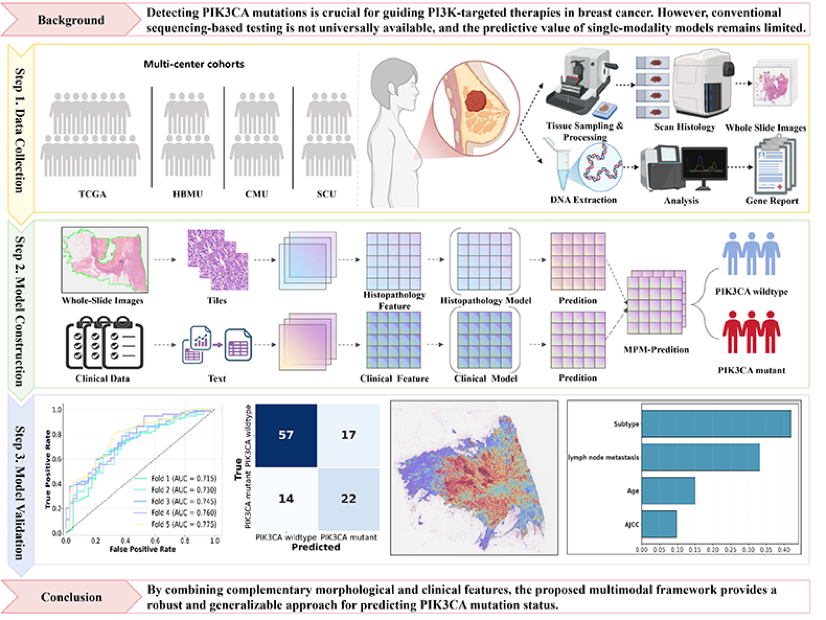
研究流程图
病理模型表现
组织病理学分支采用基于Transformer架构的预训练编码器H-optimus-0作为特征提取器,通过CLAM-SB多示例学习框架生成全切片图像级别的表示。H-optimus-0在TCGA测试集上取得了0.715的AUC表现,优于UNI-V2、CTransPath等其他四种先进病理学基础模型,并被选为最终病理分支的特征编码器。该模型在外部验证集中保持了稳定的泛化能力,在HBMU、CMU和SCU三个中心分别取得0.680、0.680和0.670的AUC,证明了其在不同染色和扫描条件下的稳健性。
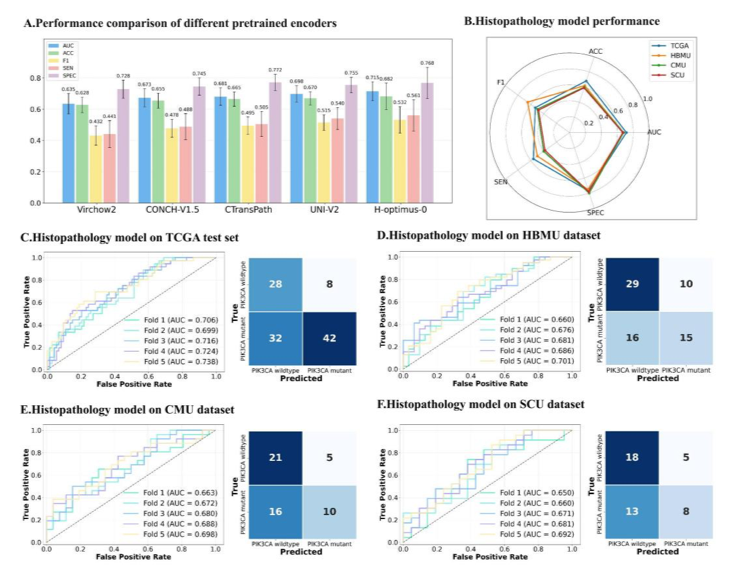
组织病理学分支在不同数据集上的性能表现
(A)不同预训练编码器的预测性能比较;(B)各中心AUC、ACC、F1、SEN和SPEC指标的雷达图汇总;(C-F)组织病理学模型在TCGA测试集、HBMU数据集、CMU数据集和SCU数据集中的ROC曲线及对应的混淆矩阵。
临床模型表现
临床分支整合了年龄、分子分型、淋巴结转移状态和AJCC分期四个核心临床变量,采用XGBoost算法进行建模。XGBoost在TCGA数据集上取得了0.694的AUC表现,优于其他四种机器学习算法,选为最终临床模型的分类器。该模型在外部验证集中保持了稳定的泛化能力,在HBMU、CMU和SCU三个中心分别取得0.660、0.640和0.650的AUC,证明了其在不同临床数据分布下的稳健性。显示出良好的泛化能力。
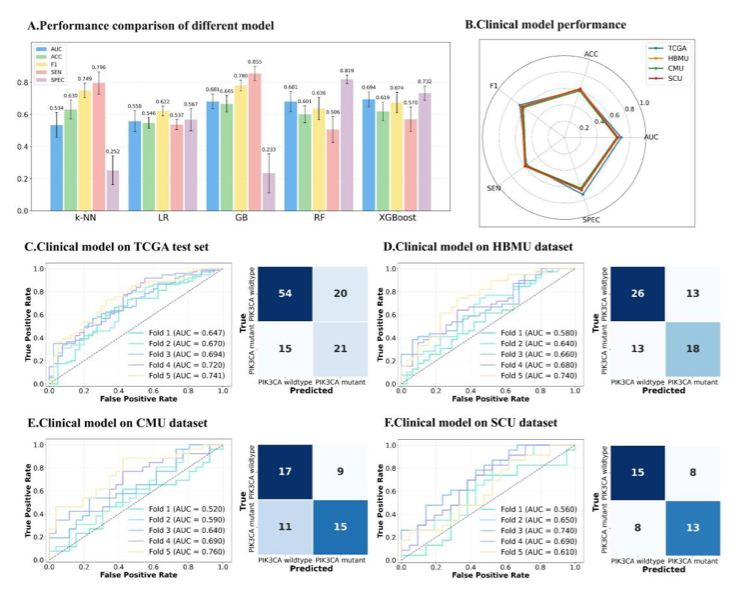
临床分支在不同数据集上的性能表现
(A)多种机器学习分类器的性能比较;(B)各中心模型性能指标的雷达图汇总;(C-F)临床模型在TCGA测试集、HBMU数据集、CMU数据集和SCU数据集中的ROC曲线及对应的混淆矩阵。
多模态融合(MPM)模型优势
MPM模型采用了决策层后融合策略,结合了图像和临床两个分支的概率输出 。结果显示,MPM的预测性能显著优于单一模态模型,其在TCGA数据集上实现了0.745的AUC。在三个外部验证队列中,MPM保持了高度稳定的性能:HBMU队列AUC为0.695,CMU队列AUC为0.690,SCU队列AUC为0.680,且在各中心均展现出平衡的敏感性与特异性。校准曲线分析显示MPM的预测概率与实际事件发生率高度一致,决策曲线分析进一步验证了其在0.020-0.500阈值概率范围内相较于“全部测序”和“不测序”两种传统策略具有更高的临床净收益。
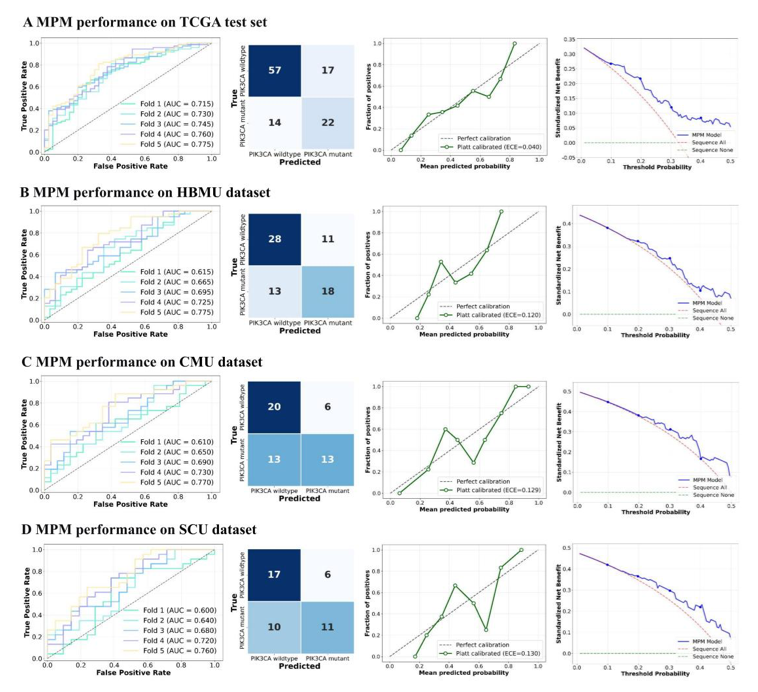
多模态PIK3CA模型(MPM)的性能表现
MPM在四个独立队列中的ROC曲线、混淆矩阵、校准曲线及决策曲线分析结果:(A)TCGA测试集;(B)HBMU数据集;(C)CMU数据集;(D)SCU数据集。
模型可解释性分析
组织病理学模型的注意力热图分析显示,模型精准聚焦于肿瘤富集区域,且此聚焦模式在多中心数据集中高度一致,证明了其强大的可解释性与跨中心稳健性。临床模型的SHAP分析则揭示分子分型是预测PIK3CA突变风险的关键正向特征,并量化了各临床特征的独立与交互影响模式。
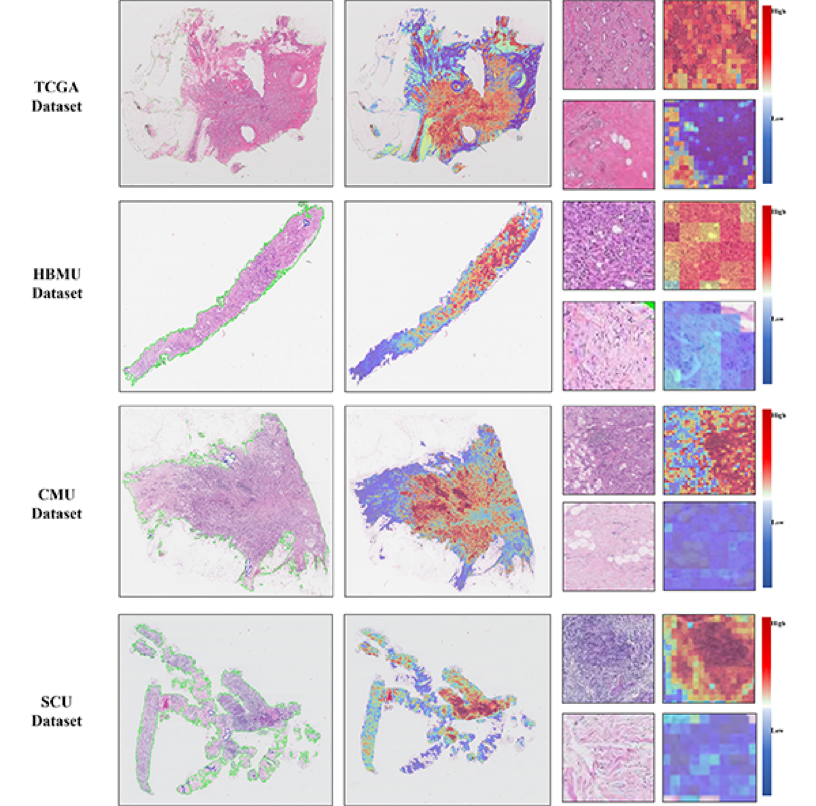
PIK3CA突变预测的WSI区域注意力热图
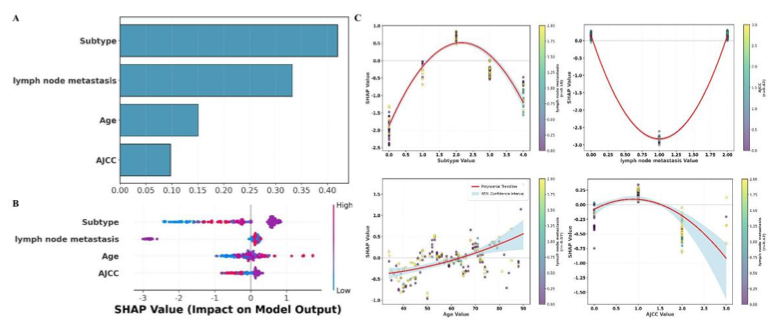
基于SHAP的临床特征模型可解释性分析
(A)基于平均绝对SHAP值排序的全局特征重要性;(B)展示特征层面贡献的SHAP蜂群图;(C)展示关键特征交互模式的SHAP依赖图。
小结
该多模态人工智能框架有效整合了互补的组织形态学和临床信息,为预测乳腺癌患者的PIK3CA突变状态提供了一种稳健且具有强泛化能力的新方法。通过系统比较多种病理基础模型与机器学习算法,为后续研究提供了方法学参考;通过可解释性分析揭示了突变相关的形态学与临床特征,加深了对PIK3CA突变生物学的理解。
未来将进一步扩大外部验证队列规模,纳入更多样化的人群以进一步提升模型的泛化能力;探索更深层次的多模态融合策略,如特征级融合或基于注意力机制的联合学习;将该框架扩展至其他驱动基因突变(如TP53、HER2)及治疗反应预测;整合纵向临床数据与治疗史,实现疾病演变的动态建模;将MPM作为预筛选工具整合至数字病理工作流程,优化分子检测资源分配,推动精准肿瘤学的临床转化。
通信作者
刘月平 教授
河北医科大学第四医院
博士生导师
河北省肿瘤医院/河北医科大学第四医院病理科主任
中华医学会病理学分会常务委员
中华医学会病理分会乳腺疾病学组组长
中国抗癌协会肿瘤病理专委会乳腺肿瘤学组组长
中国临床肿瘤学会(CSCO)肿瘤病理专家委员副主委
中国医师协会病理科医师分会常务委员
河北省医学会病理学分会主任委员
河北省医师协会病理科医师分会主任委员
《临床与实验病理学》副主编
滕梁红 教授
首都医科大学宣武医院
首都医科大学宣武医院病理科 主任
中华医学会病理学分会第十四届常务委员
中华医学会病理学分会第十四届脑神经病理学组组长
国家卫生健康委能力建设和继续教育病理学专家委员会副主任委员
中国医疗保健国际交流促进会病理学分会副主任委员
中国医师协会病理医师分会委员
中国抗癌协会肿瘤病理专委会常委
北京医学会病理学分会副主委
北京市病理质量管理与控制中心副主任
韩骁 教授
四川大学生物医学工程学院
四川大学特聘研究员,博士生导师;
美国约翰霍普金斯大学 博士,哈佛医学院博士后;
曾担任腾讯AI Lab专家研究员及AI医疗中心负责人;
在国际知名杂志和会议上发表论文100余篇,谷歌学术引用超12,000次;
近5年连续入选斯坦福大学发布的全球前2%顶尖科学家“终身科学影响力和“年度科学影响力”双榜单;
获得已授权美国国家技术专利30余项以及中国国家技术专利40余项;
2022年获得中国国际大数据产业博览会领先科技成果奖;
来源:Cancer Biology Medicine
查看更多