查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





作者:郑州市中心医院卒中中心 周玉帅 贾新州


本文报告一例71岁女性因急性缺血性中风(AIS)就诊于急诊科。她接受了rt-PA和介入血管内血管重建治疗后,出现快速进展的血管性水肿,导致紧急插管,然而常规的治疗效果不理想,在输注新鲜冷冻血浆(FFP)后有所改善。
rt-PA输注后的血管性水肿可能是一种危及生命的紧急情况,需要由熟练的专业人员快速进行气道管理,由于这种情况是由多种因素导致的,如:不受调节的组胺和缓激肽的产生,指南推荐的传统治疗方法可能还不够充分,FFP的使用可以被认为是一种安全和有价值的辅助手段。


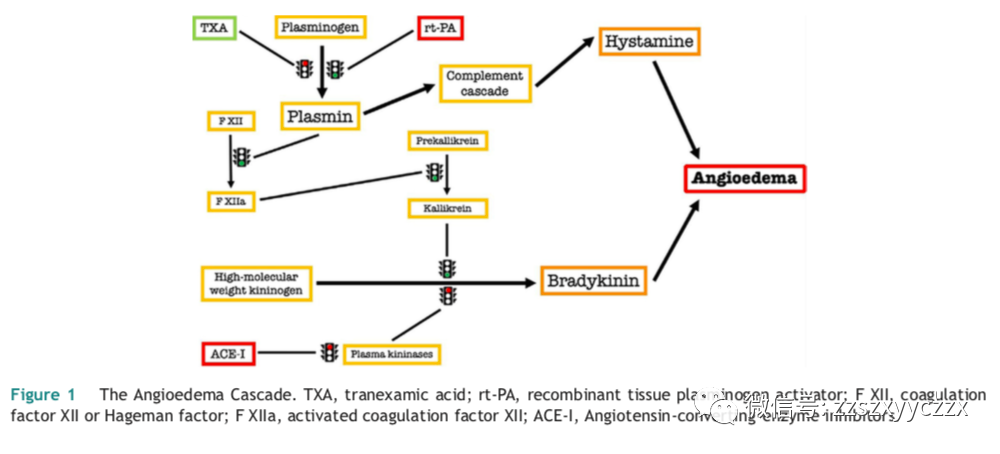
rt-PA是急性缺血性卒中(AIS)患者的一种标准治疗方法,口舌血管性水肿是该药物的一个众所周知的副作用,AHA/ASA指南中关于AIS的管理中描述这种情况的紧急救治措施。在大多数血管性水肿病例为轻到中度,但有一小部分可能导致气道紧急情况,需立即需要插管。rt-PA给药后产生血管性水肿的完整途径仍有争议,但已确定这是由于rt-PA引起的组胺和缓激肽的产生增加所致,如图1。伴随C1抑制剂缺乏的遗传性血管性水肿患者更容易发生血管性水肿;这种罕见的情况患者也未必知道,因此在收集病史时可能忽略掉。
另一个相关的危险因素是使用ACEI类药物,它可以促进缓激肽的形成,引发或加重血管性水肿。在一些血管性水肿的案例中,使用类固醇、H1拮抗剂、H2拮抗剂和肾上腺素和一些急救措施可能无效。
下面我们描述了一例血管性水肿导致气道紧急事件,应用传统的急救措施无效,然而使用FFP抢救成功。


一位71岁女性,近期有高血压病史,曾接受雷米普利和氢氯噻嗪,因突发完全性失语、右侧偏瘫、完全性注视麻痹和完全性右侧偏盲急诊入院(基线NHISS评分12分)。无药物过敏史,CTA显示左侧大脑中动脉M1段闭塞,CTP存在缺血半暗带。患者无禁忌证,首先给予阿替普酶,后在全麻下行血管内治疗,术中应用咪达唑仑,氯胺酮、罗库溴铵用于诱导,小剂量异丙酚、瑞芬太尼用于维持。通过两次血栓抽吸后获得完全血运重建(TICI 3)。手术结束时,在拔除气管内插管(ETT)后,麻醉师注意到左侧嘴唇和舌头肿胀。
患者开始呼吸急促,打鼾,不吸氧情况下氧和 89%,鼻导管吸氧后升高至93%。考虑到肿胀的逐渐恶化,首先给药氢化可的松100mg,氯苯那明30mg肌肉注射和肾上腺素(500mcg和 1mg)肌肉注射,但是症状无改善。由于神经系统状况恶化和即将出现气道阻塞的迹象,按照疑似covid-19感染患者的预防措施,在可视喉镜下行气管插管;由于舌部和声门肿胀恶化,该操作导致气管插管放置困难。在气管插管过程中,患者出现因房颤伴快速心室率导致的血流动力学不稳定,同步电复律后恢复窦性心律,在气管插管后约1小时进行了鼻喉镜检查,结果显示声门和舌基部的肿胀进一步加重。
这时有人考虑缓激肽介导的血管性水肿有两个原因:首先是瑞芬太尼和罗库溴铵通过增强组胺的释放加快血管性水肿,第二个原因是,尽管一半舌头的血管性水肿更常位于缺血半球的对侧,但与rt-PA给药相关,特别是使用ACE-I患者中,这在文献中有广泛描述。
由于常规药物治疗无法改善血管性水肿,因此考虑使用艾卡替班特(icatibant缓激肽拮抗药),但由于该药物不容易获得,因此决定输注新鲜冷冻血浆(FFP)作为抢救治疗,以恢复激肽酶II水平。患者在开始输注FFP(600mL)后不久,舌水肿迅速改善。入ICU12小时后进行了袖带泄漏试验,结果显示有持续的气道阻塞。血清胰蛋白酶水平正常,36小时后的脑部CT显示在中央前回有一个小的缺血性病变,无脑出血改变。36小时后,患者血管管水肿完全消失,第二次袖漏试验为阴性,给予拔出气管拔管。在ICU期间和随后的几天内,我们都进行了准确的凝血功能监测,提示不需要提供纤维蛋白原。
考虑到病人是一个外国人,独自生活在博洛尼亚,在头几天我们通过第三方间接与她的儿子取得联系,但由于严重语言障碍,不清楚病人或近亲既往是否有过类似情况。据我们所知,该患者没有接受C1酯酶缺乏症的筛查,第3天患者从ICU转至卒中病房,一周后出院,无后遗症。


本病例描述了rt-PA输注后需要紧急插管的血管性水肿的处理。与rt-PA给药相关的血管性水肿是一种相对罕见的事件,发生率约为1%-5%,但可能会有非常严重的后果。最重要的风险因素是ACE-I使用和潜在的病理生理学对治疗方案具有重要意义。ACE-I抑制激肽酶II是代谢缓激肽的三种锌金属蛋白酶之一,从而增加该激肽家族成员的血浆水平。
另外,rt-PA将纤溶酶原分解为纤溶酶,从而将激肽原转化为缓激肽,路径如图1所示。缓激肽是一种强大的血管扩张剂,可增加血管通透性,允许液体进入间质组织。患者还可能伴有错误识别的C1-酯酶缺乏,导致遗传性血管性水肿;C1-酯酶通常通过抑制激肽释放酶和XIIa因子来限制缓激肽的产生,因此这些患者出现反复的血管性水肿。在本案例报告中, 不能确定地排除这种可能性。
使用FFP的基本原理是恢复激肽酶II,以增加缓激肽的降解。
另一种治疗方案是艾卡替班特(icatibant),它通过阻断与缓激肽b2受体结合起到抑制缓激肽作用。AHA/ASA指南建议使用这种药物,但它相当昂贵,并不是每家医院都容易获得。
氨甲环酸可以通过减少纤溶酶的产生发挥作用,但在这种情况下,会增加颅内血栓形成的风险,应避免使用。
使用FFP治疗ACE-I诱导的血管性水肿已经被描述过了,但该治疗方案的经验仍很有限,此外,有许多使用 FFP治疗血管性水肿的病例报告,但没有一例与AIS输注rt-PA相关,主要原因可能是担心FFP可能会恶化颅内血栓形成,尽管没有证据表明存在这种风险,因此这种治疗,特别是在紧急情况下,可以被认为是安全的。
急诊治疗AIS的患者可能存在气道阻塞的潜在风险,以及血管造影过程中的镇静风险;血管性水肿可能进一步加剧这种风险,并导致困难气道的紧急管理。最重要的是,麻醉师要意识到接受溶栓治疗的患者有发生血管性水肿的风险,特别是有使用ACE-I史的患者。
在紧急情况下,迅速认识到这一问题也是初步治疗的基础, 这样能够更快地解决症状,从而缩短住院时间。
指南中建议的常规治疗方法可能无效,因此FFP可能在恢复激肽酶II水平方面发挥关键作用,FFP比艾卡替班特便宜,而且通常很容易获得,即使在一些小医院,开始输注阿替普酶过程,可同时安排患者转移到至卒中中心进行救治。
据我们所知,这是第一例使用FFP成功治疗rt-PA输注相关的血管性水肿;虽然患者出院时没有神经系统后遗症,但进一步研究使用FFP治疗这类患者的血管性水肿是可取的。
来源:郑州市中心医院卒中中心
查看更多