查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





2025年10月17日,我国自主研发的新型HER2 ADC博度曲妥珠单抗正式获得中国国家药品监督管理局(NMPA)批准上市,用于既往接受过一种或一种以上抗HER2药物治疗的不可切除或转移性HER2阳性成人乳腺癌患者。
紧随监管批准,该药的Ⅲ期临床研究(KL166-III-06)数据也在2025年ESMO年会这一全球肿瘤学顶尖学术舞台上,以重磅口头报告形式发布,其卓越的疗效与安全性赢得了国际学界的高度关注。学术突破与监管批准的同频共振,彰显了中国创新药物研发体系日臻成熟,标志着本土高质量临床研究证据同时获得了学术前沿与监管体系的双重认可。与此同时,我国另一款原研TROP2 ADC芦康沙妥珠单抗在HR+/HER2-晚期乳腺癌领域的OptiTROP-Breast02研究也在本次大会上公布了突破性成果,进一步夯实了ESMO年会的“中国证据”矩阵。值此里程碑时刻,我们特别邀请到本领域权威专家、天津医科大学肿瘤医院张瑾教授,特通过视频形式为这一重要进展录制寄语。本文将系统梳理相关研究的核心数据,深入解读其临床价值与行业影响,展望中国创新药物研发的未来路径。

博度曲妥珠单抗的华彩破晓
中国之声,震撼世界

在HER2+乳腺癌治疗领域,博度曲妥珠单抗的突破性潜力,源于其对关键临床需求的精准把握与卓越的疗效验证。其Ⅲ期研究KL166-III-06是一项多中心、随机、开放、对照的临床试验,旨在头对头比较博度曲妥珠单抗与恩美曲妥珠单抗(T-DM1)在既往接受过曲妥珠单抗和紫杉类治疗的HER2阳性不可切除或转移性乳腺癌患者中的疗效和安全性。该研究设计紧密贴合中国临床实践,入组患者中,53.8%既往晚期抗HER2治疗线数≥2,近60%有TKI治疗史,精准聚焦于后线治疗选择有限、疗效亟待提升的核心临床难题。
研究结果显示,博度曲妥珠单抗组展现出显著的生存获益——其中位PFS达到11.1个月,显著优于T-DM1组的4.4个月(HR=0.39)。
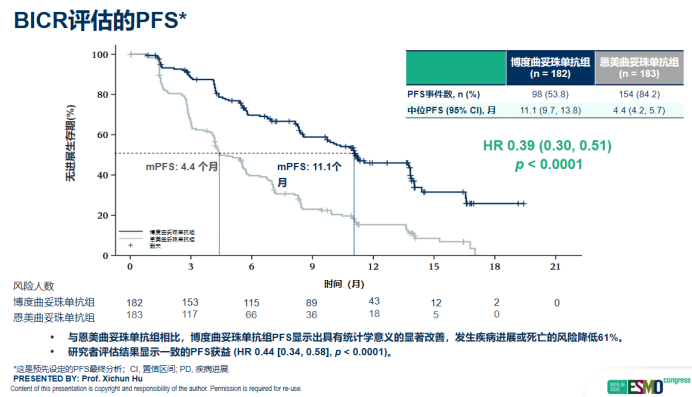
在肿瘤缓解方面,博度曲妥珠单抗组的ORR达到76.9%,显著优于T-DM1组的53.0%。
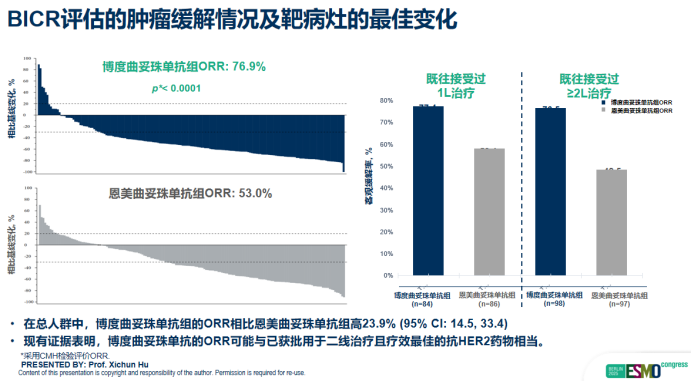
尽管OS数据尚未完全成熟,但博度曲妥珠单抗组已呈现出明确的早期获益趋势(HR=0.62),为患者的长期生存带来了积极信号。
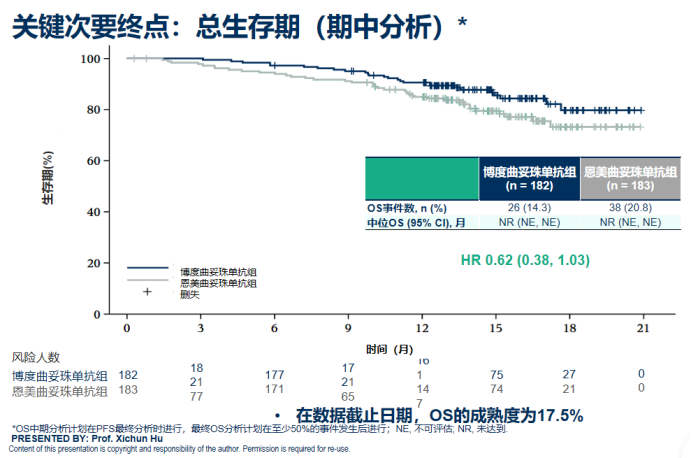
博度曲妥珠单抗基于卓越临床数据获得国家药品监督管理局正式批准,具有深刻的临床与现实意义。其获批为既往接受过抗HER2 TKI治疗的广泛人群提供了高级别循证医学证据支持的二线及以上治疗选择,进一步完善了我国HER2阳性晚期乳腺癌的治疗格局。
作为中国原研的创新药物,其获批显著提升了前沿精准治疗的可及性。本土研发与生产赋予了其在供应保障与成本控制上的潜在优势,这为后续纳入国家医保目录、切实减轻患者经济负担奠定了坚实基础,使更多中国患者能够及时获益于与国际先进水平接轨的创新疗法。
基于其卓越的临床证据与明确的治疗价值,博度曲妥珠单抗的上市将推动我国HER2+晚期乳腺癌治疗体系的进一步优化。这一进展标志着基于中国临床特征与需求研发的“中国方案”正逐步引领治疗策略的演进方向,体现了中国创新不仅致力于新药研发,更着眼于精准界定优势人群、优化临床实践路径,从而实现治疗效益的最大化,推动整体诊疗水平向更精准、更高效的新阶段持续迈进。

芦康沙妥珠单抗的璀璨征途
从TNBC到HR+/HER2-

在治疗选择匮乏、预后极差的三阴性乳腺癌领域,我国原研的芦康沙妥珠单抗同样展现了系统性的治疗价值与突破。作为中国首个获批上市的国产创新TROP2 ADC,其关键Ⅲ期研究OptiTROP-Breast01结果显示,在既往接受过至少两种系统治疗的局部复发或转移性TNBC患者中,芦康沙妥珠单抗组的中位PFS达到6.7个月,显著优于化疗组的2.5个月(HR=0.32)。在肿瘤缓解方面,芦康沙妥珠单抗组的ORR为45.4%,远高于化疗组的12.0%(P<0.00001),mDOR也优于化疗组(7.1个月vs 3.0个月),展现出卓越的抗肿瘤活性。基于此,国家药品监督管理局已于2024年11月正式批准其上市用于该适应证。
除后线治疗外,芦康沙妥珠单抗在前线治疗中也展现出拓展潜力。2025 ASCO大会上公布的OptiTROP-Breast05 Ⅱ期研究数据显示,芦康沙妥珠单抗一线治疗晚期转移性TNBC的ORR高达70.7%,mDoR为12.2个月,中位PFS达到13.4个月。这些数据显著超越了传统化疗在一线治疗中的疗效限制,为患者提供了更具优势的新型治疗选项,也为TNBC的前线治疗策略带来了重要突破。
值得关注的是,在PD-L1 CPS<10的晚期TNBC这一治疗选择受限的人群中,芦康沙妥珠单抗同样展现出突出的治疗价值。OptiTROP-Breast05研究数据显示,芦康沙妥珠单抗治疗组ORR达71.9%,中位PFS为13.1个月,12个月PFS率达59.1%,为这类患者提供了新的治疗方向。目前,聚焦PD-L1阴性,或PD-L1阳性且既往因早期乳腺癌接受过PD-1/PD-L1抑制剂治疗后复发的患者群体的Ⅲ期研究正在积极推进中,期待其研究结果为此类疗效不佳人群带来新的治疗希望。
芦康沙妥珠单抗的征程远未止步于TNBC,其在HR+/HER2-晚期乳腺癌领域取得的突破,进一步印证了其广谱的抗肿瘤潜力与我国药物研发的深远布局。2025 ESMO大会上公布的OptiTROP-Breast02研究结果,为CDK4/6抑制剂耐药后这一临床困境带来了破局之策。研究数据显示,芦康沙妥珠单抗组的中位PFS达到8.3个月,较化疗组的4.1个月实现倍增(HR=0.35)。在肿瘤缓解方面,芦康沙妥珠单抗组的ORR达到41.5%,显著优于化疗组的24.1%。尽管OS数据尚未成熟,但早期分析已显示出令人鼓舞的生存优势(HR=0.33)。这一成功不仅为临床医生提供了重要的决策依据,更从理念上引领了HR+/HER2-乳腺癌治疗模式的革新,证实了ADC在该亚型中同样能发挥卓越作用,推动治疗策略从传统内分泌治疗向精准治疗拓展。

星河璀璨
中国原研力量的崛起与全球贡献

纵观博度曲妥珠单抗与芦康沙妥珠单抗的研发历程与卓越成就,其背后折射出的正是中国医药创新体系中日益强大的“中国智慧”与“中国力量”。
在“中国智慧”层面,这两款药物展现了我国在创新药物研发领域的源头创新能力。通过差异化的分子设计、创新的技术平台和精准的临床开发策略,我们成功突破了传统技术路径的局限。这种基于深刻科学洞察与临床需求的研发思路,为中国创新药物的持续产出奠定了坚实基础。
在“中国力量”层面,我们见证了中国临床研究体系的快速成熟与国际影响力的提升。多项遵循国际标准的大型Ⅲ期临床研究的高质量完成与在国际顶级学术舞台上的成功展示,标志着中国临床研究质量实现了重要跨越。这不仅证明了我们具备执行全球水准临床研究的能力,更体现了中国学者在国际肿瘤学界日益提升的学术影响力与话语权。
展望未来,中国原创力量要继续推动全球乳腺癌诊疗进步,需要构建更完整的创新生态与全程管理理念。这意味着我们的探索应从晚期后线不断前移至前线、新辅助乃至辅助治疗场景,实现治疗阶段的全覆盖。我们坚信,这条立足中国、惠及世界,以严谨科学为基石、以患者需求为核心的创新路径,必将在全球乳腺癌诊疗体系中扮演越来越重要的角色。中国智慧与中国方案,正以其坚实的步伐,为构建人类卫生健康共同体贡献不可磨灭的力量,引领我们迈向一个乳腺癌患者高质量长生存的新时代。
二级教授、主任医师,博士生导师
中国天津乳腺癌防治研究中心常务副主任
天津医科大学肿瘤医院乳腺肿瘤三科科主任
国务院政府特殊津贴专家
第四届“国之名医”荣誉称号获得者
中国抗癌协会常务理事
中国抗癌协会乳腺癌专业委员会主任委员
中国抗癌协会整合乳腺癌委员会副主任
中国抗癌协会整合外科治疗委员会副主任
中国抗癌协会肿瘤多学科诊疗(MDT)专业委员会副主任委员
中华医学会肿瘤学分会委员
中华医学会肿瘤学分会恶性肿瘤早诊早治学组副组长
中华医学会外科学分会乳腺癌学组委员
中国医师协会外科医师分会乳腺外科专家工作组副组长
中国医师协会肿瘤多学科诊疗(MDT)专家委员会常委
天津市医学会肿瘤学分会主任委员
天津市抗癌协会常务理事
天津市乳腺癌质控专家委员会主任
审核丨天津医科大学肿瘤医院张瑾教授
查看更多