查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





作者:上海交通大学附属第六人民医院 李连喜
脆性糖尿病是指血糖波动极大、血糖极不稳定的一类糖尿病。患者高血糖与低血糖交替出现,血糖增高时容易发生酮症或酮症酸中毒,血糖降低时又容易出现低血糖甚至低血糖昏迷。脆性糖尿病见于胰岛功能差的糖尿病患者。脆性糖尿病不仅对患者的生活造成了严重影响,而且对内分泌科医生而言,脆性糖尿病的临床处理也十分棘手,极富挑战,是一个临床难题!
今天分享1例脆性糖尿病患者的临床诊治过程,经过治疗方案的合理调整,患者血糖波动明显减少,经较长时间的随诊观察,患者血糖也得到了较好的控制。
患者,男性,40岁。因“消瘦、口干、多饮3年,间断心慌2年”入院。
患者2016年下半年无明显诱因出现消瘦、口干、多饮,半年内体重下降5 kg,每日饮水量在2500 ml以上。在上海市某医院门诊查血糖17 mmol/L,糖化血红蛋白10%,诊断为2型糖尿病,予地特胰岛素早 5 U,睡前8 U皮下注射,共使用3个月,胰岛素治疗后患者多次无明显诱因出现夜间心慌、出汗、饥饿感,即时测血糖多在3.0~3.5 mmol/L,自行进食后症状可好转,每周发生2~3次。
外院调整地特胰岛素剂量(具体不详),1个月后低血糖发作次数减少,1次/月。空腹血糖控制在6~7 mmol/L,餐后2小时血糖控制在7~10 mmol/L。降糖方案改为二甲双胍500 mg tid,沙格列汀5 mg qd,服用半年,血糖控制同前,但体重仍继续下降,仍有间断口干、多饮。
自行转至上海市另一家医院求治,降糖方案改为二甲双胍500 mg tid,西格列汀100mg qd,但血糖失控,空腹血糖在8~10mmol/L,餐后血糖在12~15 mmol/L。
2018年初在上海市某医院住院治疗,查糖化血红蛋白10.69%,C-肽空腹0.76 μg/L,C肽60分钟1.24 μg/L,C肽120分钟 1.87 μg/L,抗谷氨酸脱羧酶抗体增高,为32.99 IU/ml。调整降糖方案为:地特胰岛素6 U睡前皮下注射 qd,门冬胰岛素 早6u 中3u 晚5u 三餐前即刻皮下注射,沙格列汀5 mg qd,阿卡波糖50 mg qd。半年后,患者体重增加5kg左右,血糖控制尚可,空腹血糖6~7 mmol/L,餐后2小时血糖10 mmol/L以下。
但近2年患者常有心慌、出汗、饥饿感等低血糖症状发作,即时测血糖多在3.0~3.5 mmol/L,最低2.5 mmol/L,自行进食糖果后症状可好转。晚餐前血糖较高,多在10~12mmol/L,外院门诊调整降糖方案为:沙格列汀5mg qd(中餐前服),服用1月后血糖无明显改善,调整三餐前胰岛素,改为生物合成人胰岛素注射液 早6u 中4u 晚5u,餐前30分钟皮下注射,血糖控制尚可,晚餐前血糖10 mmol/L以下。2019年底患者生物合成人胰岛素注射液改为门冬胰岛素,剂量不变。
3个月前患者血糖失控,空腹血糖常在10 mmol/L以上,餐后2小时血糖15~18 mmol/L。20天前在上海某医院住院诊治,馒头餐试验:C-肽空腹 0.03 μg/L,C肽60分钟 0.15 μg/L,C肽120分钟 0.24 μg/L,降糖方案改为:甘精胰岛素7u 晚9时皮下注射,门冬胰岛素早8u 中5u 晚5u 餐前即刻皮下注射,但血糖仍控制不佳,血糖波动仍较大,时有低血糖发作,血糖最低2.3 mmol/L,最高为21.5 mmol/L。
外院近期实验室及辅助检查结果如下:
甲状腺功能及抗体:游离T3 6.34 pmol/L,游离T3 19.28 pmol/L,TSH 3.37,抗甲状腺球蛋白抗体(TGAb)< 10 IU/ml,抗甲状腺过氧化物酶抗体(TPOAb) 11.6 IU/ml。
甲状腺超声:双侧甲状腺回声欠均,请结合甲功,右侧甲状腺胶质潴留。
血管超声:双侧颈动脉内膜光滑,管腔通畅,未见明显斑块形成,双侧股、腘动脉内膜毛糙伴斑片样强回声形成。
心电图:正常范围心电图。
眼底照相:未见明显异常。
神经电图及神经传导速度: 未见明显多发性周围神经损害性电生理改变。
患者因血糖波动大,血糖控制差,且常有低血糖发作,故来作者所在医院就诊。为进一步调整降糖方案,将患者收入院诊治。
入院后进一步询问病史,患者发病以来无视物模糊,无泡沫尿,无胸闷及心悸,无四肢麻木及疼痛,无间歇性跛行。患者起病以来,睡眠正常,每晚约6~7小时。精神尚可,胃纳可,大便如常,小便如常,体重近3月下降约1 kg左右。
既往否认高血压病史。否认血脂异常史。有糖尿病家族史。
入院体检:BP 98/72 mmHg,身高 168 cm, 体重 61.5 kg, 体质指数21.8 kg/m2, 腰围 78 cm, 臀围 89 cm。神志清醒,呼吸平稳。颈软,甲状腺无肿大。颈静脉无怒张,双肺呼吸音清,未闻及啰音,心率72次/分,心律齐,各瓣膜区未闻及病理性杂音。腹部平坦,无压痛,无肌卫,无反跳痛,肝肋下未及,脾肋下未及,无叩痛,无移动性浊音。双下肢无浮肿。无胫前斑,双侧足背动脉搏动正常。无足部溃疡。
因为患者入院前已经在其他医院做了比较详细的检查,故入院后主要补充了以下检查:








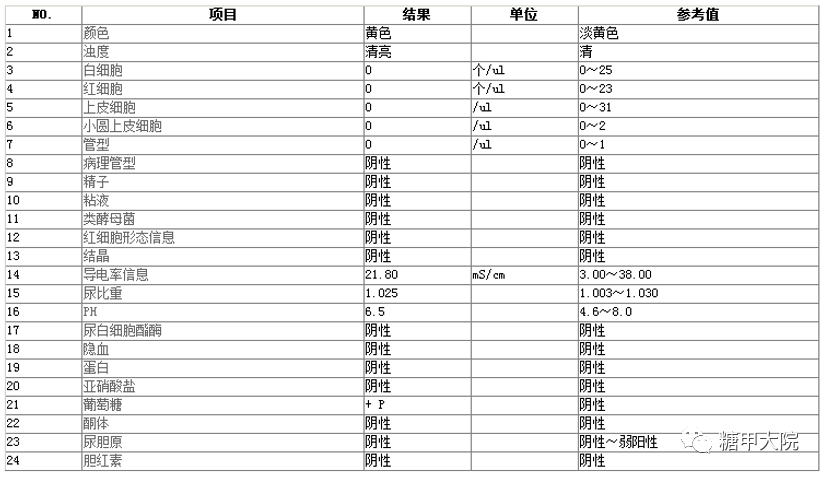
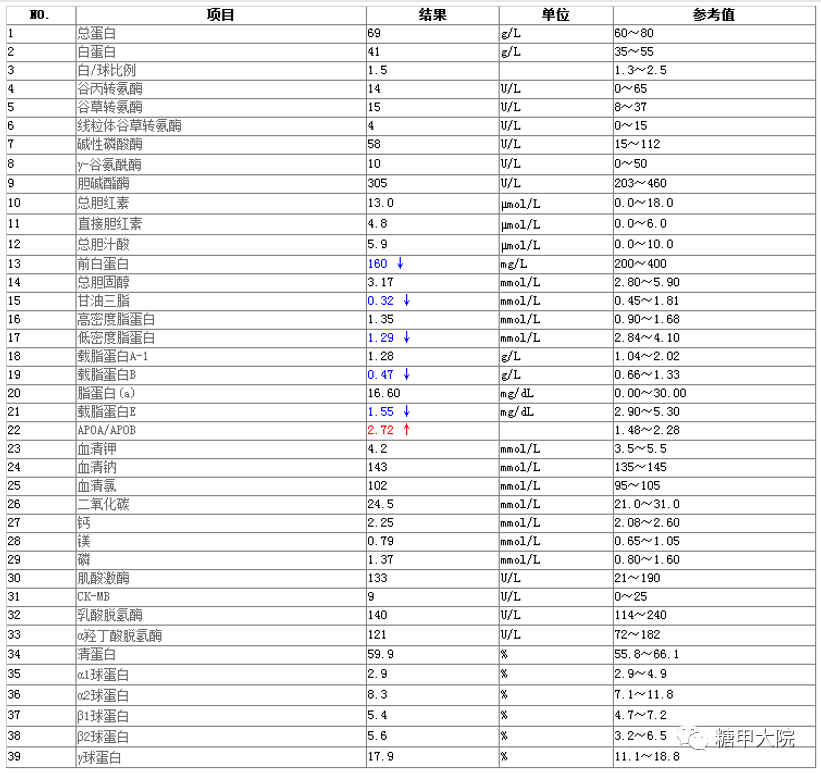


根据入院前其他医院检查结果及入院后本院检查结果,诊断比较明确,考虑1型糖尿病(LADA),同时存在下肢动脉粥样硬化,无其他糖尿病慢性并发症。患者胰岛功能差,血糖波动大,以高血糖为主,伴低血糖。
入院后首先嘱患者每天的饮食特别是主食量尽可能保持恒定,另外每天可以适当运动,但运动时间及运动量也尽可能固定。同时将降糖方案调整为:
门冬胰岛素 早8u 中5u 晚5u,三餐前皮下注射;停用甘精胰岛素,换德谷胰岛素12u睡前皮下注射;加阿卡波糖100mg tid,餐中服用。
通过血糖监测,发现患者使用以上治疗方案后,血糖控制仍不理想,中餐前和晚餐前血糖偏低,而中餐后和晚餐后血糖又偏高。根据患者的血糖谱特点,我们把白天的门冬胰岛素换成了作用时间更快的谷赖胰岛素,睡前德谷胰岛素不变,另外阿卡波糖也继续服用,治疗方案调整如下:
谷赖胰岛素 早12u 中8u 晚8u,三餐前皮下注射;德谷胰岛素16u睡前皮下注射;阿卡波糖100mg tid,餐中服用。
后面几天根据患者血糖监测结果,适当调整胰岛素剂量,患者最终出院时血糖得到了比较理想的控制,而且没有低血糖发作。
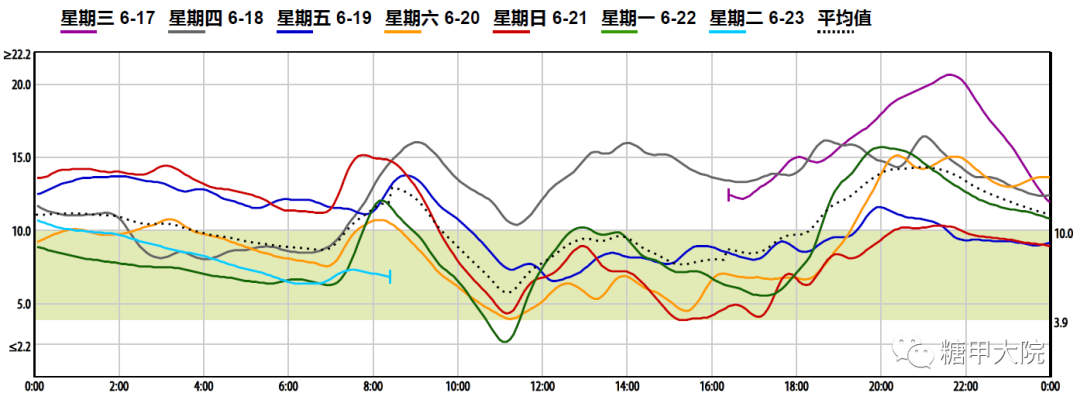
下面的图是患者在住院期间手指血糖的监测结果以及住院期间降糖方案调整的详细过程。可以看出,换用了谷赖胰岛素和德谷胰岛素后,患者血糖控制理想,而且没有小于3.9 mmol/L的低血糖发作。
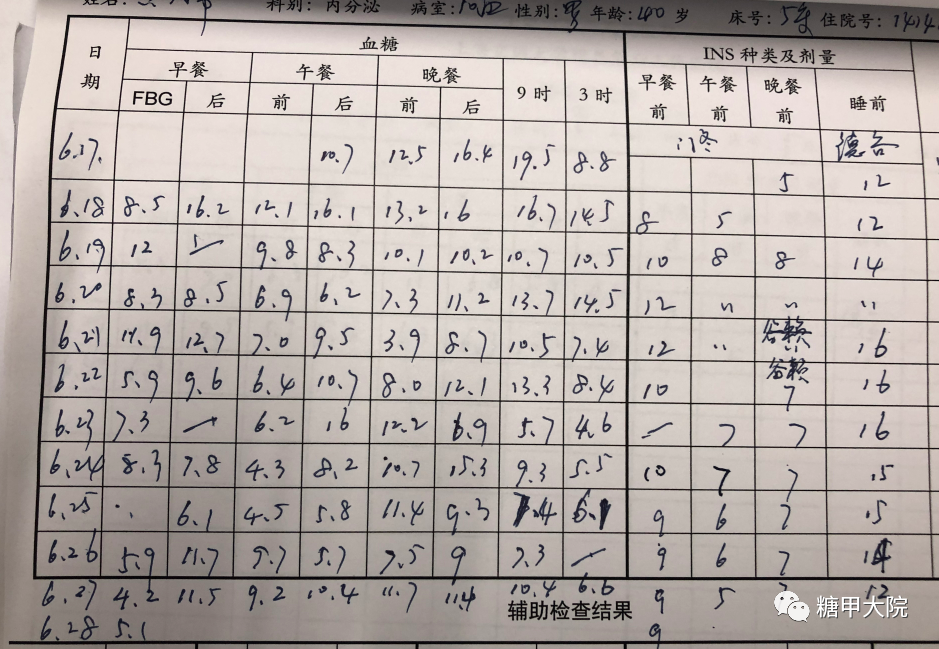
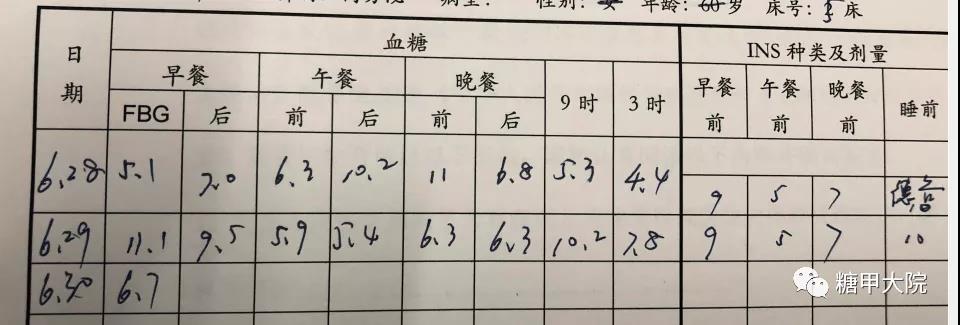
患者2020年11月,距离出院后大约4个月左右来门诊随访,复查糖化血红蛋白(HbA1c)有明显下降,从住院时的8.5%降到了现在的7.3%,提示血糖控制有明显改善,而且低血糖也很少再发生。

这个患者以前用过短效胰岛素包括门冬胰岛素,也用过甘精胰岛素和地特胰岛素这两种长效胰岛素,但效果都比较差,血糖波动大,有低血糖发生。入院后我们首先让患者的饮食及运动量相对固定,并对患者的整个降糖治疗方案进行了调整,使用了近年新出的两个胰岛素,即短效的谷赖胰岛素和长效的德谷胰岛素,同时加用了口服降糖药物阿卡波糖。
与短效的赖脯胰岛素和门冬胰岛素含锌不一样,谷赖胰岛素不含有锌,因此谷赖胰岛素是以单体和二聚体的形式被吸收入血,吸收速度更快,发挥降糖作用也更快。所以与赖脯胰岛素和门冬胰岛素相比,谷赖胰岛素的吸收和起效都更快。这样谷赖胰岛素与进餐时生理性胰岛素的分泌模式更加相似。
再来看一下德谷胰岛素,当德谷胰岛素注射到皮下后,苯酚快速弥散,德谷胰岛素构象改变,双六聚体末端开放,结合另外一个双六聚体,形成可溶、稳定的多六聚体长链,随着时间延长,锌离子缓慢弥散,多六聚体长链的末端解离出德谷胰岛素单体,单体吸收入血后发挥平稳的降糖作用,因此德谷胰岛素的半衰期长达25小时,明显长于甘精胰岛素和地特胰岛素。
除了饮食量和运动量的相对固定、胰岛素类型的调整,另外一个比较关键的方案调整是增加了阿卡波糖,因为这个患者餐后血糖高,而餐前又容易发生低血糖,而阿卡波糖恰好可以延缓进餐后葡萄糖的吸收,从而可以降低患者的餐后高血糖,又避免了餐前低血糖。最终通过整个治疗方案的调整,患者血糖得到了较好的控制。
推荐阅读
来源:糖甲大院
查看更多