查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





原发性胆汁性胆管炎(PBC)、原发性硬化性胆管炎(PSC)和妊娠肝内胆汁淤积症(ICP)等肝胆疾病的患者常出现胆汁淤积性瘙痒症状,令患者无法忍受。由于胆汁淤积性瘙痒潜在的病理生理机制尚不清楚,其治疗效果仍不能令人满意。
2021年4月2日,Gastroenterology发表的一项研究表明,皮肤表面的角质细胞起“前神经元”的作用,而溶血卵磷脂(LPC)是诱发胆汁淤积性瘙痒的分子基础,为临床胆汁淤积性肝胆疾病伴随的瘙痒治疗带来新靶点。
首席研究员、杜克医学院神经学教授Liedtke认为,“皮肤细胞在某些条件下可感受外界刺激,特别是最外层的角质细胞。”
Liedtke教授一直致力于细胞表面钙离子通道的研究,20年前曾发现TRPV4通道。TRPV4通道存在于包括皮肤细胞在内的许多组织中,起着至关重要的作用,如痛觉反应。
Liedtke教授表示,“最初认为皮肤中TRPV4通道起着分层和屏障作用,但目前的研究显示,皮肤实际上还可作为感觉器官。”角质细胞接受瘙痒的化学信号并传递给皮肤中的神经末梢,该神经末梢属于近脊柱的背根神经节中的瘙痒感觉神经细胞。本研究的第一作者Chen与Liedtke教授合作,共同发现了皮肤TRPV4通道在慢性皮肤瘙痒中的作用。
研究显示,胆汁淤积性瘙痒与胆汁酸、胆红素、黄体酮代谢物和溶血磷脂酸(LPA)有关。LPA是一种具有多种生物功能的生物活性磷脂,自分泌素(ATX)催化溶血卵磷脂(LPC)水解为LPA。研究显示,ATX和LPA水平与胆汁淤积性肝病患者的瘙痒程度相关,LPA通过TRPV1和TRPA1引起瘙痒。TRP离子通道可能参与瘙痒的分子机制,受神经支配的上皮细胞和感觉神经元表达的TRPV4通道也可能与瘙痒相关。
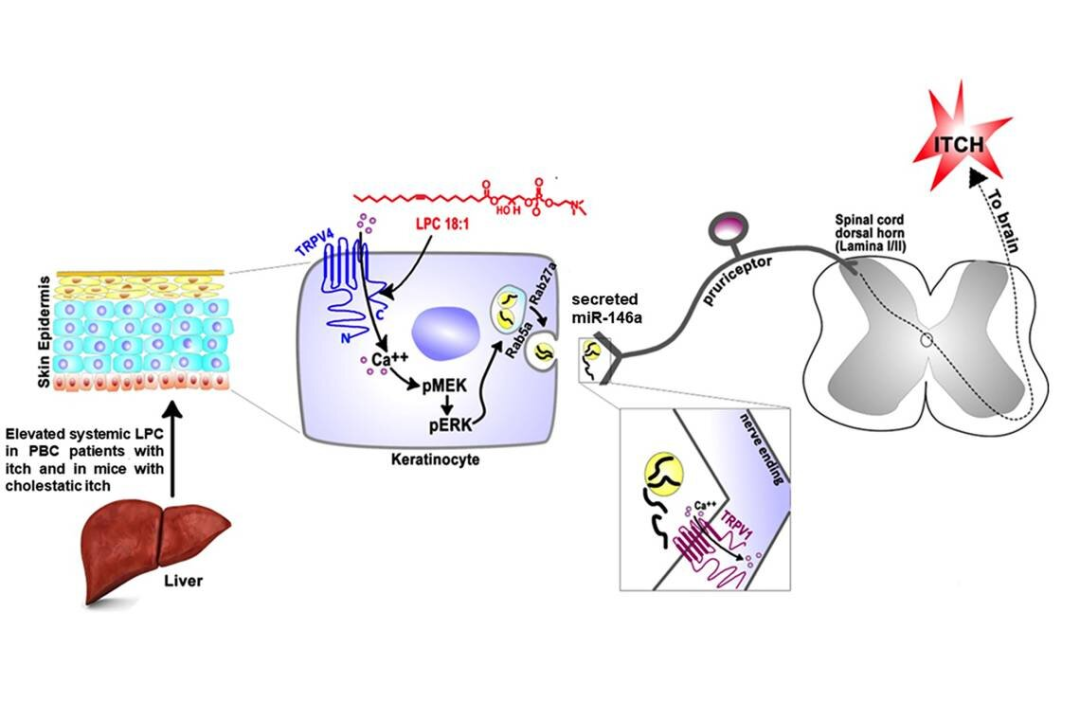
研究人员发现,原发性胆汁性胆管炎(PBC)患者血液中的一种磷酸化脂质或脂肪LPC过剩。动物实验表明,注射到小鼠和猴子皮肤中的LPC会引起瘙痒。那么,LPC如何导致强烈的瘙痒感?研究人员发现,当LPC到达皮肤时,可以直接与TRPV4通道结合,激活离子通道,钙离子通道开放。此时,研究人员追踪发现细胞内的信号级联反应,导致皮肤细胞表面形成一个叫作囊泡的微小气泡。囊泡可在细胞中生长并带走细胞里的物质。在这种情况下,小气泡里包含的微小RNA,起着信号分子的作用,微小RNA本身就是引发瘙痒的信号。研究人员确定的一种微小RNA分子是miR-146a,将miR-146a注射到小鼠和猴子体内,立即引起瘙痒,而不是几小时后,就像调节基因一样。
Chen表示,“除了TRPV1依赖性信号传递外,未来的研究重点是,哪些特定的瘙痒感觉神经元对miR-146a发生反应,及其深层机制。”通过搜集PBC患者的血液和瘙痒数据,研究人员发现血液miR-146a水平与瘙痒的严重程度一致,LPC的水平也与瘙痒的严重程度一致。
弄清楚从LPC过量到难以忍受的瘙痒所有信号通路,可为科学家找到晚期肝脏疾病的新型标志物提供一种新的方法。同时,研究指出了治疗瘙痒的新途径,一种是通过局部治疗攻击启动瘙痒的特定的微小RNA,使皮肤中的TRPV4通道脱敏,另外一种是靶向清除LPC。
文章首发自消化界公众号
查看更多