查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





作者:复旦大学附属华山医院神经内科血管组 徐非凡 董漪
2026年5月6—8日,第12届欧洲卒中组织大会(ESOC 2026)于荷兰马斯特里赫特召开。
来自中国首都医科大学附属北京世纪坛医院的李深教授团队开展了FOCUS研究,并在ESOC 2026上公布了研究结果。
低温疗法可通过抑制兴奋毒性、减轻炎症反应、减少氧化应激、保护血脑屏障完整性、降低脑能量代谢、减少细胞凋亡等多种病理生理机制参与卒中后神经保护。而传统的全身低温疗法存在诸多副作用,包括寒战、感染风险增加、药物清除率改变、高血糖、电解质紊乱、心血管系统影响(心输出量、心率、心脏电活动、血压变化)、尿量减少以及凝血功能障碍等,因此限制了其在急性缺血性卒中(AIS)患者中的应用[1]。
选择性动脉内低温灌注(SI-AC)是一种新型局部低温技术,通过血管内途径直接将冷生理盐水灌注至缺血区,实现靶向低温,从而避免全身低温的副作用。既往研究已初步证实SI-AC的安全性和可行性[2, 3],为其在AIS神经保护中的应用奠定了基础。
为进一步确定SI-AC在接受血管内取栓(EVT)的大血管闭塞性AIS(AIS-LVO)患者中的有效性和安全性,来自中国首都医科大学附属北京世纪坛医院的李深教授团队开展了FOCUS研究,并在ESOC 2026上公布了研究结果。
本研究是一项多中心、全国性、研究者发起并实施的随机、对照、受试者和评估者双盲的优效性临床试验。258例患者来自中国12个中心,采用分层区组随机化设计。
1. 纳入标准
年龄≥18岁且≤80岁
临床表现为前循环AIS-LVO,经CTA/MRA/DSA证实为颈内动脉颅内段(IICA)或大脑中动脉M1段(MCA-M1)闭塞
筛查时美国国立卫生研究院卒中量表(NIHSS)评分≥6且≤25分
卒中前改良Rankin量表(mRS)评分≤1分
距症状发作或最后已知正常(LKW)时间24 h内完成动脉穿刺
获得患者或法定授权代表的书面知情同意
发病6 h内入院的患者,要求Alberta卒中项目早期CT评分(ASPECTS)≥6分;6~24h内入院的患者,采用DAWN或DEFUSE-3研究的神经影像学标准(① DAWN研究影像学纳入标准:NIHSS≥10分,核心梗死体积<31 ml;NIHSS≥20分,核心梗死体积31~51 ml;② DEFUSE-3研究影像学纳入标准:核心梗死体积<70 ml,灌注不匹配体积比>1.8,且不匹配体积差>15 ml)。
2. 排除标准
基线CT/MRI显示多血管供血区急性梗死
CTA/MRA/DSA证实存在动脉夹层
取栓前已有颅内出血或出血转化
对抗板药、抗凝药、碘造影剂或麻醉剂过敏/不耐受
严重感染(如脓毒症)或多器官功能衰竭
遗传性或获得性出血倾向、凝血因子缺乏、近期口服抗凝治疗且国际标准化比值(INR)>3
例外:距末次使用新型口服抗凝药≥48 h且活化部分凝血活酶时间(APTT)正常
基线血小板计数<50×10⁹/L
血糖<50 mg/dl(2.7 mmol/l)或>400 mg/dl(22.2 mmol/l)
药物难以控制的难治性高血压(收缩压持续>185 mmHg或舒张压持续>110 mmHg)
NYHA心功能分级>Ⅰ级
冠状动脉狭窄>70%或冠状动脉搭桥手术史
正在进行血液透析或腹膜透析;严重肾功能不全:肾小球滤过率<30 ml/min或血肌酐>220 mmol/l(2.5 mg/dl)
已知颅内动脉瘤或脑动静脉畸形
恶性脑肿瘤或中枢神经系统感染
可能影响神经功能评估的既往神经系统或精神疾病(如痴呆或精神疾病)
妊娠或哺乳期
预期寿命<6个月
正在参加其他药物或器械研究
因任何其他原因,主管临床医师认为患者不适合接受SI-AC
3. 主要终点
90±7 d mRS评分分布
4. 次要终点
90 d mRS 0~2的比例、90 d mRS 0~1的比例、7 d NIHSS评分、90 d Barthel指数(BI)、7 d最终梗死体积、24 h神经功能快速改善程度、鼓膜温度变化。
5. 安全性终点
症状性颅内出血(sICH)、颅内出血(ICH)、手术相关并发症、感染、凝血异常、电解质紊乱、直肠温度变化。
本研究纳入发病24 h内、经CTA/MRA/DSA证实为IICA或MCA-M1闭塞的AIS患者,按1:1比例随机分配至SI-AC组和对照组,在基线、24±12 h、48±12 h、第7±2 d/出院、第30±3 d、第90±7d时进行随访评估。
SI-AC组: SI-AC+EVT+最佳药物治疗(BMM)
对照组: EVT+BMM(即当前临床实践标准治疗)

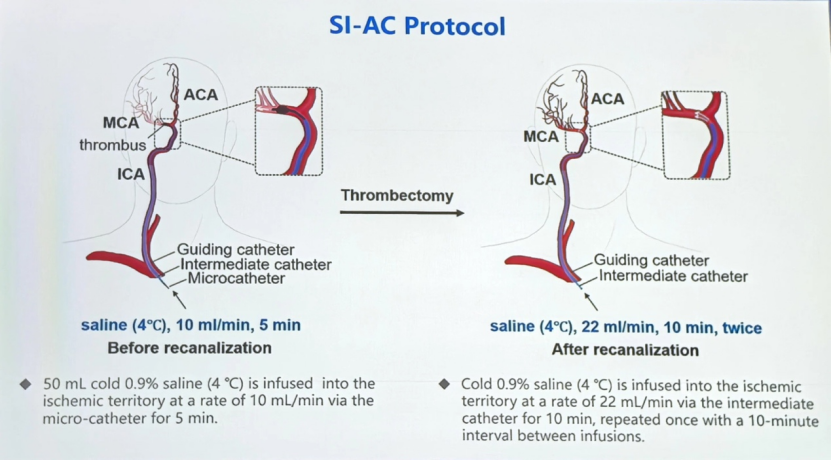
SI-AC分两阶段:
① 再通前:通过微导管以10 ml/min的速度向缺血区输注50 ml 4°C的0.9%冷生理盐水,持续5 min。
② 再通后:通过中间导管以22 ml/min的速度向缺血区输注4°C的0.9%冷生理盐水,持续10 min;间隔10 min后,重复输注一次。
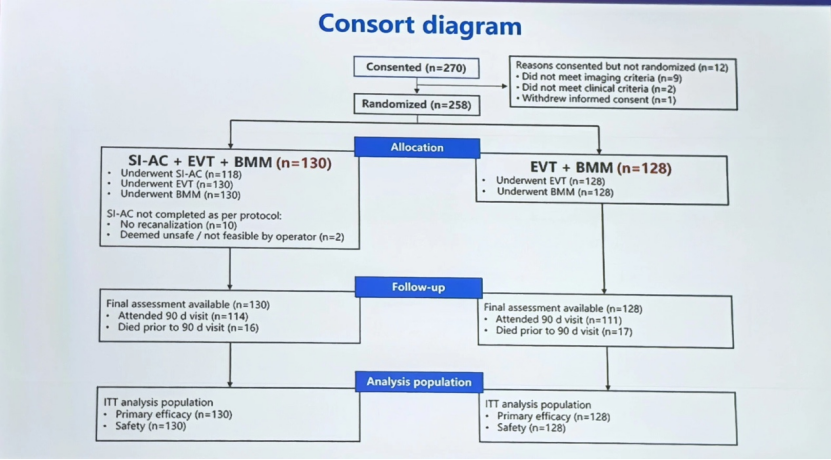
本研究共筛选270例患者,排除12例(9例不符合影像学标准、2例不符合临床标准、1例撤回知情同意),最终纳入258例,其中SI-AC组130例(包括12例未按方案完成SI-AC:10例未再通、2例术者认为不安全/不可行),对照组128例,进入意向性治疗(ITT)分析。
所有患者均完成最终评估,33例患者在90 d访视前死亡(SI-AC组16例,对照组17例),其余患者均完成90 d随访。
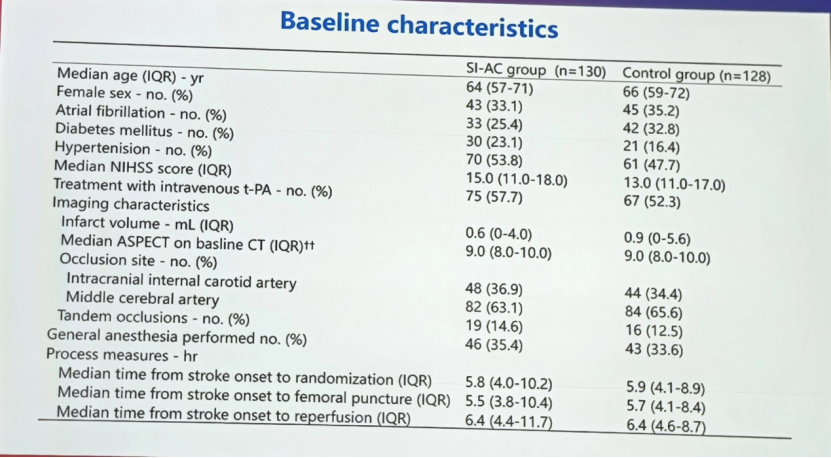
两组间的基线信息如下图所示,在人口学特征、血管危险因素、卒中严重程度、影像学特征、治疗时间窗等方面均具有良好的可比性。
两组间的90 d mRS评分分布无统计学差异。
未校正共同比值比(Common OR)1.15,95%CI 0.75~1.77,P=0.52;校正年龄、NIHSS、房颤、发病至随机时间后的OR为1.16,95%CI 0.75~1.79,P=0.51。
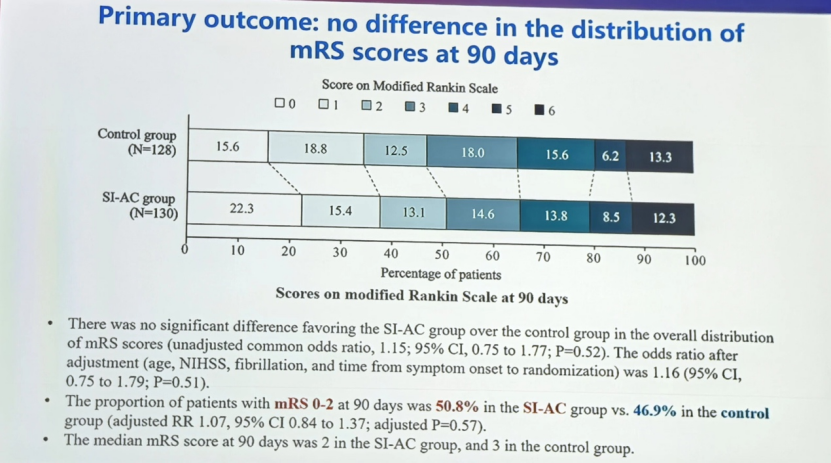
SI-AC组90 d mRS 0~2比例高于对照组(50.8% vs. 46.9%),但未达到统计学差异(校正后P=0.57)。
SI-AC组90 d中位mRS为2分,对照组为3分。
SI-AC组的24 h ICH发生率显著低于对照组(26.9% vs 45.3%),绝对风险差异达-18.4%,具有统计学意义(校正后P=0.003)。
在sICH、手术并发症、感染、凝血异常、电解质紊乱、90 d死亡率方面,两组间无显著差异。
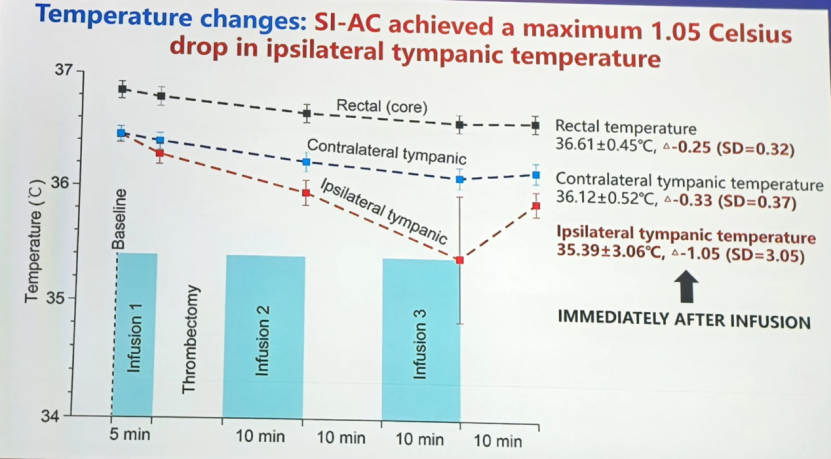
值得注意的是,SI-AC组的患者在输注完成后,同侧鼓膜温度下降1.05°C,而直肠温度和对侧鼓膜温度仅略微下降,体现了其选择性的局部低温效应,从而避免了全身低温的副作用。
综上,与标准取栓相比,SI-AC作为EVT的辅助治疗并未改善90 d功能预后,但可降低ICH发生率,可能提示其对血脑屏障的保护作用。由于出血转化是影响AIS预后的重要因素,这一安全性获益具有潜在的临床意义。
当然,本研究的样本量可能不足以检测出功能预后差异,因此未来仍需更大样本量的研究或更精细的患者选择策略,以充分发掘低温治疗的神经保护潜力。此外,一种将患者血液抽出、体外冷却并氧合血液回输的新技术,或能克服生理盐水灌注的局限性,为AIS的神经保护治疗开辟新途径,让我们拭目以待!
[1] WU L, WU D, YANG T, et al. Hypothermic neuroprotection against acute ischemic stroke: The 2019 update [J]. J Cereb Blood Flow Metab, 2020, 40(3): 461-81.
[2] WU C, ZHAO W, AN H, et al. Safety, feasibility, and potential efficacy of intraarterial selective cooling infusion for stroke patients treated with mechanical thrombectomy [J]. J Cereb Blood Flow Metab, 2018, 38(12): 2251-60.
[3] HUANG Z X, HU M, ZHANG P, et al. Intra-arterial selective hypothermia for acute ischemic stroke neuroprotection: A multicenter pilot trial in China [J]. PLoS Med, 2025, 22(7): e1004668.

查看更多