查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





第56届美国临床肿瘤学会(ASCO)年会线上首秀圆满落幕,肺癌领域继续领跑,多项前沿进展闪耀ASCO舞台,免疫治疗继续前行,在非小细胞肺癌(NSCLC)领域颇多建树。本报特邀吉林省肿瘤医院程颖教授,梳理NSCLC领域免疫治疗进展,指导临床实践,展望未来方向。
程颖 教授
二级教授,博士研究生导师,博士后工作站导师
享受国务院特殊津贴,卫生部突出贡献中青年专家
吉林省肿瘤医院党委书记
吉林省癌症中心主任
吉林省肺癌诊疗中心主任
中国临床肿瘤学会(CSCO) 副理事长
CSCO小细胞肺癌专业委员会主任委员
CSCO临床研究专家委员会候任主任委员
CSCO非小细胞肺癌专业委员会副主任委员
CSCO肝癌专家委员会副主任委员
CSCO肿瘤大数据专家委员会副主任委员
中国抗癌协会肺癌专业委员会副主任委员
中国抗癌协会肿瘤临床化疗专业委员会副主任委员
中华医学会肿瘤学分会委员
全国医师定期考核肿瘤专业编辑专业委员会副主任委员
国家卫生、计生委常见肿瘤规范化诊疗专家组成员
中国医师协会肺癌培训专业委员会副主任委员
吉林省医师协会肿瘤医师分会主任委员
吉林省医学会肿瘤专业委员会主任委员
担任《中华肿瘤杂志》等多家杂志编委
程颖教授:今年ASCO年会免疫治疗仍然是最炙手可热的研究领域,在NSCLC免疫治疗也有几项重磅的研究结果公布。KEYNOTE-189研究更新了最终结果,帕博利珠单抗联合化疗组与安慰剂联合化疗组中位总生存(OS)分别为22.0个月和10.6个月(HR 0.56,95% CI 0.46-0.69),中位无进展生存(PFS)分别为9.0个月和4.9个月(HR 0.49,95% CI 0.41-0.59),该结果进一步巩固了帕博利珠单抗联合化疗作为转移性非鳞NSCLC患者标准一线治疗的地位。
双免疫联合治疗成为了今年NSCLC一线治疗的新贵,从CheckMate 227研究看到与化疗相比,无论PD-L1表达如何都可以从双免疫一线治疗中获得OS的长期获益 [3年的OS率:双免疫和化疗分别为33%和22% (PD-L1≥1%);34% 和15% (PD-L1<1%)]。今年5月美国食品药物管理局(FDA)也批准了纳武利尤单抗联合ipilimumab一线治疗PD-L1≥1%且EGFR及ALK基因阴性晚期NSCLC患者的适应证,为晚期NSCLC一线免疫“去化疗”方案提供一种新的选择。
CheckMate 9LA研究是今年ASCO上又一项重要研究,该研究通过双免疫联合短程化疗的设计有效克服了免疫治疗起效缓慢的不足。与化疗相比,双免疫联合短程化疗获得显著的OS改善(15.6个月对10.9个月,HR 0.66,95% CI 0.55-0.80),并且两条生存曲线在最初阶段就开始分离,使免疫治疗的优势早期显现。安全性方面,双免疫联合化疗在一定程度上增加了不良事件的发生率,但是并没有新的预料之外的毒性发生,患者的耐受良好。基于CheckMate 9LA研究结果,今年5月FDA也批准了纳武利尤单抗联合ipilimumab及短疗程化疗一线治疗无驱动基因突变晚期NSCLC的适应证,为免疫联合治疗策略增添了一种新的选择。
免疫治疗与新型免疫靶点药物的联合显示了巨大的潜力,TIGIT为免疫抑制性检查点受体,与癌细胞上高表达的CD155结合,可以抑制细胞毒性T细胞和NK细胞介导的肿瘤杀伤作用,同时抑制TIGIT及PD-1受体能够协同免疫细胞杀伤肿瘤,增强抗肿瘤免疫应答。今年ASCO年会报道了一项Ⅱ期研究,评估TIGIT抗体tiragolumab联合阿替利珠单抗对比单药阿替利珠单抗一线治疗NSCLC的疗效,该研究共入组135例受试者,结果显示tiragolumab联合阿替利珠单抗治疗组的客观有效率(ORR)为31.3%,阿替利珠单抗单药治疗的ORR为16.2%,两组PFS分别为5.4个月和3.6个月。在PD-L1高表达的患者中,联合治疗组的ORR为55.2%,单药阿替利珠单抗的ORR为17.2%。安全性方面,联合治疗组也显示了较好的耐受性,两组3级以上不良事件的发生率相似。该研究提示TIGIT抗体tiragolumab联合阿替利珠单抗能够提高ORR和PFS,未来需要Ⅲ期研究进一步验证。
程颖教授:随着新的研究结果的公布,NSCLC免疫一线治疗呈现多种治疗选择,包括免疫单药治疗、免疫联合化疗、双免疫治疗以及双免疫联合化疗等策略。在众多的治疗模式中,对于PD-L1高表达(PD-L1≥50%)患者,根据KEYNOTE-024研究结果,免疫单药成为了有效而且低毒的治疗选择,虽然KEYNOTE-042研究结果证实PD-L1表达阳性的患者都能从帕博利珠单抗单药治疗中获益,然而我们也看化疗与免疫单药的OS曲线存在交叉,提示需要通过联合策略使患者尽快从免疫治疗中获益。而基于KEYNOTE-189和KEYNOTE-407研究,免疫联合化疗显著改善了晚期NSCLC患者的生存状态,且不用考虑PD-L1的表达情况。免疫联合化疗提高了疗效,扩大了获益人群,新的联合治疗方式也在不断探索,CheckMate 227研究结果的陆续公布,证实了在PD-L1≥1%人群中获益显著,在PD-L1<1%的人群中也有获益趋势,但未纳入统计分析,仅为描述性结果,双免疫去化疗的方案获得了相似的3年OS,为“去化疗”方案提供了一种新的选择。虽然CheckMate 227研究证实纳武利尤单抗联合ipilimumab改善了晚期NSCLC患者的中位OS,但是两条生存曲线存在交叉现象,提示双免疫联合治疗存在着早期进展和死亡的患者。CheckMate 9LA研究在双免疫联合治疗的基础上加上短疗程的化疗,能够快速的控制症状、减轻肿瘤负荷,鳞癌或者非鳞癌的患者,无论PD-L1表达情况都能够获得生存的改善。需要注意的是:CheckMate 9LA研究的ORR为38%,CheckMate 227的ORR为36.4%,提示在免疫联合化疗基础上加入ipilimumab似乎需要对有效人群进行选择。
目前FDA批准NSCLC一线治疗方案的疗效和安全性数据
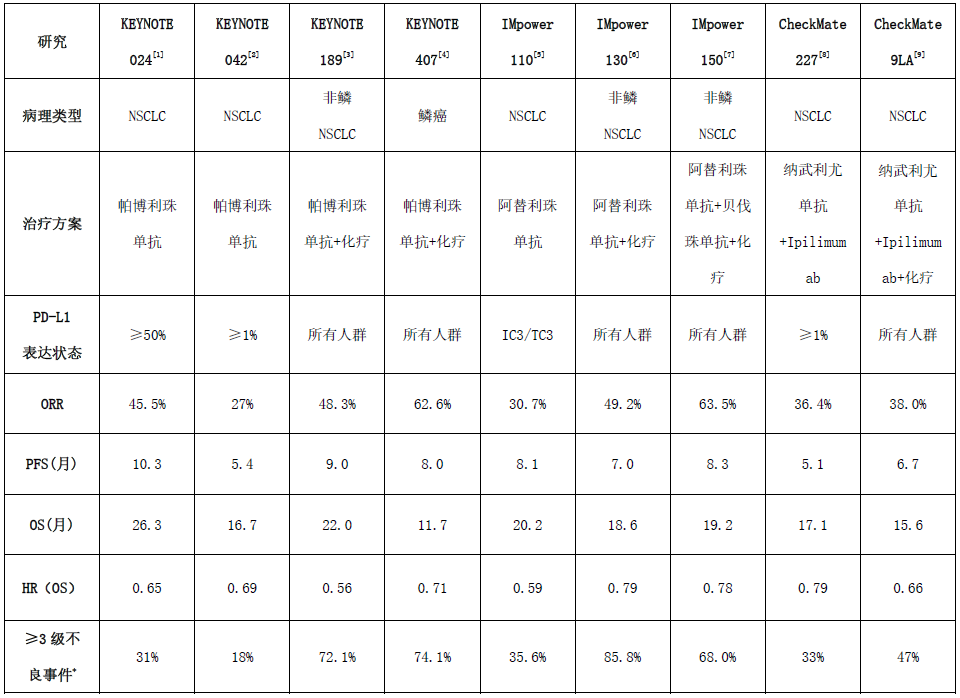
*注:≥3级AE事件中,KEYNOTE -189,KEYNOTE - 407,IMpower110,IMpower130为全因AE(All cause AE);KEYNOTE-024,KEYNOTE-042,IMpower150,CheckMate227,CheckMate9LA研究为治疗相关的AE(TRAE)。
程颖教授:目前,晚期NSCLC一线免疫治疗模式选择众多,临床实践中如何选择合适的免疫治疗模式值得关注。首先,我们要选择免疫治疗的适合人群,了解肿瘤PD - L1的表达及肿瘤突变负荷(TMB)状态等;第二,我们要关注不同治疗策略疗效的差异,包括免疫治疗的近期疗效和远期疗效评价,让肿瘤能够快速缓解的同时达到长期生存;第三,要结合患者身体的耐受情况,重视免疫联合治疗带来的毒副反应以及对患者生活质量的影响;此外,药物可及性以及经济效价比也是选择治疗策略的重要参考因素。
随着免疫治疗适应证逐渐扩大,临床应用人群越来越多,免疫治疗带来的不良反应需要引起重视。免疫相关性不良事件发生率低,通常程度较轻,常见的免疫相关性不良事件有皮肤病、内分泌性疾病、结肠炎、肺炎、肝炎等,但偶尔也会出现一些罕见但是致命性的不良事件,如胰腺炎、心肌炎、免疫相关性神经系统疾病等。对不良事件的识别和处理需要多学科共同协作,做好全程监控和管理,根据不良事件的严重程度采取相应的处理措施。对于轻度的不良事件一般无需特殊处理,注意监控和随访观察;中重度的不良事件,应及时应用皮质类固醇激素,症状消退至1级时激素可逐渐减量,对于激素治疗无效的患者应考虑应用免疫抑制剂英夫利昔单抗治疗。
程颖教授:免疫治疗推动NSCLC进入了一个全新的时代,在取得举世瞩目成就的同时,未来仍有很多领域值得进一步探索。生物标志物的探索一直是免疫治疗研究的热点,在NSCLC免疫一线治疗的研究中已经证实免疫单药疗效与PD-L1表达的相关性,在免疫联合治疗和免疫后线治疗中发现,无论PD-L1表达如何都能从中获益。随着今年6月帕博利珠单抗基于KEYNOTE-158研究获批用于肿瘤突变负荷高表达泛癌种的治疗以来,TMB作为另一个重要的免疫标志物再次备受关注,在CheckMate 568,CheckMate 227研究中也发现高TMB患者双免疫治疗获益,然而在KEYNOTE - 189探索性研究中并没有发现TMB与免疫联合化疗疗效的相关性。
除了PD-L1和TMB,肿瘤微环境中肿瘤浸润淋巴细胞(TIL)的密度、表型和多样性、免疫抑制的生物标志物(如LAG - 3、Tregs、MDSCs等)、肿瘤基因组特征(正向基因:KRAS、P53、DDR、PBRM1;负向基因:EGFR、ALK、STK11、PTEN、B2M、JAK1/2)、患者胚系遗传因素(如HLA - I类多样性、HLA-I类等位基因LOH等)、新抗原克隆性、T细胞炎性微环境和宿主肠道微生物等众多生物标志物与NSCLC免疫治疗疗效的相关性也正在探索中。
治疗模式的优化是另一个重要的探索方向,除了目前的双免疫,免疫联合化疗,双免疫联合短程化疗,免疫联合抗血管治疗等模式外,新型免疫靶点也正在探索,包括作用于免疫检查点共抑制性受体(LAG3,TIM3,BTLA、TIGIT等)、协同刺激分子(CD137、OX40、CD40、GITR等)、肿瘤微环境中的免疫细胞(MDSCs、Tregs)的新型免疫药物,双克隆抗体、CAR-T疗法、抗体偶联药物、细胞因子以及癌症疫苗等研究也在如火如荼开展中,未来新型免疫疗法将进一步助力免疫治疗在NSCLC领域的发展。
在免疫治疗打破了晚期NSCLC的治疗格局、并在局晚期NSCLC中大获成功之后,免疫治疗正在向早期肺癌进军,几项II期临床研究已经显示免疫新辅助治疗在早期肺癌中展现了初步的疗效和安全性,免疫联合化疗新辅助治疗的Ⅲ期临床研究(CheckMate 816、KEYNOTE-671、IMpower030和AEGEAN)目前正在入组阶段,除了新辅助免疫治疗,免疫辅助治疗几项III期研究(PEARLS、ANViL、IMpower010、BR31、KEYNOTE-091)也正在进行中,未来这些研究结果的公布有可能再次改变早期肺癌患者的临床实践,让免疫治疗在NSCLC领域真正实现全人群的覆盖。
本资讯由默沙东医学团队编辑提供,旨在用于医学专业人士间的学术交流,请勿随意转发或转载。文中相关内容不能以任何方式取代专业的医疗指导,也不应被视为治疗建议。医学专业人士对文中提到的任何药品进行处方时,请严格遵循该药品在中国批准使用的说明书。默沙东不承担相应的有关责任。
审批编号:MI-PD1-0445-CN
过期日期:2021-2-2
查看更多