查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





基本资料
性别:女
年龄:43
主诉:降结肠癌术后3年,右卵巢、多发淋巴结转移1周
伴随症状:(-)
既往史:2012/01/15 左半结肠根治术,术后病理:中分化腺癌,脉管/神经束:(-),LN(+) : 0/15,术后分期 :pT3N0M0,IIA,pMMR
伴随疾病:慢乙肝肝硬化,因脾亢行脾切除术,定期监测HBV DNA(-)
家族史:母亲患“结肠癌”去世。
辅助检查
查体:ECOG PS 1分,左锁上LN(+)。
影像学检查:
(2015/11/07我院胸腹盆CT):结肠癌术后 右卵巢转移;左锁上、下腔静脉旁、腹主动脉旁、左髂总血管旁淋巴结转移。
病理诊断:(2015/11/11左锁上LN穿刺)病理 腺癌,结合IHC, 考虑肠来源。
分子诊断: RAS/BRAF基因野生型
无化疗禁忌症:血常规、肝肾功能、HBV DNA、心电图(-)
诊断:
1.降结肠中分化腺癌术后(pT3N0M0,IIA)右卵巢、多发淋巴结转移,pMMR,RAS/BRAF野生型
2.慢性乙型病毒性肝炎肝硬化 脾切除术后
基线CT:
治疗前CT2015-10-21
靶病灶:
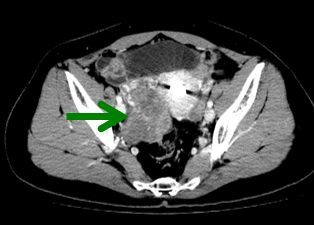
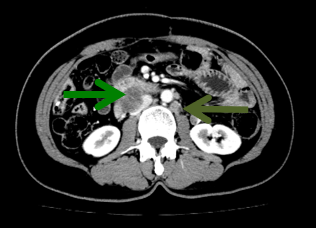
非靶病灶:
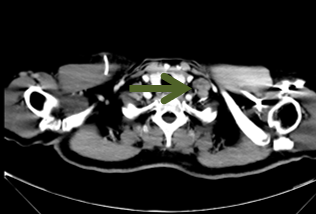
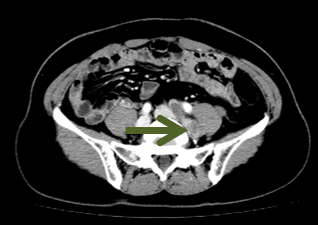
治疗方案:
一线治疗:
PS 1;异时性转移;未行辅助化疗;不可切除 ;左半 ;pMMR ;RAS/BRAF(-);经济一般。
Folfox+Bev



一线化疗:
一线化疗方案:Folfox+Bevacirumab
疗程:9
疗程起止日期:2015/11/14 ~2016/03/29
疗程时间;4.5m
最佳疗效:SD
不良反应:II°粒细胞减少;III°外周神经毒性
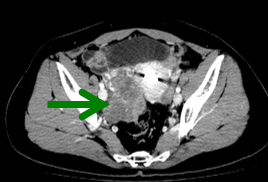
基线
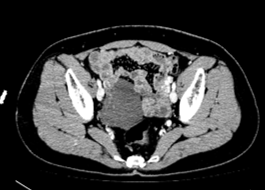
4程后 SD
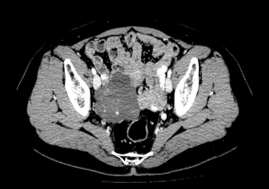
8程后 SD
一线维持化疗:
一线维持方案:Capecitabine
疗程:6
治疗起止日期:2016/04/18~2016/08/05
治疗时间:3.5m
最佳疗效:SD
不良反应:I°粒细胞减少
PD时间:2016/08/29
一线PFS:9.5m
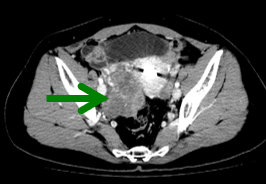
基线
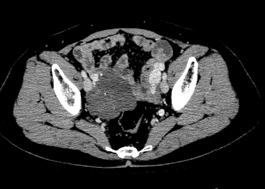
3程后 SD
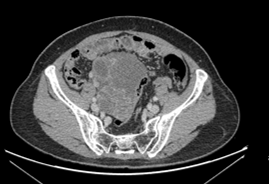
6程后 PD
二线化疗:
二线治疗方案:FOLFIRI
疗程:12
疗程起止时间:2016/09/13~2016/04/01
治疗时间:6.6m
最佳疗效:SD
不良反应:III°粒细胞减少
PD时间:2017/07/14
二线PFS:10m
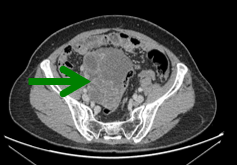
基线
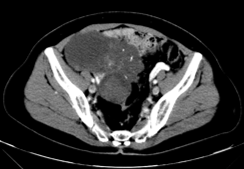
4程后 SD
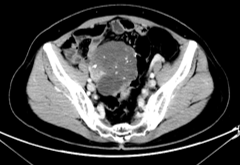
8程后 SD
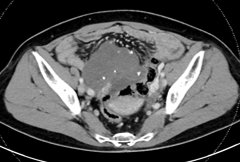
12程后 SD
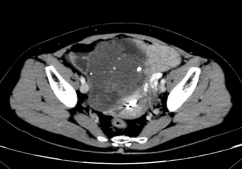
化疗后3月随访 PD
mCRC后线治疗
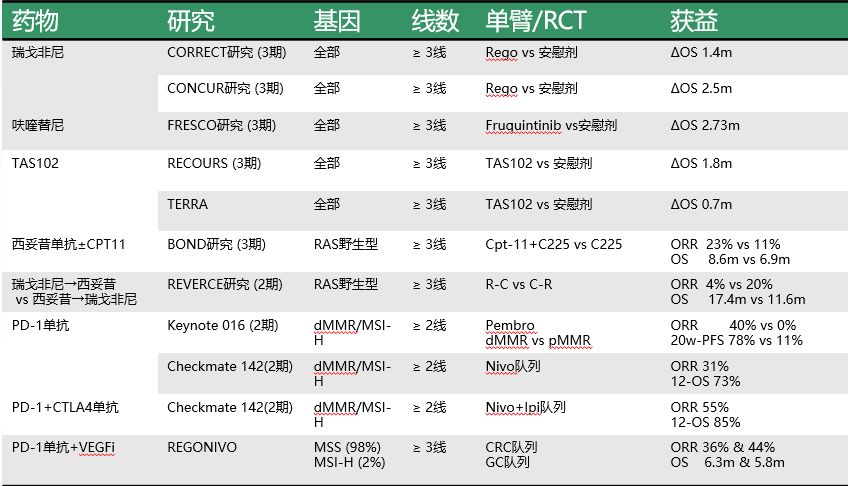
西妥昔单抗 (C225)+/- 伊立替康 (CPT-11)
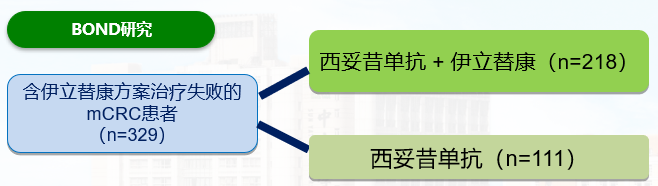
79.4%的患者接受过2线以上治疗
主要研究终点: ORR
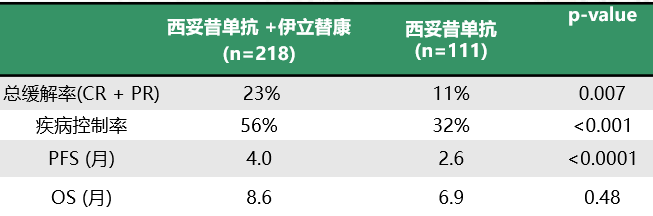
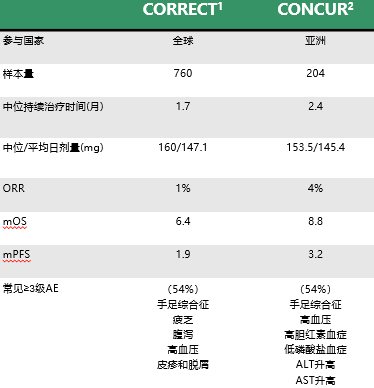
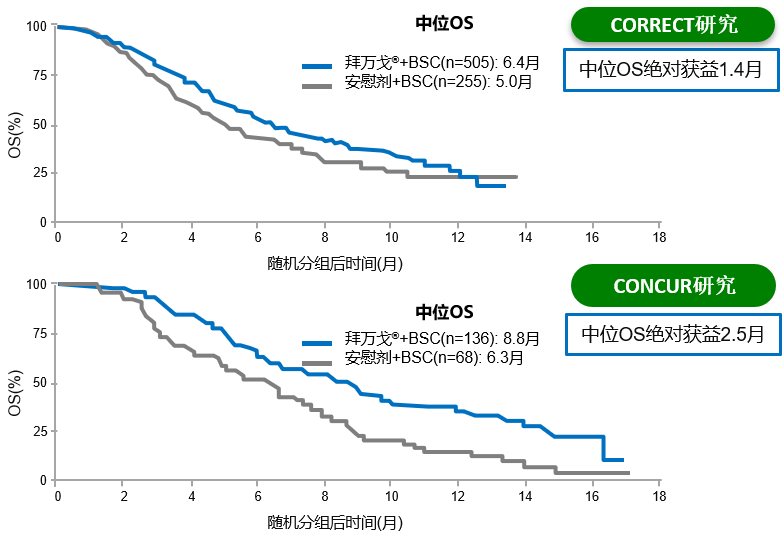
瑞戈非尼III期:CORRECT&CONCUR
CORRECT研究:一项全球性研究,涉及国家包括澳大利亚、比利时、加拿大、中国、捷克共和国、
法国、德国、匈牙利、以色列、意大利、日本、荷兰、西班牙、瑞士、土耳其和美国。
纳入760例mCRC患者:
既往接受标准治疗:氟尿嘧啶、奥沙利铂、伊立替康、贝伐单抗和西妥昔单抗或帕尼单抗(如果为KRAS野生型)。
瑞戈非尼 :口服,160 mg /天,(服用3周,停用1周)+ 最佳支持治疗。
安慰剂:(服用3周,停用1周) + 最佳支持治疗。
主要终点:总体生存期。
次要终点:无进展生存期,客观缓解率,疾病控制率和安全性。
第三终点:疾病缓解/稳定持续时间,生活质量(QOL), PK, 生物标志物。
CONCUR研究:一项亚洲的临床试验,涉及国家及地区包括中国、香港、韩国、台湾及越南。
纳入200例mCRC患者:既往接受标准治疗:氟尿嘧啶、奥沙利铂、伊立替康、贝伐单抗和西妥昔单抗,或帕尼单抗(如果为KRAS野生型)。
瑞戈非尼 :口服,160 mg /天,(服用3周,停用1周)+ 最佳支持治疗。
安慰剂:(服用3周,停用1周) + 最佳支持治疗。
主要终点:总体生存期。
次要终点:无进展生存期,客观缓解率,疾病控制率和安全性。
第三终点:疾病缓解/稳定持续时间,QOL,PK,生物标志物。

瑞戈非尼是首个治疗mCRC的多靶点多激酶抑制剂,可以通过抑制RET、VEGFR1、VEGFR2、VEGFR3、KIT、PDGFR-α、PDGFR-β、FGFR1、FGFR2、TIE2、DDR2、TrkA等的活性,而抑制肿瘤细胞增殖、肿瘤转移、肿瘤血管新生及肿瘤免疫逃逸相关靶点,从而发挥多重抗肿瘤作用。
亚组分析显示,在ECOG PS 0/1,既往单纯化疗,既往治疗线数 < 3,首诊M~随机前 < 18m,HFS的人群效果更好。
ReDOS研究: 低剂量 vs 标准剂量。
一项研究低剂量或标准剂量瑞戈非尼治疗耐药的mCRC患者的II期随机, 开放, 多中心试验。
患者接受预防性或反应性丙酸氯倍他索治疗。
丙酸氯倍他索是类固醇药膏, 常用于治疗各种皮肤问题和有助于防止在患者接受瑞戈非尼治疗时的手足皮肤反应(掌足红肿综合征, PPES)。
n=120
年龄≥18岁;组织学或细胞学证实为结直肠腺癌;接受标准治疗后进展, 无法根治的晚期或转移性CRC ECOG PS 0-1
对以上120人进行随机分组,
ARM A1: 低剂量a瑞戈非尼, 预防性使用丙酸氯倍他索;
ARM A2: 低剂量a瑞戈非尼, 反应性使用丙酸氯倍他索;
ARM B1: 标准剂量b瑞戈非尼, 预防性使用丙酸氯倍他索;
ARM B2: 标准剂量b瑞戈非尼, 反应性使用丙酸氯倍他索。
主要终点:有意向开始第3周期治疗的患者比例(未见疾病进展)
次要终点: OS ;PFS;TTP;前2周期中患者接受的瑞戈非尼总剂量 ;发生3/4级HFS或疲劳的总患者数及每组比例 ;QoL改变 ;PK。
2015年3月纳入第一例患者, 主要结果的最终数据收集时间: 2018年2月。
a.低剂量:80mg 1w, 120mg 1w, 160mg 1w, off 1w(依据药物相关毒性反应情况决定是否每周爬坡);
b.标准剂量:160mg 3w,off 1w。
预防性使用丙酸氯倍他索: 服药第1天开始预防性外用丙酸氯倍他索, 2次/天*12周。
反应性使用丙酸氯倍他索: 从第1天发生≥1级的HFSR开始外用丙酸氯倍他索, 2次/天。
瑞戈非尼低剂量组:
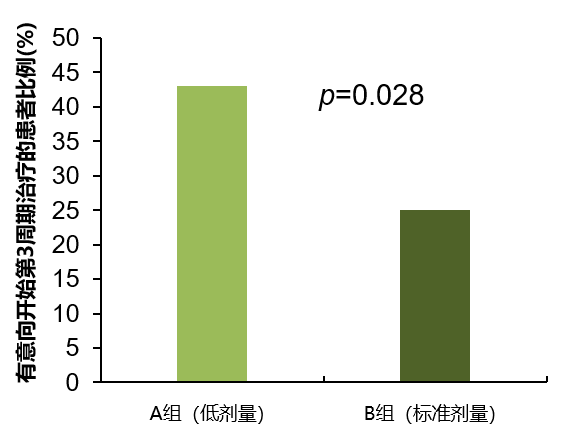
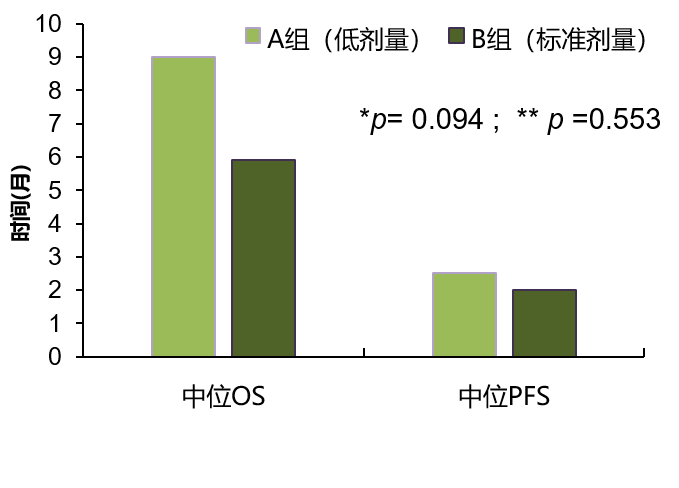
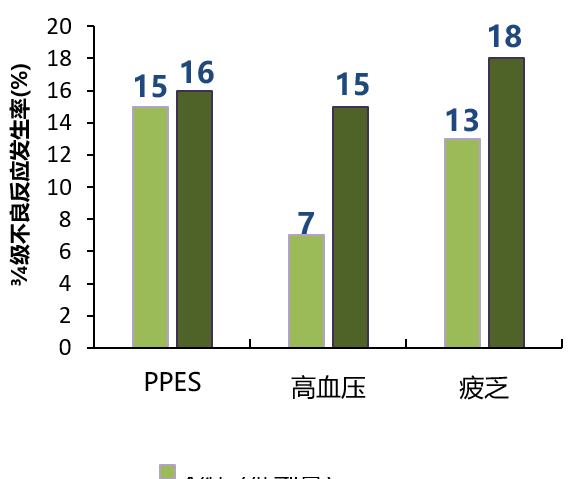
有意向开始第3周期治疗的患者比例明显更多;
中位OS更优;
中位PFS无统计学差异;
3/4级毒性反应稍低。
亚洲人群-瑞戈非尼剂量调整II期研究:
背景: CORRECT研究显示瑞戈非尼可显著改善标准治疗后进展的mCRC患者的总生存期(OS). 160mg/d是瑞戈非尼的标准起始剂量, 但部分病例因不良事件(AE)需下调剂量至120mg/d或更低,这在日本人群进行的研究中更常发生(84.6% vs 51.3%) 。
研究目的: 旨在通过剂量滴定研究瑞戈非尼的有效性和安全性。
患者(n=60)
纳入60例无法手术切除,标准化疗失败的mCRC患者(RAS突变型/野生型) PS 0-1。
瑞戈非尼起始剂量: 120mg / d*21天, 随后停用7天。
瑞戈非尼: 120mg / d*21天, 随后停用7天或者选择瑞戈非尼: 160mg / d*21天, 随后停用7天。
疾病进展/不可预测的毒副反应
单臂多中心II期研究, 2015年9月10日至2017年3月7日期间, 共入选60例患者, 中位年龄为68.5(范围: 30-84), ECOG PS 0/1为70%/ 30%. 患者每8周接受影像学评估。
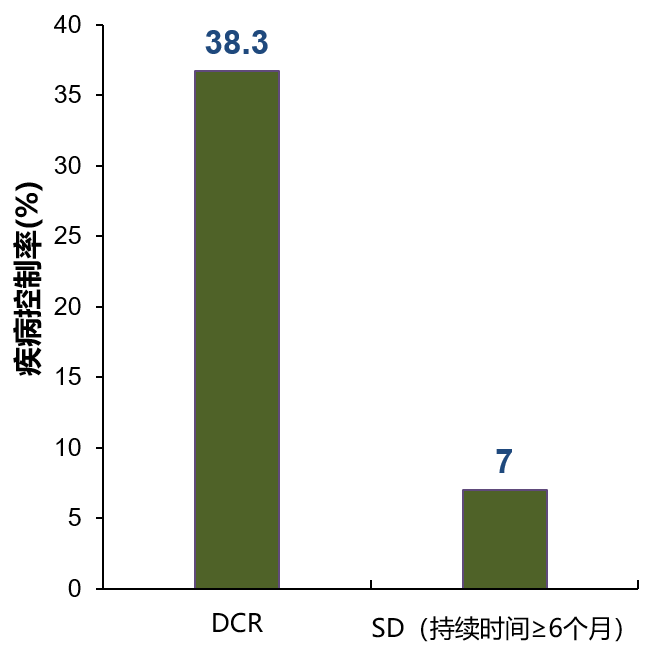
主要终点: 疾病控制率(DCR: CR + PR + SD≥6周)
主要的次要终点: 无进展生存(PFS), OS和安全性。
瑞戈非尼起始剂量120mg/d:
3.3%(2/60)的患者按规定剂量递增至160mg;
40%(24/60)因AE降低剂量至80mg;
DCR为38.3%(23/60) ,7%(4/60)的患者疾病稳定(SD)持续≥6个月;
中位PFS: 2.5个月(95%CI: 1.9 – 3.7);
52%(31/60)的患者发生3-4级AE。
呋喹替尼:
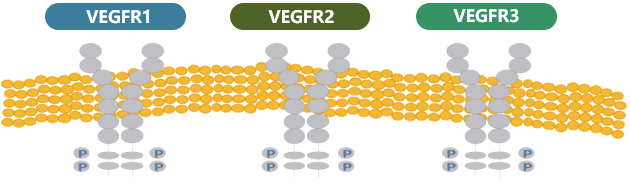
呋喹替尼 (爱优特®) 是具有高度选择性的肿瘤血管生成抑制剂,其主要作用靶点是VEGFR激酶家族VEGFR1,2,3,可抑制肿瘤血管生成,从而抑制肿瘤生长
FRESCO研究
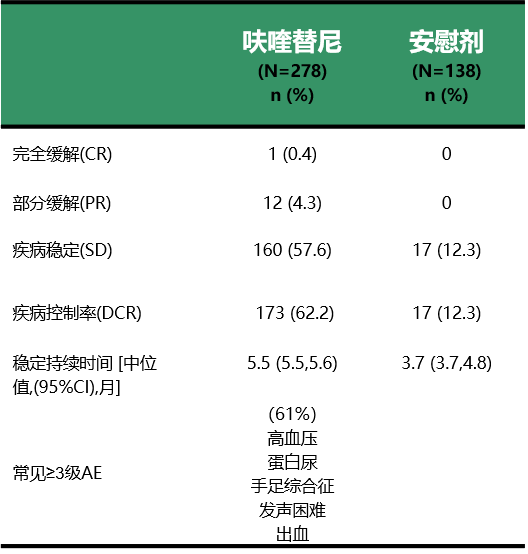
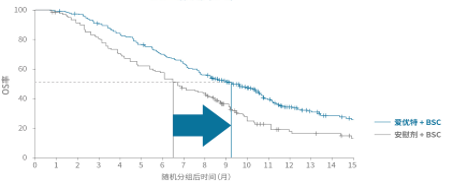
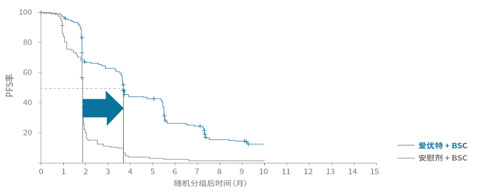
后线治疗顺序:瑞戈非尼 vs西妥昔单抗
REVERCE研究:
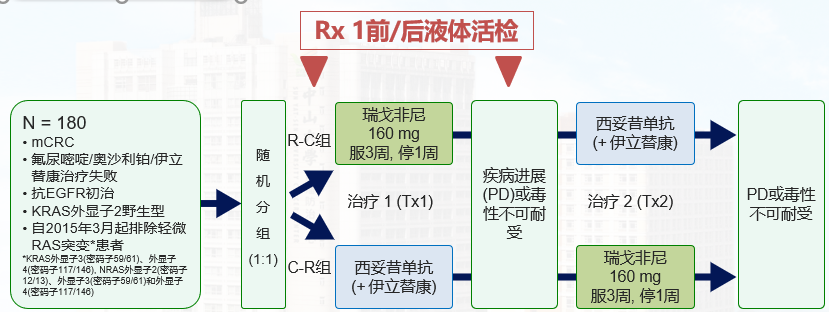
按入组时意向使用伊立替康、既往贝伐珠单抗治疗史和机构进行分层
主要终点: OS
80%以上的概率两组相似[HR 0.8-1.25, 对照组(C-R组)的预期中位OS为12个月], 需180例受试者以观察132例事件
次要终点: TTF, PFS, ORR, DCR, 不良反应, QOL (治疗前, Tx1和2治疗4周和8周时)
探索性终点: 液体标志物分析, 包括来自ctDNA或血清蛋白的与EGF/VEGF通路相关的癌基因突变
101例患者随机分组, 其中98例收集血浆及血清样本
因招募缓慢于2016年9月中止入组
2013年11月-2016年9月期间来自29个研究中心的共计101例患者接受随机分组 •最终分析(81例事件)的数据截止日期是2017年8月。
R-C方案对比C-R显著延长OS

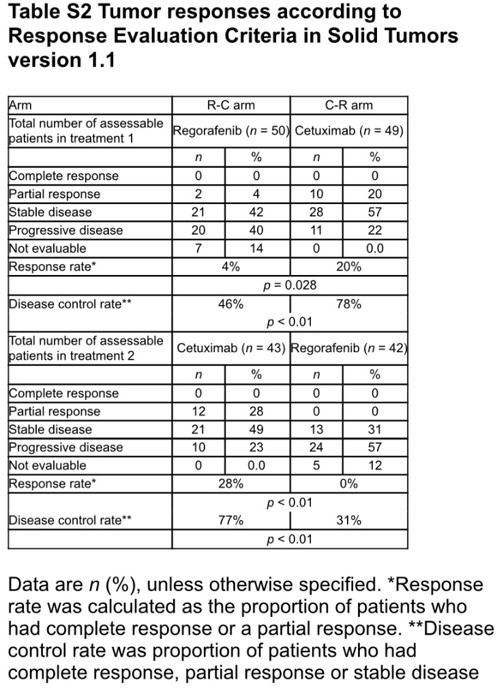
REVERCE研究主要终点:
贝伐珠单抗进展后R-C组患者中位OS为17.4个月,较C-R组患者中位OS的11.6个月,绝对获益为5.8个月,降低死亡风险39%,P值为0.029。由此可见,贝伐珠单抗进展后R-C组显著延长mCRC患者生存获益。
R-C方案瑞戈非尼治疗后对患者基因突变状态无影响。
使用拜万戈的持续抗血管治疗不影响基因状态,可能是R-C方案中位OS延长6个月的主要原因。
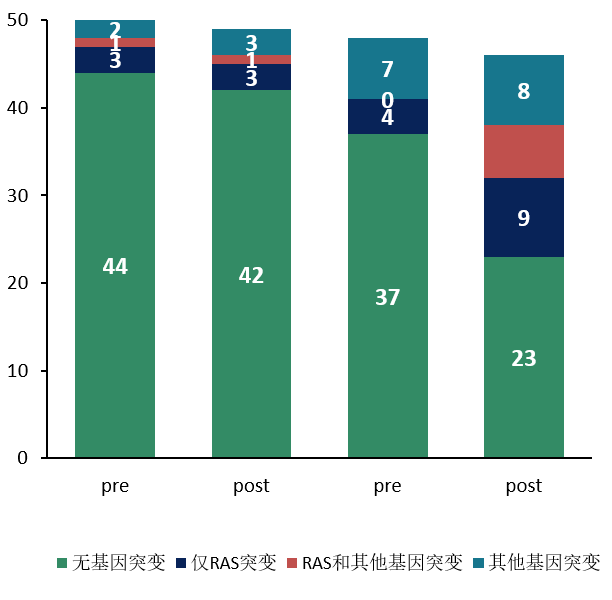
C-R方案西妥昔单抗治疗后突变率显著增加。
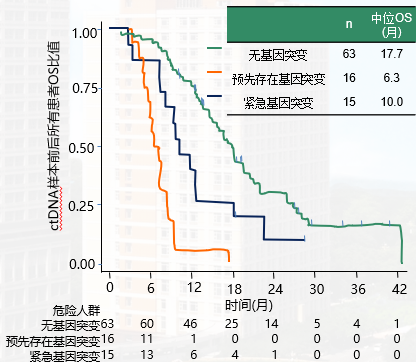
无基因突变患者(即持续抗血管)中位生存期更长。
通过对比两种药物的第一阶段治疗前后基因状态,可以看出,瑞戈非尼治疗前后没有明显差异。而西妥昔单抗治疗后基因突变患者数明显增多,说明:治疗1阶段西妥昔单抗治疗后发生紧急基因突变的患者增多。因贝伐珠单抗进展后先使用拜万戈®的持续抗血管治疗不影响基因状态,可能是R-C方案中位OS延长6个月的主要原因。
三线化疗:
三线方案:瑞戈非尼
剂量:120mg
疗程:23
治疗起止日期:2017/08/03~至今
治疗时间:27m
最佳疗效:SD
不良反应:I度高血压,I度手足综合症
末次随访:未PD
三线PFS:27m
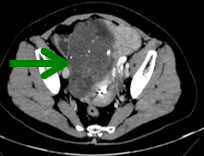
基线
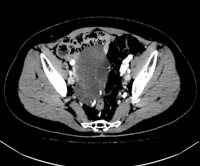
1程后 SD

3程后 SD
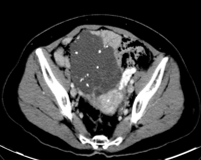
6程后 SD
末次CT:2019-11-20,SD
病例总结:
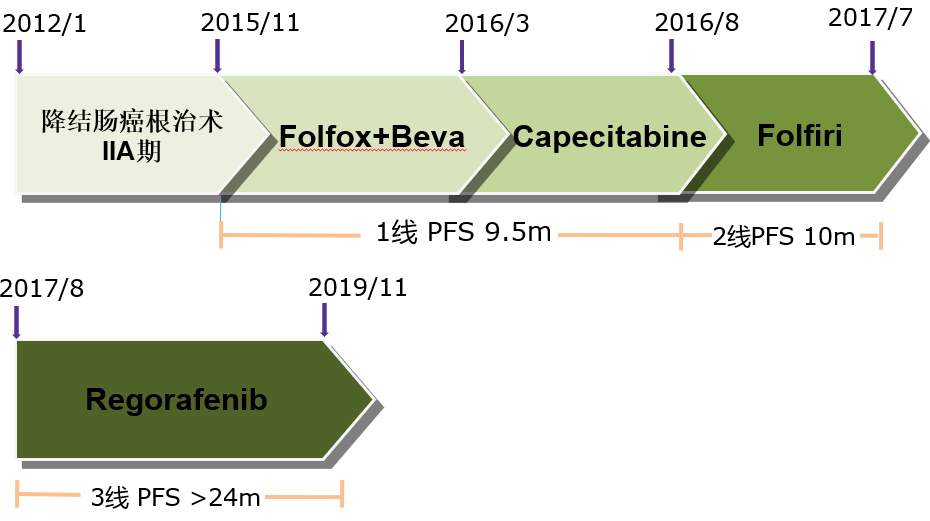
OS ≈ 4 years
查看更多