查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





北京协和医院 陈雪妍 李骥 李景南
患者女性,51岁。因“反复大量水样便 1 年半”入院。
患者于 2022 年 11 月因“结膜炎”口服二丁颗粒等中成药,后逐渐出现黑绿色水样便,5~8次/d,每次约 200~300 ml,总量约1~2 L/ d,有恶臭,无明显不消化食物,对症止泻治疗效果欠佳。2022年12月出现进食后恶心,呕吐胃内容物及胆汁,无呕吐隔夜宿食,外院胃镜示“慢性非萎缩性胃炎”,结肠镜示“盲肠炎、糜烂性结肠炎”。予益生菌、抑酸对症治疗后腹泻好转,排黄色成形软便 1 次/d。2023年2月受凉后再发腹泻,排黑绿色水样便 7~8 次/d,总量同前,伴恶心、呕吐、反酸。就诊于当地医院,住院查血常规正常,粪便常规+隐血试验(OB)阴性。血清白蛋白(Alb)正常,C反应蛋白(CRP)5 mg/L (0<3 mg/L),免疫球蛋白G(IgG)正常,抗脱氨基麦醇溶蛋白抗体IgG(+),余乳糜泻抗体谱阴性。
胃镜及结肠镜检查:十二指肠、末段回肠绒毛短,未见糜烂、溃疡。
病理:十二指肠及末段回肠黏膜重度慢性炎,绒毛萎缩消失,上皮及固有层内以淋巴细胞为主的炎细胞浸润。
考虑诊断乳糜泻,给予去麦胶膳食及甲泼尼龙 28 mg qd 口服治疗,患者腹泻缓解。

患者中年女性,慢性病程,反复大量水样泻,每日量>1 L,有恶臭,无不消化食物,对症治疗效果不佳,CRP轻度升高,血脱氨基麦醇溶蛋白抗体IgG阳性,存在小肠绒毛萎缩,且上皮内淋巴细胞增多。从腹泻类型上考虑,患者存在水样泻,便量>1 L,须考虑渗透性腹泻(包括吸收不良性腹泻)或分泌性腹泻,可见小肠绒毛萎缩,更支持渗透性腹泻或吸收不良性腹泻,但分泌性腹泻不完全除外。另患者存在乳糜泻抗体谱的阳性,组织病理学提示小肠绒毛萎缩,上皮内淋巴细胞浸润增多,高度支持乳糜泻的诊断,但上皮内淋巴细胞数量不详,小肠绒毛萎缩严重程度有待明确。多数情况下去麦胶膳食的疗效对于乳糜泻的诊断也比较重要,后续要严密观察患者停用激素、单独去麦胶膳食后疗效。在鉴别诊断方面,其他导致小肠绒毛萎缩、吸收不良性腹泻的病因仍须警惕,包括自身免疫性(自身免疫性肠病、免疫缺陷病继发)、肿瘤性(淋巴瘤)、炎症性(嗜酸性粒细胞性胃肠炎、炎症性肠病)、药物性(奥美沙坦、吗替麦考酚酯等)、感染性及特发性小肠绒毛萎缩。

患者于外院出院后继续去麦胶膳食及激素治疗,当甲泼尼龙减量至2 mg qd 时患者腹泻再发,每日水样便总量达3~4 L/d。再次就诊于当地医院,检查提示存在低钾血症、轻度代谢性酸中毒,积极补液支持、纠正水电解质及酸碱紊乱,给予甲泼尼龙40 mg qd治疗后症状改善。考虑患者存在激素依赖,先后加用沙利度胺和环磷酰胺治疗。2024 年1月,当甲泼尼龙减量至 25 mg qd时,患者出现腹胀、恶心、呕吐、腹泻,当地医院再次足量激素联合抗白介素(IL)-12/IL-23单抗(2程)治疗,腹泻无好转。2024年5 月,患者出现咳嗽、咳痰、高热,Tmax 39.5℃,血气分析提示Ⅰ型呼吸衰竭,胸部影像提示肺部多发斑片影,考虑肺部感染,予积极抗感染及人免疫球蛋白治疗,停用激素,肺部感染逐渐控制,而腹泻无明显好转;此外,外院影像学还显示,患者存在腰椎压缩性骨折、多处肋骨骨折,予积极补钙及补充维生素D治疗。为进一步诊治收入我院。患者自发病以来,睡眠尚可,小便偏少,体重下降 5 kg。无反复口腔溃疡以及关节痛。
既往体健,否认手术史,否认药物过敏史。个人史、月经婚育史及家族史无特殊。
T 36℃;P 120 次/min;R 20 次/min;血压 80/54 mmHg;体重 35.5 kg;体质指数 13.9 kg/m2。库欣貌,神志清。鼻空肠营养管固定良好。睑结膜稍苍白,胸骨、肋骨多发压痛,双肺呼吸音清,左下肺呼吸音低,未闻及干湿性啰音及胸膜摩擦音。腹软,无压痛、反跳痛,肝脾肋下未及,双下肢轻度可凹性浮肿。
腹泻、小肠绒毛萎缩原因待查;重度骨质疏松;多发肋骨骨折;腰椎压缩性骨折;肺部感染史。

患者持续去麦胶膳食及坚持甲泼尼龙治疗减量过程中再发腹泻,初期激素加量后症状改善,存在激素依赖,但先后经验性加用沙利度胺、环磷酰胺、足量激素、抗IL-12/ IL-23单抗治疗后均无效,提示存在激素抵抗,且出现了机会性肺部感染、重度骨质疏松伴病理性骨折。那么患者的诊断还能用乳糜泻解释吗?应如何去明确诊断?
接诊慢性腹泻患者,首先需明确腹泻的病生理分型,该患者水样泻可达3~4 L/d,伴电解质及酸碱平衡紊乱,粪便无红白细胞,考虑分泌性腹泻、渗透性腹泻可能,可行禁食试验明确。其次,患者拟诊乳糜泻,但起病较晚、去麦胶膳食效果不佳,病理诊断不确切,不支持这一诊断;尽管部分乳糜泻可在6~12月内对去麦胶膳食无反应(无反应性乳糜泻),或对12月以上的去麦胶膳食无反应(难治性乳糜泻),但遇到上述两种情况均需要先明确诊断。因此,须复查麦胶敏感性抗体谱,复核外院内镜病理或重复内镜活检。再次,排查其他病因。患者无反复感染史,IgG正常,肠道病理未报浆细胞显著减少或缺如,故暂无明确原发性免疫缺陷证据;无热带地区居留史,发病前非免疫抑制状态,无胃肠外的其他明显症状,惠普尔病(Whipple病)证据不足,可行组织过碘酸-雪夫染色(PAS染色)或病原体全基因组测序筛查;无明确肠道溃疡性病变、外周血及组织中嗜酸性粒细胞计数不高,炎症性肠病、嗜酸性粒细胞性胃肠炎证据不足。
成人自身免疫性肠病(AIE)可表现为去麦胶膳食无效的慢性腹泻,麦胶性肠病抗体谱阴性,伴小肠绒毛萎缩,上皮内淋巴细胞浸润少见,而杯状细胞、帕内特细胞减少或缺如,可见凋亡小体,治疗上对激素治疗有效,因此,该患者须警惕AIE。

入院后,患者大便为水样便,总量2~3 L/d,48 h禁食后大便总量减少至1 L/d 左右,提示腹泻以分泌性腹泻为主,合并渗透性腹泻可能。查胃泌素正常,生长抑素受体显像阴性,无明确神 经内分泌肿瘤证据。查免疫球蛋白正常,人类免疫缺陷病毒抗体检测(HIV-Ab)阴性,淋巴细胞亚群提示 CD4+ T细胞计数正常,B 细胞数量轻度减低,提示无显著体液免疫、细胞免疫缺陷。复查麦胶敏感性抗体谱阴性,外院组织病理学切片送我院会诊,小肠(十二指肠)黏膜活动性炎症,小肠绒毛消失,未见杯状细胞及帕内特细胞,无浆细胞减少或消失,形态符合自身免疫性肠病。
胃镜 复查胃镜可见十二指肠球、降部黏膜肿胀,小肠绒毛变短,偶见扇贝样改变(图1)。
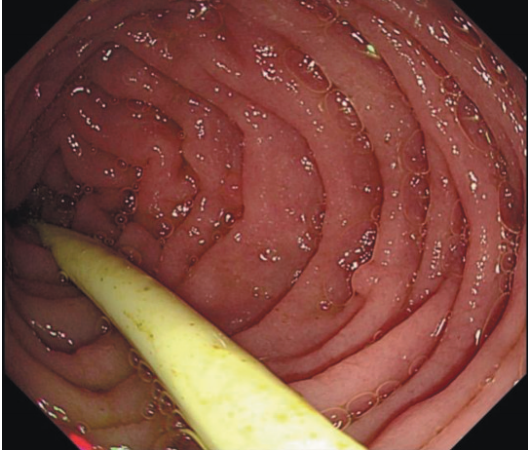
图1 胃镜提示十二指肠球后、降部黏膜皱襞稍肿胀,绒毛变钝, 可见扇贝样改变
病理 小肠(十二指肠)绒毛重度萎缩,杯状细胞、帕内特细胞明显减少,上皮内少许淋巴细胞浸润,浆细胞无明显减少,符合自身免疫性肠病(图2)。
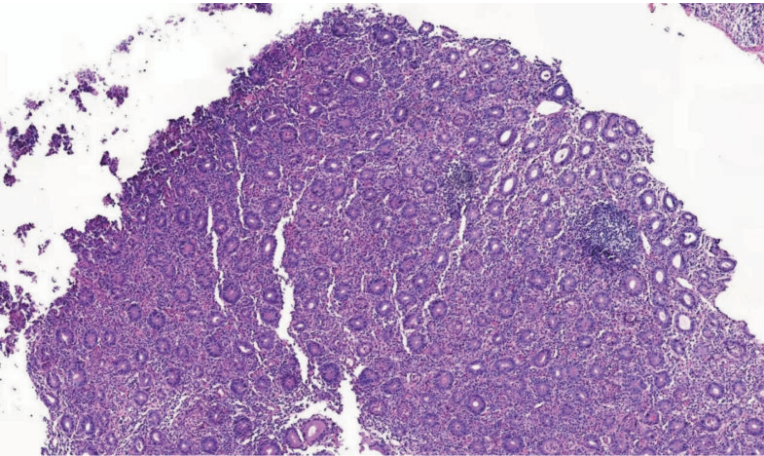
图2 十二指肠降部黏膜活检病理结果:小肠(十二指肠)绒毛重度萎缩,杯状细胞减少(10×)
此外,患者咳嗽、咳痰好转,复查胸部影像提示肺部斑片影消失,提示肺部感染已被控制。
乳糜泻和AIE都可出现难治性腹泻、小肠绒毛萎缩,前者很少出现分泌性腹泻,且多数情况下去麦胶膳食有效,而后者80%为分泌性腹泻且对去麦胶膳食无效;前者多数情况下乳糜泻抗体谱阳性,后者只在极少数个案中报道存在乳糜泻抗体阳性;前者组织病理学中存在显著的上皮内淋巴细胞浸润,无明显杯状细胞、帕内特细胞减少,后者典型的组织病理学特点,包括杯状细胞、帕内特细胞减少或消失。综上,该患者诊断更支持成人AIE。进一步结合2018年《成人自身免疫性肠病:梅奥诊所罗切斯特分院经验》(以下简称《梅奥标准》)及2025年北京协和医院提出的修正后的“成人AIE诊断标准”(以下简称“协和标准”),患者无明确免疫缺陷证据,乳糜泻诊断不成立,最终确诊为成人AIE。
患者最终确诊成人自身免疫性肠病。

患者已存在激素依赖、激素抵抗,常规免疫抑制剂疗效不佳,且出现机会性感染及重度骨质疏松,后续AIE治疗药物如何选择?
数据分析显示,半数以上的AIE患者疾病会复发,且有近2/3患者存在激素依赖或激素抵抗,治疗棘手。国内外尚无高水平研究数据支持激素依赖、激素抵抗成人AIE的治疗选择。此前,笔者团队曾汇总国际报道的成人AIE相关数据发现,其中41%患者曾使用免疫抑制剂治疗,包括硫唑嘌呤、他克莫司、沙利度胺、环磷酰胺等。2025 年8月,笔者团队还汇总了北京协和医院31例成人AIE临床资料并进行随访分析,发现 35.5%患者存在激素依赖,39.4%患者存在激素抵抗,15例患者接受低剂量他克莫司(血药浓度维持在3~5 ng/ml)治疗有效或获得临床缓解,且他克莫司治疗有助于减停激素、促进组织病理学改善或缓解。此外,国外也有个案报道,抗英夫利西单抗有助于控制AIE病情,对于存在基因突变的AIE患者接受针对性的单抗或小分子药物也有助于改善患者预后。该患者曾在病程中使用抗IL-12/IL-23单抗效果不佳。
患者曾存在机会性感染,此次入院评估感染已痊愈,无加用免疫抑制治疗禁忌。因此,经知情同意后,患者同意使用他克莫司治疗。

在院期间,评估患者存在明显营养不良,积极给予经鼻空肠管肠内营养支持治疗,并加用他克莫司 1 mg 2 次/d,5 天后患者腹泻好转,逐渐减少至2~3次/d,稀糊便,总量 300~400 ml。监测他克莫司血药浓度维持在3 ng/ml左右。半年后,患者体力、体重恢复正常,逐渐饮食过渡至正常饮食,无腹泻。建议患者择期复查胃镜并进行十二指肠黏膜活检明确组织恢复情况,患者希望在2026年中复查。
成人AIE的治疗包括一般性支持治疗及对因治疗。其中,营养支持治疗尤其重要。患者存在显著的小肠绒毛萎缩、肠道吸收功能严重受损,鼻饲要素膳食是患者可以耐受的较好的营养支持方式。在对因治疗方面,小剂量他克莫司成功诱导并维持了该患者的临床缓解,有效控制原发病,避免了疾病的复发以及激素的再次暴露,为成人AIE的治疗药物选择提供了经验。
诚然,成人AIE存在复发风险,且尚未对患者小肠绒毛的恢复情况进行内镜及组织学评价,因此,他克莫司维持治疗的疗程尚不明确。笔者团队曾长期随访AIE患者,有近一半患者复查胃镜可见内镜下小肠绒毛恢复正常,且组织病理学恢复正常,其停用药物后复发风险降低,但上述经验仍有待积累和总结。
疾病分析
AIE 是一种非常罕见的肠道疾病。该病于1982 年首次在儿童患者中被报道;1997年首次在两名成年患者中发现。AIE相对多见于婴幼儿,成人AIE发病率极低。截至2024年底,全球报道的成人AIE患者仅208 例,中位发病年龄为 49.0 岁,男女比例为1∶1.3,中位病程为6个月。广义上,AIE包括儿童原发性AIE、儿童综合征性 AIE、成人原发性 AIE、成人继发性AIE、副肿瘤性AIE;而狭义上,临床更关注成人原发性AIE。
随着对成人 AIE 认识的逐渐增多,特别是 2007 年梅奥诊所基于对15例成人AIE患者的总结,提出了首个诊断标准,该标准同时考虑了患者的临床和病理特征,即① 成人持续>6周的腹泻;② 有吸收不良的表现;③ 小肠黏膜特征性的病理改变(部分或完全的小肠绒毛钝缩,深部隐窝淋巴细胞浸润,隐窝凋亡小体 增多,少量上皮内淋巴细胞增多);④ 排除其他导致小肠绒毛萎缩的疾病,如乳糜泻、普通变异型免疫缺陷病;⑤ 抗肠上皮细胞抗体和(或)抗杯状细胞抗体阳性。同时满足①~④ 条标准即可以诊断,抗体阳性更加支持诊断,但抗体阴性也不能除外诊断。
2018 年,梅奥诊所又对该诊断标准进行修订,强调了病理诊断中杯状细胞、帕内特细胞消失,以及除外其他引起小肠绒毛萎缩疾病的重要性,删除了抗杯状细胞抗体、抗肠上皮细胞抗体的诊断条目。2025 年,北京协和医院结合自身经验,特别是通过与普通变异性免疫缺陷病胃肠受累患者的比较,提出了修正的“成人 AIE 诊断标准”(表1)。相较于《梅奥标准》,“协和标准”纳入了 5条组织病理学特征,强调了须除外严重的免疫缺陷,且增加了支持 AIE 诊断的条目,有助于对拟诊成人 AIE 但不完全符合必备条件的患者及时采用经验性激素治疗。
表1 2025年北京协和医院修订的“成人AIE诊断标准”
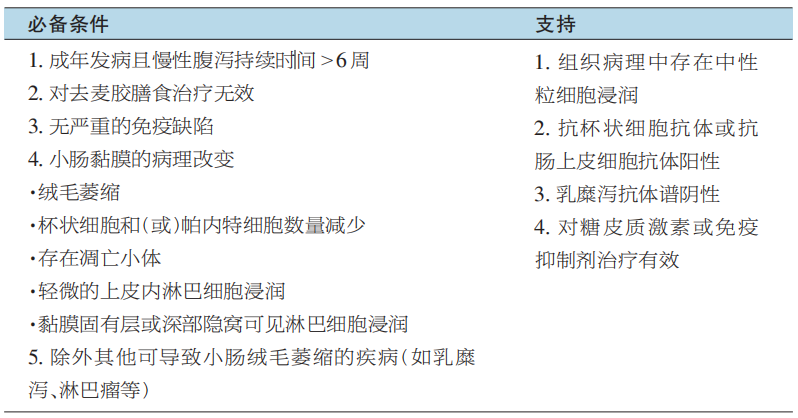
回顾本患者的临床特征、组织病理学特征和药物治疗效果,均符合 2018 年《梅奥标准》及 2025 年的“协和标准”。需要说明的是,此前文献报道部分成人 AIE 抗体或肠上皮细胞抗体患者存在抗杯状细胞,且该抗体阳性有助于 AIE 诊断,然而,上述抗体并非AIE的致病性抗体,其在其他肠道疾病中也存在一定阳性率,且北京协和医院单中心队列中接受上述抗体检查患者的两项抗体指标均为阴性,因此,临床中对于上述抗体的临床价值仍在研究中。
目前,成人AIE尚缺乏治愈性手段。其治疗包括一般支持性治疗、免疫抑制治疗及生物制剂治疗等。一般支持性治疗包括纠正水电解质、酸碱紊乱,积极营养支持,及其他对症治疗。免疫抑制治疗主要包括糖皮质激素及免疫抑制剂人。AIE 糖皮质激素是目前成治疗的首选药物。对于病情较重、一般情况差、白蛋白明显降低的患者,首选静脉糖皮质激素治疗,然后序贯口服治疗。多数患者在 3~7 天内腹泻改善。如前所述,2/3的患者存在激素依赖或激素抵抗,需要免疫抑制剂治疗,结合文献及笔者团队经验,他克莫司或许为首选的免疫抑制剂,小剂量就可以起到诱导、维持疾病缓解的作用,但仍需要更多经验总结及报道来证实其安全性及有效性。有个案报道,生物制剂包括抗肿瘤坏死因子(TNF)单抗、抗整合素单抗、抗 IL-12/IL-23 单抗及造血干细胞移植有助于控制发表偏移 AIE 病情,且相关研究极。但考虑到少,在使用时需要做好充分的知情同意。本例患者曾使用抗 IL-12/IL-23 单抗无效,也进一步支持更谨慎的生物制剂药物治疗选择。
成人 AIE 具有较高的疾病复发风险,笔者团队曾对26例成人AIE进行长程随访,1年、4年的累积复发风险为 47.9%、65.2%。此外,AIE患者随访中也须警惕恶性肿瘤的发生,特别是淋巴瘤、消化道肿瘤等。
第一,成人AIE极其罕见,虽诊断标准不断演变,但仍缺乏疾病诊断的“金标准”,而诊断及鉴别诊断困难,极易造成漏诊或误诊。第二,成人 AIE 容易复发,一线激素治疗有效,但有相当比例的患者存在激素依赖或激素抵抗,二线药物治疗选择缺乏高级别循证医学证据支撑。第三,在面对机会性感染时,把握免疫抑制治疗强度与避免再发机会性感染是天平的两端,需要做好平衡。
首先,对于疑难慢性腹泻患者,从其病生理机制分型入手,是做好诊断及鉴别诊断的首要节点。其次,对于成人AIE这样的疑难、罕见疾病,多学科协作是疾病诊断、药物治疗决策最强有力抓手。再次,面对缺少循证医学证据支持的罕见疾病,医生在进行临床决策时,需要进行充分的医患沟通,向患者全面告知病情、治疗方案及潜在风险,医患携手共进,才能最大限度为患者争取更好的预后。
对于诊断疑难的慢性腹泻患者,从其病生理机制分型入手,是做好诊断及鉴别诊断的首要节点。成人AIE是一种罕见、疑难危重的肠道自身免疫性疾病,诊断缺乏“金标准”,医患认识不足,漏诊及误诊率高,且容易复发,需要长期随访。该疾病的诊治离不开多学科诊疗团队协作,更需要医患共同决策。此外,随着我国罕见病研究的不断深入,契合中国罕见病患者诊治的科研成果不断产出,也将为世界罕见病的诊治贡献更多中国力量。

消化内科副主任、教授
中华医学会消化病学分会副主任委员
中国医师协会消化医师分会副会长

北京协和医院消化内科副主任
中华医学会消化分会消化肿瘤协作组副组长
中华医学会消化分会消化系统罕见病研究协作组成员
中国罕见病联盟/北京罕见病诊疗与保健学会消化病学分会副主任委员
北京罕见病诊疗与保障学会第二届理事会青年委员
亚洲炎症性肠病协会(AOCC)临床研究委员会委员
海峡两岸医药卫生交流协会消化分会青年委员会副主任委员及炎症性肠病学组委员
版权说明:本文来源于中国医学论坛报“罕见病临床思辨”专栏,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。
查看更多