查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





作者:东部战区总医院国家肾脏疾病临床医学研究中心 王霞 刘正钊
通信作者:王霞
病史摘要61岁男性患者,临床表现间断浮肿,少量蛋白尿伴有明显低蛋白血症,肾功能正常。肾外无高血压、糖尿病、皮疹、关节痛、腹痛、黑便,病程中偶有腹胀,无腹泻,无恶心、呕吐,体重无明显变化。
症状体征 BP 117/81mmHg,心率78次/分,身高174cm,体重78.5kg,BMI 25.9kg/m2,神清,咽不红,扁桃体不大,心、肺、腹部未见明显异常,双下肢轻度浮肿。
诊断方法 肾活检穿刺检查提示肾小球轻微病变。胃镜提示:胃窦黏膜充血水肿糜烂;胃体黏膜皱襞充血肥大、大弯侧黏膜增生隆起;胃底皱襞充血肥大如脑沟回样迂曲。
治疗方法给予艾司奥美拉唑片抑制酸、益肾丸保肾治疗。
临床转归 尿检完全缓解,白蛋白升至正常范围。
关键词:肾小球轻微病变;非肾病性蛋白尿;低蛋白血症;
引 言
巨大肥厚性胃炎是由于胃黏膜的过度增生而使胃壁广泛增厚,又称为 Ménétrier 病,是一种特殊类型的胃炎,临床罕见,男性好发,年龄为 40-55 岁,临床表现主要包括上腹痛、体重下降、呕吐、上消化道出血、腹泻以及胃源性蛋白丢失。胃体、胃底黏膜皱襞粗大、胃酸分泌减少和低蛋白血症。报告 1 例肾小球轻微病变合并严重低蛋白血症,经质子泵抑制剂治疗后病情缓解的病例,旨在提高临床医生对低蛋白血症、非肾病性蛋白尿的认识,提高低蛋白血症的诊治水平,避免漏诊、误诊。
临床资料
一、一般资料
患者,男性,61岁,2016年12月出现双下肢浮肿, 2017年3月7日检查尿蛋白567mg/24h,血白蛋白17.7g/l,肌酐78umol/L,予氯沙坦钾片、百令、利尿、降脂、抗凝等治疗。仍间断浮肿但未复查。2018年期间曾行胃肠镜检查提示:慢性胃炎、肠息肉。2019年4月26日我院查尿蛋白0.7g/24h,肌酐1.06mg/dl、白蛋白25.7g/L、球蛋白23.8g/L、胆固醇18.11mmol/L、甘油三酯4.99mmol/L,血糖8.06mmol/L(餐后),血抗PLa2R阴性。肾脏B超116/115mm、皮质回声稍增强。病程偶有腹胀,无腹泻,无恶心、呕吐,体重无明显变化。个人史、家族史无特殊。
患者因双下肢浮肿就诊,发现明显低蛋白血症,但尿蛋白定量仅为少量蛋白尿,而自诉食欲正常,偶有腹胀,无恶心、呕吐、呕血、便血及黑便,体重无明显变化。曾行胃肠镜检查提示慢性胃炎、肠息肉,余无特殊。患者无吸烟史、饮酒史及药物滥用史。患者所表现的低蛋白血症、非肾病范围蛋白尿,与典型的肾病综合征不相符合,无营养不良因素,无严重感染、慢性消耗性疾病表现,是否存在蛋白质合成障碍及蛋白质丢失过多等需要进一步完善检查。
二、检查
白蛋白 23.2g/L、球蛋白 17.4g/L、ALT 18U/L、AST 22U/L、BUN18.5/dl、SCr 1.12mg/dl、UA 476μmol/L、胱抑素C 0.92mg/L,TC 15.12mmol/L、TG 3.82mmol/L,钙 1.95mmol/L、空腹葡萄糖6.29mmol/L, HbA1c 6%。
自身抗体:ANA、抗ds-DNA、PLA2R阴性;体液免疫:IgG 3.46g/L;补体C3 0.649g/L、补体C40.1g/L。淋巴细胞免疫分型:CD8 465/ul、CD4 1333/ul、CD3 1781个/ul,CD20 89个/ul;
肿瘤标志物:CA125 206.2U/ml,余正常。血轻链比值正常,免疫固定电泳图谱阴性。
肝纤维化:Ⅲ前胶原N端肽33.31ng/ml,透明质酸(HA)79.07ng/ml、层粘连蛋白(LN)25.75ng/ml、Ⅳ型胶原(CIV)28.14ng/ml。胃蛋白酶原正常;大便常规正常;粪钙卫蛋白62.8ug/g(0-50);13C尿素呼气试验:阴性。
眼底检查未见虹膜炎。
腹部CT:1、双肾周渗出、腹腔渗出,盆腔积液;2、左肾结石;3、前列腺钙化灶。肺部CT:1、左肺少许机化性炎症,左侧少量胸腔积液;左侧胸膜增厚;2、心包积液;主动脉及冠状动脉粥样硬化。心脏彩超:左心房内径37mm,右心室内径27mm,室间隔厚度9mm,左室后壁厚度11mm。LVEF63%。1、主动脉瓣钙化。2、少-中等量心包积液。心电图:窦性心动过速;顺钟向转位、电轴左偏、低电压趋势。
肾活组织检查:免疫荧光:IgM trace,弥漫分布呈颗粒状沉积于系膜区,余阴性。 IgG、IgA、C3、C1q阴性;κ轻链、λ轻链均阴性。光镜:系膜区节段轻度增宽,毛细血管袢开放好,囊壁节段增厚。PASM-Masson:阴性。小灶性小管萎缩、基膜增厚,散在小管上皮细胞刷状缘脱落,数处小管炎,管腔内少量蛋白管型,间质小灶性单个核细胞及少量浆细胞浸润,小灶性水肿。动脉未见明确病变。电镜:观察2个肾小球。肾小球系膜区增宽,系膜基质增多,系膜区、基膜内、上皮侧未见电子致密物沉积,基膜厚度300-510nm。肾小球足细胞足突融合约10%~20%。(图1)
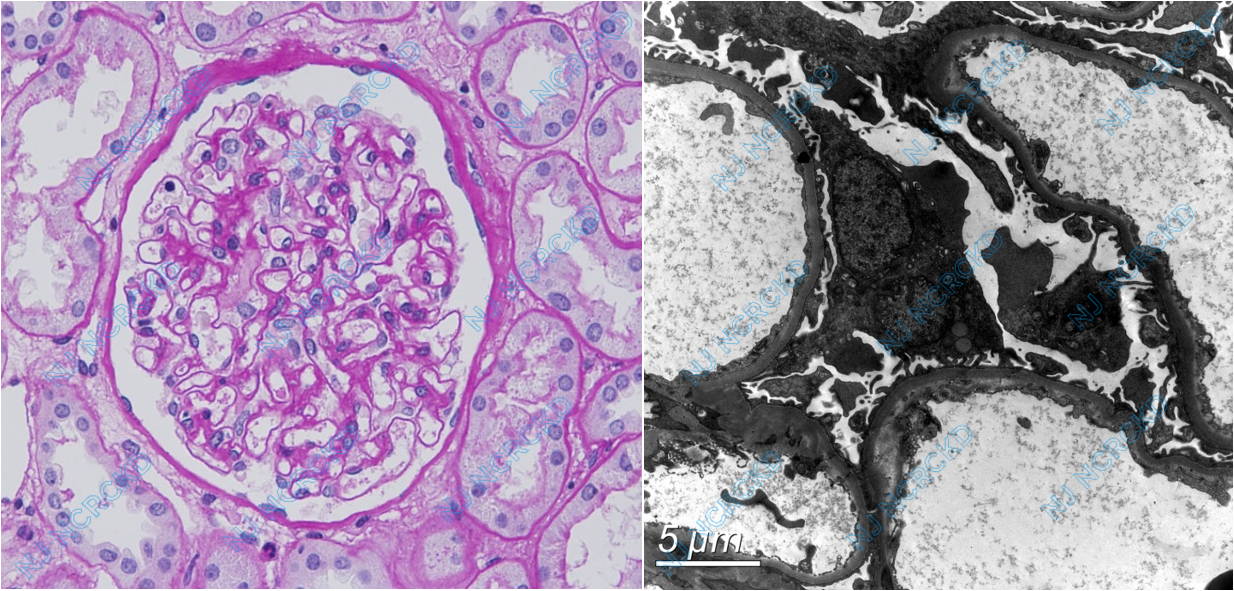
图1.肾活组织病理检查(A:PAS×200;B:电镜)
三、诊断与鉴别诊断
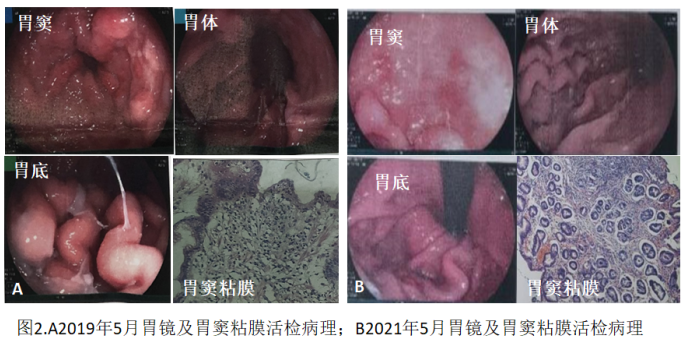
该患者临床主要表现为浮肿、严重低蛋白血症,而患者INR值、前白蛋白、胆碱酯酶正常,提示肝脏合成功能正常,尿液检查提示少量蛋白尿,肾活检光镜为轻度系膜增生性肾炎,电镜下足突融合比例不高,提示血白蛋白并未肾源性丢失,从肾脏角度难以解释患者为何存在严重低蛋白血症。患者进食大致正常,其明显的低蛋白血症也并非摄入减少所致。腹部CT 扫描并未发现肿瘤存在的证据,胸腔积液和腹水可能是由于低蛋白血症导致的漏出液。粪钙卫蛋白检查超出正常范围,故该患者故重点考虑肠源性蛋白丢失多所致可能性大。出院时给予患者给予艾司奥美拉唑片抑制酸、中成药保肾治疗。外院完善胃镜检查提示:胃窦粘膜充血水肿糜烂;胃体粘膜皱襞充血肥大、突融侧粘膜增生隆起;胃底皱襞充血肥大如脑沟回样迂曲 (图2A)。病理提示:(胃窦黏膜)中度慢性浅表炎伴轻度急性活动。诊断:胃窦病变性质待定:巨大肥厚性胃炎?结合患者临床临床表现诊断考虑:巨大肥厚性胃炎,继发性低蛋白血症。
四、治疗
给予艾司奥美拉唑片抑制酸、益肾丸保肾治疗。
五、治疗
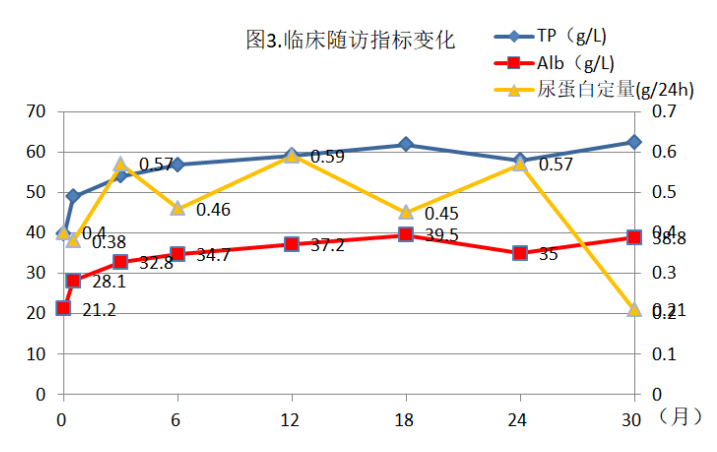
给予艾司奥美拉唑治疗半月后复查白蛋白升至28.1g/L,肌酐1.01mg/dl,尿蛋白定量0.38g/24h。半年后复查白蛋白升至34.7g/L,1年后复查白蛋白37.2g/L。尿蛋白定量波动0.49-0.21g/24h。末次访视(2021年12月7日):肌酐0.89mg/dl,白蛋白38.8g/l,胆固醇6.27mmol/L,甘油三酯1.56mmol/L,尿蛋白定量0.21g/24h,微量白蛋白尿14.01mg/24h。(图3)
2021年5月复查胃镜提示:胃体大弯侧皱襞粗大肥厚、表面散在红斑糜烂;胃窦及胃底表现为黏膜充血。病理提示:(胃窦黏膜)中度慢性浅表炎(图2B)。
讨 论
低蛋白血症是临床常见的临床综合征,常见的原因包括蛋白摄入不足或吸收不良(饥饿,营养不良等)、蛋白质合成障碍(肝脏疾病)、蛋白质分解加速(长期发热、恶性肿瘤、皮质醇增多症、甲状腺功能亢进等)、体内蛋白消耗过多(严重感染、慢性消耗性疾病等),蛋白质丢失过多(失血、烧伤、腹水穿刺)、蛋白沉积到器官(系统性淀粉样变性)、血液稀释等。而本例患者低蛋白血症,与典型的肾病综合征的表现并不相符,尿检提示非肾病范围蛋白尿,分析原因排除了肝脏合成功能障碍、营养不良及慢性消耗性疾病。而对于胃肠丢失蛋白,不能完全除外,患者基于曾行胃肠镜检查未见异常为由拒绝复查。而尿液检查提示少量蛋白尿,故望从肾活检病理的角度为诊断拨开云雾见月明。肾活检光镜为轻度系膜增生性肾炎,电镜下足突融合比例不高,提示血白蛋白并未肾源性丢失,从肾脏角度难以解释患者为何存在严重低蛋白血症。高度考虑肠源性蛋白丢失多所致可能性大。再次建议行胃镜检查提示胃黏膜皱襞肥厚,从而发现患者低蛋白血症原因。给予质子泵抑制剂治疗后,患者低蛋白血症纠正,尿检缓解,肾功能稳定。复查胃镜提示胃黏膜皱皮肥厚较前明显缓解,最终诊断低蛋白血症,巨大肥厚性胃炎所致。
巨大肥厚性胃炎是一种罕见获得性胃病,常见于中年男性,起病隐匿,进展缓慢对于儿童,该疾病可能自发缓解,或在使用更昔洛韦治疗CMV感染后消退。尽管先前的研究表明其与幽门螺杆菌和CMV等病原体的感染有关,但其发病机制尚不清楚,涉及表皮生长因子受体信号转导增强,从而导致胃黏液上皮细胞增生。在患者的胃黏液细胞中肿瘤坏死因子α(TNF-α)水平升高,提示该病的发生可能与TNF-α诱导的增生有关。其确诊的依据是对过度增生的黏膜皱襞进行活检,发现胃小凹增生、腺体萎缩、壁细胞数目减少。对临床怀疑、内镜下表现为胃皱襞增厚和特征性组织学改变,包括:小凹增生、腺体弯曲和扩张、壁细胞数量减少和炎性浸润,应考虑巨大肥厚性胃炎。而本例患者胃黏膜活检未取到腺体,排除了恶行肿瘤证据,根据胃皱襞增厚的特征,结合相关检查未发现存在巨细胞病毒或者幽门螺杆菌感染证据,低蛋白血症暂考虑胃源性蛋白丢失,仅质子泵抑制剂治疗症状很快得到缓解,最终诊断为巨大肥厚性胃炎。
巨大肥厚性胃炎可能与胃癌风险增加有关,但该风险的大小尚不清楚,在已发表的病例中变化在0%~10%之间。故应对患者进行长时间的随访,目前的建议是每1至2年进行一次内窥镜对照评估。
鉴别诊断包括继发于幽门螺杆菌、巨细胞病毒、组织胞浆菌病、结核、支原体、梅毒、隐球菌病或曲霉菌病的感染性相关胃炎;肿瘤如淋巴瘤、腺癌、Zollinger-Ellison综合征、浸润性病变如结节病、淀粉样变性或其他原因如嗜酸性胃肠炎或胃静脉曲张。
巨大肥厚性胃炎的治疗仍存在争议。对于较轻微的病例,主要治疗为支持性治疗,在这种情况下,我们给予质子泵抑制剂对症支持治疗,患者的症状得以完全缓解。
综上,低蛋白血症是临床常见表现,临床医师在诊断中要充分鉴别,对于高度疑诊的情况,可尝试性治疗,并做好定期随访复查,根据患者指标变化及时修正诊断,避免漏诊、误诊。
参考文献:略
来源:东部战区总医院供稿
查看更多