查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





作者:首都医科大学附属北京天坛医院 杨中华
诊断
检测PFO和临床相关分流的最佳方法是什么?
可通过直接观察PFO或辨认RLS来检测PFO。可用的工具包括经食管超声心动图(TEE)、经胸超声心动图(TTE)、经颅多普勒超声心动图(TCD)和心内超声心动图。它们都有不同的优势和局限性。可通过TEE、TTE或TCD注射对比剂(c-TEE、c-TTE或c-TCD)来评估是否存在RLS和大小。尽管彩色血流多普勒TEE可以显示PFO内的血流,但可能会遗漏小分流。把搅动盐水(微泡)作为造影剂的一部分,在静息状态下和Valsalva动作(增加右心房的压力,提高血液通过分流通道。所有这些技术都需要专业知识和经验来执行和解释。
尽管c-TEE被认为是诊断PFO的金标准,但前瞻性研究的荟萃分析报告,与尸检、手术和右心导管插入术相比,其敏感性为89%,特异性为91%。这种差异可能归因于技术限制,包括患者对TEE探头的不耐受、镇静期间的Valsalva操作不当、患者解剖结构的变化和操作员经验。在TEE期间,可通过压迫下腔静脉,多次注射对比剂(>=5),将患者血液与搅拌过的生理盐水混合,或将搅拌过的生理盐水注入下肢静脉(导致气泡从下腔静脉直接进入心脏间隔[septum]和PFO)来提高其敏感性。
在检测PFO方面,c-TTE不如c-TEE敏感,前者通常会遗漏小的PFO。相反,据报道,c-TCD检测小RLS比c-TEE更敏感,这可能是因为Valsalva的动作做得更好。此外,各种不同的体位,c-TCD都可很容易地重复。荟萃分析显示,与c-TEE相比,c-TCD的加权平均敏感性和特异性分别为94%和92%。此外,尽管c-TCD能够检测RLS,但很难直接确认分流的部位,不过肺内分流很少见。与心内分类相比,肺内分流的微气泡更为延迟。TEE,以及某些情况下的TTE(高质量图像和谐波成像模式),允许直接显示房间隔。TEE还可以诊断动脉粥样硬化性主动脉疾病和左心耳血栓,这可能是卒中的原因。TEE是一种侵入性检查,很少引起出血、误吸或食管穿孔。因此,c-TCD的一个主要优点是无创性且成本较低。
心内超声心动图在临床实践中不是诊断的常规方法,而是在PFO闭合术中进行,可以实时高分辨可视化提供心脏结构。心内超声心动图和c-TCD高度一致。尽管传统上c-TEE被认为是诊断PFO的金标准,但鉴于c-TCD检测RLS的灵敏度高于c-TEE或c-TTE,c-TCD可作为卒中患者的筛查方法。如果检测到较大的RLS并考虑进行PFO闭合术,可通过c-TEE或心内超声心动图进行确认。
针对PFO患者管理的欧洲立场文件指出,任何技术都不能被视为诊断PFO的金标准。美国神经病学学会指南同样允许采用不同的诊断方法,但规定c-TCD可用于筛查评估RLS,尽管需要TTE或TEE来确认。需要高质量的对比研究来确定最佳诊断策略。
筛查深静脉血栓的意义是什么?
由于矛盾性栓塞是PFO与卒中因果关系的机制之一,因此在静脉循环中发现血栓,即在下肢或盆腔静脉中发现血栓,加强了特定患者PFO与卒中之间的因果关系。此外,发现血栓会改变治疗方案,比如更换为抗凝治疗或放置下腔静脉滤器。通常通过下肢超声(B型[2维])成像和脉搏波多普勒评估深静脉血栓形成(DVT),发现0%至57%的DVT患者无明显症状。大多数研究的规模较小且具为回顾性,容易产生选择偏差。
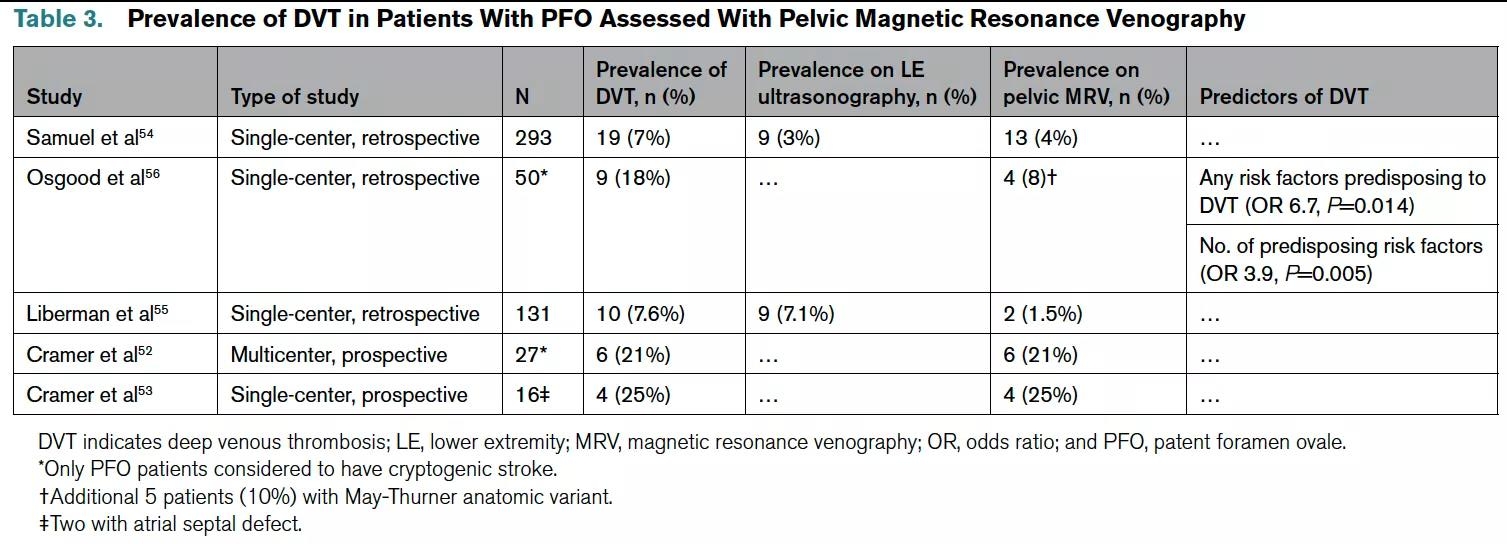
尸检研究显示,22%的先前不明原因的反常栓塞患者存在孤立的盆腔静脉或下腔静脉血栓。PELVIS研究采用磁共振静脉造影(MRV)检测骨盆DVT,研究发现PFO和隐源性卒中患者中盆腔DVT更常见(比PFO和卒中原因确定的患者),尽管差异不显著(6/27[21%]与0/9[0%],P=0.302)。在针对卒中或TIA合并PFO患者比较下肢超声和盆腔MRV的DVT检出率的研究发现,DVT总体患病率较低(表3)。大多数骨盆MRV评估的研究是单中心、回顾性的,纳入了较少的患者。值得注意的是,MRV还会发现May-Thurner解剖变异(右侧髂总动脉覆盖并把左侧髂总静脉压迫在腰椎上),这可能增加血栓形成的风险。需要进一步评估骨盆MRV以及常规进行下肢超声对伴有PFO的卒中和TIA患者的作用。此外,MRV可能会出现与血流相关的伪影,CT静脉造影可以提高对解剖学的评估,但缺乏比较数据。
需要设计精良的前瞻性研究以及成本效益分析,以改进DVT评估的患者选择。2014年美国心脏协会/美国卒中协会指南规定,患有隐源性TIA或卒中伴PFO的年轻患者,应评估下肢或盆腔静脉血栓形成;然而,这不是正式建议的一部分。
实验室检查是否有助于诊断PFO相关卒中?
有助于建立PFO与卒中或TIA之间因果关系的实验室检查可能是有用的。D-二聚体是纤维蛋白降解的产物。在纤维蛋白形成然后分解的情况下,可以看到D-二聚体水平升高。它们通常用于筛查DVT或肺栓塞,因为它们具有很高的阴性预测值,因此似乎是PFO相关卒中的潜在标志物。心源性卒中患者的D-二聚体水平通常高于其他卒中原因患者。在一项小型研究中,PFO伴ASA患者(n=18)的D-二聚体水平低于其他心源性栓塞患者(n=51;中位数分别为1.0[四分位间距,0.5-2.8]和2.0[0.7-3.5]mg/mL,P=0.020)。这表明D-二聚体可能不是区分PFO作为卒中原因与其他常见隐源性卒中原因(如阵发性房颤)的有用生物标志物。
越来越多的证据表明D-二聚体是预后的生物标志物。在570例接受了TEE检查的首次隐源性卒中患者中,241例(42.3%)检测到PFO,D-二聚体水平>1.0μg/mL是PFO患者复发性缺血性卒中的独立预测因子(危险比,5.3[95%CI,1.7–17.3],P=0.005),但在无PFO的患者中没有发现这个现象。这些结果需要进一步验证。
PFO和卒中或TIA患者BNP水平可能增加,但前提是PFO可能改变左心房的电活动,或导致心房或心室的机械拉伸。然而,脑钠肽水平可能无助于区分PFO作为卒中病因与其他常见隐源性卒中病因,如阵发性房颤。在一项PFO和ASA患者的BNP水平(n=18)的研究中,PFO患者的BNP水平低于其他心脏栓塞病因患者(n=51;中位数35[四分位数范围,13-85]与144[61-274]pg/mL,P<0.0001)。
来源:脑血管病及重症文献导读
查看更多