查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





本期将分享一例初诊时为CNLC Ⅲb期的巨块型晚期肝癌病例。患者经免疫(替雷利珠单抗)联合靶向(甲磺酸仑伐替尼)转化治疗后达到CR,并获得根治性手术的机会。
王在国 教授
主任医师、教授、岭南名医、东莞名医
广东省东莞市人民医院外科主任
广东省东莞市人民医院肝胆胰脾外科学科带头人
广东省东莞市人民医院肿瘤科学科带头人(2008-2016)
广东省抗癌协会肝癌专业委会副主任委员
广东省医学会肝胆胰外科分会常务委员
广东省医学会肝癌专业委员会常务委员
广东省医师协会肿瘤外科专业委员会常务委员
广东省医师协会胰腺病专业医师分会常务委员
广东省临床医学学会肝癌与肝转移瘤专委会常务委员
四川省抗癌协会肝癌专业委会副主任委员(1999-2001)
深圳市抗癌协会肝癌专业委会副主任委员
东莞市医学会肿瘤学分会主任委员(第1-2届)
东莞市肿瘤防治联盟肝癌专业委员会主任委
《中国肿瘤外科杂志》 、 《岭南现代外科杂志》编委
《当代医学杂志》、《中华肝胆外科杂志》(第4届)编委
李浩权 主治医师
东莞市人民医院
肝胆外科 主治医师
广东省基层医药学会肝癌防治专业委员会委员
一般资料:患者老年男性,70岁,于2020年7月6日就诊。
主诉:检查发现肝占位1月。
既往史、个人史及家族史:无特殊。
入院查体:腹部稍膨隆,余无明显阳性体征。
肝功能检查:AST 55.0U/L↑、γ-GGT 223.4U/L↑、ALP 132.4U/L↑、ALB 43.2g/L、TBIL 19umol/L。
肿瘤标记物:AFP 1635.13ng/mL↑。
HBV-DNA:7.41E+02IU/mL。
上腹部MRI+增强(2020年7月10日):肝脏右叶肿块(约112×100×97mm),肝细胞癌可能性大,伴肝右静脉、下腔静脉肝内段及肝中静脉侵犯可能,门静脉主干及其分支栓子。门腔静脉间隙结节占位(约26×35mm),邻近下腔静脉受压、变扁,淋巴结肿大、转移?如图1所示。
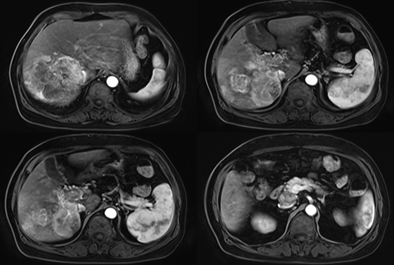
图1:治疗基线上腹部MRI+增强(2020年7月10日)
临床诊断:1.右肝巨块型癌(CNLC Ⅲb期,BCLC-C期)合并门静脉主干及右干癌栓、淋巴结转移
治疗方案:根据患者病史及影像学检查考虑诊断为右肝巨块型癌,合并门静脉主干及右干癌栓、淋巴结转移。与患者充分沟通病情,经患者充分知情同意并签署知情同意书后,自2020年7月14日起至2021年4月7日,予患者免疫联合靶向治疗9周期,具体方案为替雷利珠单抗200mg Q3W+仑伐替尼8mg QD。
实验室评价:AFP逐渐降至正常(从1653.13ng/ml降至4.88ng/ml)。
影像学评价及疗效评价:患者先后于2、6、9周期治疗后复查腹部增强CT,2周期后(2020年8月26日)AFP降至22.52ng/ml,影像学评价为完全缓解(CR),建议患者进行手术治疗,但患者自觉药物疗效较好,且对手术有顾虑,故拒绝;6周期后(2020年11月13日)AFP降至正常,MRI显示病变内上缘部分强化,再次建议患者手术或介入治疗,患者再次拒绝手术;9周期治疗后(2021年4月6日)肝右叶肿块(62×41×52mm) 伴肝右静脉破坏,现肝中静脉近段、下腔静脉肝内段受侵犯不明显,门静脉主干及其分支栓子,大部分为瘤栓,部分为血栓。门腔静脉间结节占位,较前相仿。肝左叶新结节出现,但无强化。如图4所示;影像学评价为部分缓解(PR);因出现肝左叶新发病灶,再次建议患者手术,患者同意。
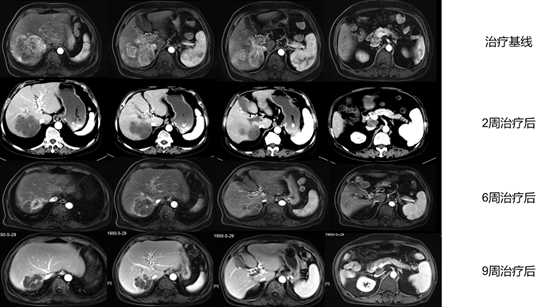
图2:治疗期间腹部增强MRI动态变化
治疗方案:患者于2021年4月9日行手术治疗(右后叶肝癌及胆囊切除术+门腔间隙淋巴结切除+肝右静脉根部结扎及肝中静脉探查+门静脉输液港置入及门脉压监测+门静脉栓子术中超声造影检查+可疑转移灶消融术)。
术后病理:1.(肝右后叶肿瘤)肝细胞肝癌,中分化,肿物大小约6.5×5×3cm。肿物内大部分为坏死组织,完全坏死区(约占90%)内未见癌细胞,均为坏死组织;半坏死区(约占10%)内见较多癌细胞及少量坏死组织;另于肿物周边距肿物0.15cm处见一结节(直径约1.3cm),该结节内全部为癌组织,未见坏死。脉管内未见癌栓,神经未见癌侵犯。(切缘)未见癌累及。周边肝组织见结节性肝硬化改变。免疫组化:CK18(+),Hepatocyte(+),HSP70(+),Glypican-3(部分+),AFP(-),CEA(-),CK19(-),GS(-),CD34(血管+),p53(少量+),Ki-67(约50%+)。特殊染色结果:网染(示肝板增厚)。2.(门腔间隙淋巴结)送检为癌组织,其内见大量坏死,肿瘤细胞约占50%,未见淋巴结结构。3.送检(肝硬化组织)肝组织结构大致正常,部分肝细胞水肿,汇管区伴少量急慢性炎细胞浸润,肝硬化改变不明显。4.(胆囊)慢性胆囊炎。如图3所示。
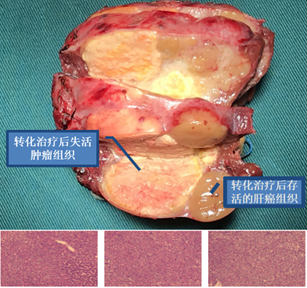
图3:术后病理
本例患者因“检查发现肝占位1月”就诊,既往体健,否认肝炎病史及肝癌家族史。结合患者病史及相关影像学检查,诊断为右肝巨块型癌合并门静脉主干及右干癌栓、淋巴结转移。患者为CNLC Ⅲb期、BCLC-C期,无手术及介入指征。
为将无法切除的病灶转化为可手术切除,经患者知情同意后采用了免疫联合靶向的全身系统性治疗方案。2周期后患者即达到了CR,建议患者进行手术治疗,但患者出于对手术的顾虑及药物疗效的信赖,拒绝手术。直至治疗9周期后,腹部MRI显示肝脏右叶肿块明显缩小,肝左叶新发病灶。综合考虑后继续予以根治性手术切除治疗,术后病理诊断为肝细胞肝癌,中分化(意味着影像学疗效评价CR不等于病理学CR,即影像学疗效评价CR时仍有可能存在病灶残留)。术后恢复良好,除反复电解质紊乱外,与普通肝切除术患者无明显不同。出院时复查腹部CT提示无肿瘤残留,且AFP降至正常,肝功能及电解质恢复正常。
原发性肝癌是肝脏最常见的恶性肿瘤,也是全世界范围内第二大癌症相关死亡原因。患者一旦出现相应症状或影像学检查提示肝脏占位病灶,疾病大多已是晚期,伴肝内或肝外转移。肝移植、手术切除、射频消融这些方式便失去了治疗机会。近年来,全身系统治疗包括新型分子靶向药物和免疫检查点抑制剂的问世,为肝癌患者带来了新希望。由于影像学检查难以精准判断肿瘤细胞是否已完全失活,所以对于不可切除的晚期肝癌,经转化治疗后,达到部分或完全缓解后均应积极行手术治疗,最大程度清除仍有活性的肿瘤细胞。
《肝细胞癌转化治疗中国专家共识(2021版)》中提到基于协同增效的作用机制、治疗的便利性与较高的转化成功率,ICIs(免疫检查点抑制剂)联合AATDs(抗血管生成靶向药物)治疗值得作为晚期肝细胞癌的转化方案进行尝试。一项旨在评估PD-1抑制剂+靶向治疗用于不可切除/晚期肝癌转化治疗的疗效和安全性的真实世界研究证实,该方案安全耐受,部分初始不可切除肝癌接受该方案治疗后可转化为可切除肝癌。本例患者的治疗过程也用临床实例证实了这一联合方案在肝癌转化降期治疗策略中的有效性。
本例患者应用的替雷利珠单抗是我国百济神州自主研发且为目前唯一成功对Fc段进行特殊基因工程改造的PD-1单抗。在临床前研究中所显示,独特结构优化使之具有避免抗体依赖性细胞介导的吞噬作用(ADCP)、Fab段彻底持久阻断PD-1/PD-L1结合、半衰期长、抗肿瘤活性强等优势。2019年CSCO会议上的口头报告指出替雷利珠单抗治疗不可手术的中国晚期肝癌患者,客观缓解率(ORR)高达17%,疾病控制率(DCR)达56%,其免疫相关不良反应也更低。此外,RATIONALE 208研究结果也证实,替雷利珠单抗单药二线治疗不可切除肝细胞癌的中位总生存(mOS)达13.8个月,近80%客观缓解患者持续缓解时间超过一年(一年DoR率79.2%);部分患者实现深度缓解,单药治疗后有3例患者达到完全缓解(CR),疗效比肩国际同类药物既往数据,表明替雷利珠单抗单药治疗或可为患者带来更多生存获益。安全性方面,≥3级治疗相关不良事件(TRAE)发生率仅为14.5%,处于同类药物较低区间。基于RATIONALE 208研究数据,国家药品监督管理局(NMPA)于6月22日正式批准替雷利珠单抗用于至少经过一种全身治疗的肝细胞癌的治疗。期待替雷利珠单抗在晚期肝癌领域的研究能够获得更多高质量数据,为临床治疗带来更多选择,为肝癌患者带来更大希望。
查看更多