查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





1. 简述肝源性糖尿病的定义?
答:肝源性糖尿病(HD)主要指除非酒精性脂肪性肝病(Non-alcoholic fatty liver disease, NAFLD)以外的其他病因肝硬化合并的糖尿病,如乙型肝炎病毒(Hepatitis B virus, HBV)和丙型肝炎病毒(Hepatitis C virus, HCV)感染、酒精性肝病、自身免疫性肝病导致的肝硬化,这些患者先有肝硬化,后有糖尿病。
2. 简述肝源性糖尿病的临床特征?
答:HD的临床特征为:(1)与肥胖、T2DM家族史等代谢和心血管危险因素的相关性较低;(2)并发糖尿病视网膜病变、心血管疾病、糖尿病足、慢性肾病的风险低;(3)高渗性昏迷、糖尿病酮症酸中毒等并发症少见;(4)易发生与肝功能受损严重程度相关的低血糖;(5)肝移植术后部分患者糖尿病可以缓解。
作者:胡靥
肝脏是葡萄糖代谢的重要脏器,当发生损伤及疾病侵袭时会导致糖代谢障碍。肝硬化病人罹患DM的危险因素包括年龄大、超重和T2DM家族史等。
研究表明,大约70%的肝硬化患者存在糖代谢障碍,肝硬化病人建议常规筛查糖尿病(DM)。慢性肝病和DM互相影响导致彼此疾病顽固难治,使得患者生活质量下降和预期寿命缩短。除了代谢相关脂肪性肝病(MAFLD)肝硬化与T2DM 有共同的危险因素和相似的发病机制,其他类型肝硬化激发的DM同“普通T2DM”的病因、临床表现及治疗方法有较多不同。
因此,熟知慢性肝病对DM的影响及机制,制定针对性的防治及随访策略,对此类病人至关重要。

慢性肝病对DM的影响
1.慢性肝病与DM发生
慢性肝病病人普遍存在糖代谢异常。文献报道,肝硬化病人30%糖耐量正常,30%~50%存在糖耐量受损(IGT),30%患DM,与之相比,普通人群IGT发病率15%,DM发病率8%。继发于肝硬化的DM称之为肝源性糖尿病(HD),1999年于日本糖尿病会议上将其归类为T2DM的一种。肝硬化患者容易出现IGT和以餐后血糖升高为主的DM。MAFLD相关肝硬化、隐源性肝硬化、丙型肝炎肝硬化、酒精性肝硬化患者DM患病率分别为 56%、51%、32% 和27%。乙型肝炎肝硬化和慢性乙型肝炎(CHB)患者DM患病率分别为22.2%和12.8%。
2. 慢性肝病对DM诊断的影响
普通DM的诊断主要依据空腹血糖(FPG)、口服葡萄糖耐量试验(OGTT) 2h血糖(2h PG)和糖化血红蛋白(HbA1c)等指标。
值得一提的是,慢性肝病患者推荐OGTT用以诊断IGT或DM,因为肝功能损伤会降低FPG和HbA1c诊断的敏感性。以FPG≥7.0 mmol/L为依据可能会漏诊20%的DM。为此,有专家建议将肝硬化患者诊断DM的FPG界值降低到5.9 mmol/L。
HbA1c同样不适合用于肝硬化患者DM的诊断。HbA1c水平与红细胞寿命呈正相关,肝硬化患者因脾功能亢进、消化道出血、造血原料缺乏等导致贫血和HbA1c降低,从而降低HbA1c诊断DM的敏感性。
利用持续葡萄糖监测(CGM)技术发现几乎所有的肝硬化患者都有IGT或DM。通过CGM技术在肝硬化患者中发现了14%被 FPG和HbA1c漏诊的DM,提示未来也许可以应用 CGM 技术来筛查肝硬化患者的DM。研究推荐采用指尖毛细血管血糖自我监测代替HbA1c检测用于肝硬化合并DM的血糖监测。

慢性肝病影响DM的机制
众多研究表明,HD患者存在高胰岛素血症及胰岛素抵抗(IR)。肝脏摄取减少、门体分流胰岛素绕过肝脏进入体循环是高胰岛素血症的2大主要原因。而肝脏灭活减少,导致胰高血糖素水平升高,也可促进高胰岛素血症。胰岛肥大,胰岛素分泌增多,进一步导致高胰岛素血症。长期高胰岛素血症引起细胞膜受体数量及与胰岛素亲和力下降,导致IR。纠正高胰岛素血症可恢复胰岛素敏感性。
研究显示,显著临床门脉高压与IR相关,可能由于存在门体分流。经颈静脉肝内门-体静脉支架分流术(TIPS)会加重高胰岛素血症,而球囊阻塞逆行曲张静脉闭塞术(BRTO)可纠正高胰岛素血症。
肝硬化非氧化性葡萄糖处理包括葡萄糖转化为糖原或脂肪,以及无氧糖酵解降低,导致IR。骨骼肌是IR发生的主要场所。肝硬化患者骨骼肌胰岛素依赖葡萄糖转运及糖原合成下降。
2. 胰岛功能障碍
肝硬化患者尽管胰岛细胞增殖,但能产生胰岛素的胰岛细胞减少。研究表明,门脉高压导致胰腺静脉扩张,胰腺组织淤血,胰岛素分泌减少。当胰岛β细胞分泌的胰岛素无法代偿IR,IGT则发展为DM。肝移植后β细胞功能恢复后DM可逆转。长期高血糖的毒性损伤导致β细胞功能障碍。肝脏对糖基化终末产物灭活减少,加重β细胞氧化应激。体内微缺氧状态也可导致β细胞功能恶化。缺氧诱导因子-1α(HIF-1α)可以调节细胞葡萄糖摄取,糖酵解酶活性和胰岛素敏感性。HIF-1α激活后可促进β细胞炎症反应,导致DM。
肝硬化原发病因不同,导致β细胞功能障碍的机制也不同。长期饮酒和血色病抑制葡萄糖激酶和加重氧化应激,从而导致β细胞凋亡和削弱葡萄糖促胰岛素分泌作用。MAFLD患者长期高血糖和高游离脂肪酸导致的糖脂毒性,导致β细胞功能障碍。慢性HCV感染通过免疫损伤和直接细胞毒性破坏胰岛功能,因此HCV比HBV感染更易并发IGT和DM。
3. 肠促胰岛素水平下降
肠促胰岛素对维持葡萄糖稳态起关键作用。肠内分泌细胞产生2种肠促胰岛素,胰高血糖素样肽-1(GLP-1)和葡萄糖依赖性促胰岛素分泌多肽,他们通过促进餐后胰岛素素分泌、抑制胰高血糖素分泌调控血糖水平。二肽基肽酶-4(DPP-4)是一种细胞膜相关的肽酶, DPP4 使 GLP-1失活, 导致IGT甚至DM。肝硬化患者肝脏DPP-4表达水平升高,血清DPP-4增多,抑制了肠促胰岛素功能,促进DM发生。
4. 肠道菌群失调
肠道菌群调控人体免疫、代谢和肠道内分泌功能。慢性肝病患者肠道微生物组成及功能发生改变,导致肠道屏障破坏,细菌易位及系统炎症。细菌内毒素(LPS)易位激活Toll样受体导致IR。肠道菌群失调导致高血氨症,以及肠菌代谢产物支链氨基酸,都和IR及DM发生相关。慢性肝病合并肌少症的病人肠道菌群中,产LPS革兰阴性菌比例增加,厚壁菌门/拟杆菌门比例下降,肠道菌群DM化。
5. 高氨血症
高氨血症和IR有关。肝脏将氨转变成尿素能力下降及门体分流可导致高血氨。肝硬化患者高氨血症与骨骼肌组织肌抑素高表达相关。肌抑素可以抑制肌肉蛋白合成,导致肝硬化病人的肌少症。高氨血症还可诱发肌肉脂肪变,降低肌肉细胞胰岛素受体表达,致使IR。
6. 肌少症
骨骼肌是餐后葡萄糖利用的主要场所,因此是胰岛素重要的靶器官。骨骼肌丢失可引起显著的IR。高氨血症,氨基酸缺乏,激素失衡,肠道菌群失调,IR和慢性炎症这些代谢因素导致肌肉蛋白更新障碍,引起肌少症。肌少症常伴随肌肉脂肪变,线粒体功能障碍,巨噬细胞浸润和炎症因子释放,导致IR和葡萄糖利用障碍。
7. 肝细胞因子及脂肪因子
肝细胞因子及脂肪因子是分别由肝脏及脂肪组织分泌的蛋白因子,用以调控系统代谢和能量动态平衡。肝细胞因子,脂肪因子和骨骼肌细胞因子相互影响调控脂肪和骨骼肌的炎症和脂肪代谢,与IR发生有关。一些肝细胞因子可直接影响胰岛素分泌,导致代谢综合征、MAFLD、T2DM的发生。肝细胞因子,比如胎球蛋白A、胎球蛋白B、视黄醇结合蛋白4、硒蛋白P和代谢综合征有关。抵抗素是一种脂肪因子,在肝硬化患者中升高。抵抗素可降低脂肪细胞、骨骼肌和肝细胞的胰岛素敏感性。

(1)各种肝病导致肝实质损害,诱发糖代谢紊乱,慢性肝病和DM互相影响导致彼此疾病进展及预后不良。肝硬化病人30%~50%存在IGT,30%罹患DM。
(2)肝硬化患者FPG及HbA1c诊断DM的敏感性下降,推荐运用OGTT诊断 IGT或DM。
(3)肝硬化病人体内胰腺β细胞功能不全,骨骼肌丢失、肠道功能失调、高血氨症等共同参与,引发胰岛素抵抗及分泌减少,导致DM发生(图1)。
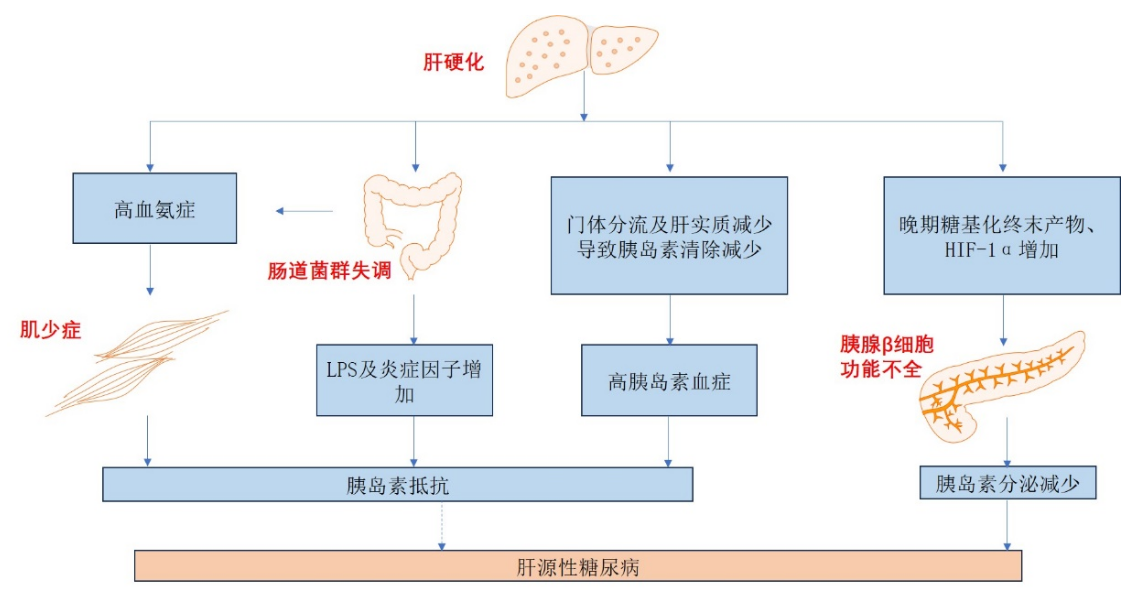
图1 肝硬化相关DM的发病机制

胡靥
医学博士,主治医师
美国Cedars-Sinai医学中心及加州大学洛杉矶分校(UCLA)博士后
长期从事消化道肿瘤的基础及临床研究,擅长代谢相关脂肪性肝病和消化道癌前病变的防治
1. 肝硬化患者的DM诊断推荐何种检测?(单选题)
A. OGTT B. FPG C. HbA1c
2. 肝源性糖尿病的发病机制包括哪些?(多选题)
A.肝脏摄取减少及门体分流导致高胰岛素血症
B.胰岛β-细胞功能障碍
C.肠促胰岛素水平下降
D.肠道菌群失调
E.肌少症
F.高氨血症
原创内容,转载须授权
查看更多