查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





过敏性肺炎(HP)是一种由吸入抗原引起的复杂且异质性高的间质性肺疾病(ILD)1,是继特发性肺纤维化(IPF)和结缔组织病相关间质性肺疾病(CTD-ILD)之后的第三种最常见的ILD2。HP患病率因气候、职业暴露、环境暴露的地区差异而不同。现有研究估计,发病率为0.3-0.9/10万人。自1700年发现HP以来,发现许多刺激性抗原与HP有关,尽管有完整的病史,但高达60%的HP患者无法确定抗原及是否暴露3,因此HP的诊断较为困难;而且有些情况下,即使避免接触抗原,疾病仍可能继续进展4。近年来,美国胸科学会/日本呼吸学会/拉丁美洲胸科学会(ATS/JRS/ALAT)和美国胸科医师学会(CHEST)分别发布了HP诊断指南,对HP的疾病定义、分类、诊断进行了规范1,但HP治疗尚无既定指南,本文将邀请安徽省胸科医院方浩徽教授为您梳理HP诊疗相关最新进展。

安徽省胸科医院PCCM科主任医师,学术主任
安徽医科大学兼职教授
安徽省临床重点学科呼吸内科学术带头人
安徽省胸科医院临床药物伦理委员会主委
中国老年医学会呼吸病学会感染委员会委员
安徽省呼吸病分会常委兼间质病学组副组长
安徽省呼吸医师分会副主任委员兼感染学组组长
安徽省全科医学会常务理事兼呼吸专委会主任委员
HP的定义和分类
HP是一种影响肺实质和小气道的炎症性和/或纤维化性疾病。它通常是由易感个体吸入显性或隐性抗原引起的免疫介导反应所致。过去根据症状持续时间将HP划分为急性、亚急性或慢性,但由于难以区分这些类别,而且这些类别与预后缺乏关联,因此这种分类方法现在被认为没有什么临床价值1。由于放射学或组织病理学检查中发现纤维化是不良预后的主要决定因素,ATS/JRS/ALAT发布的HP诊断指南提出,将患者归类为非纤维化性(单纯炎症)HP和纤维化性HP(炎症和纤维化混合或单纯纤维化)3。
HP的临床表现及预后
HP的常见症状和体征包括呼吸困难、咳嗽和吸气中期吱吱声(或哮鸣音或哮笛音)。发病可能是急性的(数天至数周内发病,偶尔伴有胸腔积液),也可能是隐匿性的(数月至数年内发病并恶化);发作可能是反复的3。
HP的自然病史具有异质性,病情可以好转,也可以出现进展,甚至因呼吸衰竭而死亡。非纤维化性HP患者如能避免持续接触诱发因素,则预后良好,有可能病情稳定或完全康复。而纤维化性HP患者,尤其是表现为UIP(普通型间质性肺炎)表型的患者,生存期则会缩短,且预后与IPF相似3,5。
部分纤维化性HP患者还会发展为进展性肺纤维化(PPF),其特征是HRCT(高分辨率计算机断层扫描)上的纤维化异常增加、肺功能恶化和早期死亡1。来自加拿大的一项前瞻性登记研究发现,高达58%的纤维化性HP患者会发展为PPF6。HP患者ILD疾病进展和死亡相关的几个危险因素已被确定(表1),应监测HP患者的疾病进展,包括定期检查症状和肺功能,并在必要时复查HRCT。
表1. 与HP患者ILD疾病进展及死亡相关的因素
注释:BAL:支气管肺泡灌洗;DLco:肺一氧化碳弥散量;FVC:用力肺活量;NSIP:非特异性间质性肺炎;UIP:普通型间质性肺炎
HP诊断
将HP与其他ILD区分开来可能具有挑战性,因为HP的临床、放射学和组织病理学特征高度可变,并且与其他ILD的特征重叠1。在对所有纤维化性ILD患者进行鉴别诊断时应考虑纤维化性HP,这尤其具有挑战性,因为高达50%的纤维化HP患者未发现可识别的暴露,而且纤维化性HP可能被误诊为IPF。非纤维化性HP通常与明确的暴露相关,较少造成诊断困境1,3。
HP的诊断需要基于临床(暴露评估)、放射学(HRCT征象)、支气管肺泡灌洗液(BALF)细胞分类中淋巴细胞增多和组织病理学(肺活检)数据进行多学科讨论(MDD)。根据CHEST指南,确定暴露且在HRCT上有典型HP征象的患者可对HP进行可靠诊断(图1)。根据ATS/JRS/ALAT指南,HP的可靠诊断还需要BALF淋巴细胞增多的证据(图2)1。
图1. 2021年CHEST指南关于HP的诊断流程
图2. 2020年ATS/JRS/ALAT指南关于HP的诊断流程
注释:*建议对潜在非纤维化性HP患者进行经支气管肺活检(TBLB)。**根据当地专业知识,建议对潜在纤维化性HP患者进行经支气管冷冻肺活检(TBLC)。***在非纤维化性HP患者中很少考虑外科肺活检(SLB)
暴露评估:
暴露评估工具包括:收集全面的临床病史(有或没有问卷调查),针对HP相关潜在抗原的IgG (血清免疫球蛋白G)检测,针对特异性抗原的吸入激发试验。ATS/JRS/ALAT指南建议使用经验证的问卷来确定潜在的暴露,而在获得经验证的问卷之前提倡临床医生采集全面的病史3。而CHEST指南建议不进行抗原特异性吸入激发试验来支持HP诊断7。目前已经报道了一些潜在的刺激性抗原和多达数百种抗原来源,可以是有机颗粒物(微生物、植物或动物蛋白、酶),也可以是无机颗粒物(化学品、药剂、金属)(表2)3,8。
表2. 抗原和来源的一些常见例子
HRCT:
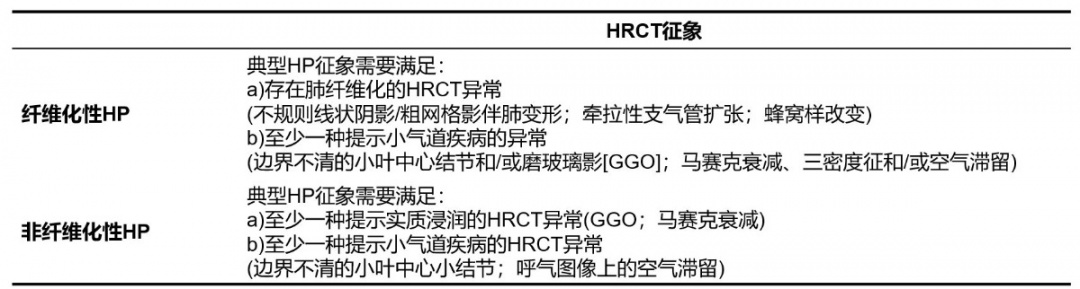
HRCT在HP的诊断和纤维化的检测中起关键作用。纤维化性HP与非纤维化性HP在HRCT上的典型HP征象不同(表3) 1,3。
BALF淋巴细胞增多:
对于疑似HP患者,BAL是检测肺泡炎的最敏感工具,健康不吸烟成人的BALF淋巴细胞百分比为10%-15%3。BALF淋巴细胞增多定义为淋巴细胞百分比>15%,在HP中很常见4。BALF淋巴细胞增多的价值很大程度上取决于检查前的HP诊断概率1。ATS/JRS/ALAT指南推荐:对于新发现ILD的患者,在进行多学科讨论之前,应先进行暴露评估、BALF淋巴细胞分析和HRCT扫描3。BALF淋巴细胞百分比>30%有助于区分非纤维化性HP与结节病以及区分纤维化性HP与IPF和结节病。而CHEST指南推荐:在考虑BAL之前,应多学科讨论暴露情况和HRCT征象,而对于有暴露史、临床背景和HP典型HRCT征象的患者,不应进行BAL7。
肺活检:
在对临床和放射学结果、暴露史和BALF淋巴细胞增多进行多学科讨论后,可确诊为HP的患者应避免进行肺活检。在疑似HP但根据现有数据无法做出可靠诊断的患者中,如果有必要,建议权衡个体患者的风险与收益决定是否进行肺组织活检。
ATS/JRS/ALAT指南建议非纤维化性HP患者应进行TBLB而不是TBLC, 而纤维化性HP患者应进行TBLC而不是TBLB3。TBLB所获取的活检标本小,非纤维化HP病变的小叶中心分布可增加检出率,但纤维化性HP检出率较低,不一定能确诊。TBLC采用冷冻探针来获取组织标本,其标本比TBLB标本大,但比手术肺活检标本小,对于弥漫性实质性肺疾病,TBLC的诊断准确度与手术肺活检接近9。ATS/JRS/ALAT和CHEST指南对非纤维化和纤维化HP的病理表现提出了相同的一般标准(表4)1。
表4. 诊断典型HP的组织病理学标准
HP管理
识别和消除刺激性抗原对于改善HP患者的预后至关重要,但在实践中可能难以实现。可征聘环境卫生学家对室内空间进行评估,并就如何减少暴露源提出建议。虽然避免接触刺激性抗原是最重要的治疗策略,但许多患者并没有确定抗原。且即使避免接触抗原,也可能会出现持续的呼吸道症状、肺功能下降和/或影像学进展,这就需要考虑使用抗炎或抗纤维化药物进行治疗4。
目前有关HP的药物治疗尚无既定方案。HP最初可能对皮质类固醇有反应,但几乎没有证据表明皮质类固醇能提供长期获益或减缓纤维化性HP的进展。且已有研究证实皮质类固醇对非纤维化性HP有效,但对纤维化性HP无效1,10。
HP患者通常接受免疫抑制剂治疗,但支持其应用的证据较差。两项回顾性研究显示:霉酚酸酯或硫唑嘌呤治疗后,DLco或FVC有所改善11,12。然而,另一项回顾性研究发现,在纤维化性HP患者中,使用硫唑嘌呤或霉酚酸酯加泼尼松治疗的患者与单独使用泼尼松的患者在肺功能下降或生存率方面没有差异1,13。
据推测,无论最初的诱因是什么,一旦ILD发生纤维化,就需要一种抑制纤维化途径的治疗来减缓其进展。然而,对于纤维化性HP患者应何时开始抗纤维化治疗,目前仍未达成共识1。
尼达尼布是一种细胞内酪氨酸激酶抑制剂,已在多个国家获批用于治疗PPF1,且已被最新的ATS/ERS/JRS/ALAT临床实践指南14推荐用于治疗PPF。随机双盲对照临床试验INBUILD研究对除IPF以外的663名PPF患者进行了研究(其中:173名[26%]患者患有纤维化性HP,在不同ILD亚型中占比最高):与安慰剂相比,尼达尼布在52周内使FVC的下降率降低了57%;且在试验期间,尼达尼布组的ILD急性加重或死亡的风险也有所降低。尽管INBUILD试验的研究设计并不针对单个ILD,但根据不同ILD诊断类型进行分层的亚组分析发现,尼达尼布在降低FVC下降率的作用及相关不良事件发生率方面在亚组间一致1,15。(图3)。
图3. INBUILD试验中除IPF以外的PPF患者52周内FVC的下降率(ml/年)
尚未在随机双盲对照试验中将吡非尼酮作为治疗HP的药物进行研究。RELIEF研究调查了尽管接受了标准治疗,但因结缔组织病、纤维化性非特异性间质性肺炎、HP或石棉肺引起的PPF患者中吡非尼酮的作用,但该研究因招募率低而提前终止。然而对纳入的127例患者(其中57例患有HP)的数据分析表明:与安慰剂相比,吡非尼酮组患者在48周内的FVC占预计值%降幅较小。
非药物干预措施,如氧疗、肺康复、肺移植、疫苗接种、支持性护理和加入患者团体,可能是PPF患者整体护理的重要组成部分。对HP常见合并症的管理,如胃食管反流病和慢性阻塞性肺疾病,也有助于改善患者的预后和生活质量1。
总结
参考文献:
1.Hamblin M, et al. Eur Respir Rev. 2022 Feb 9;31(163):210169.
2. Cottin V, et al. Eur Respir Rev. 2018 Dec 21;27(150):180076.
3. Raghu G, et al. Am J Respir Crit Care Med. 2020 Aug 1;202(3):e36-e69.
4. Barnes H, et al. Allergy. 2022 Feb;77(2):442-453.
5. Alberti ML, et al. Pulmonology. 2020 Jan-Feb;26(1):3-9.
6. Hambly N, et al. Eur Respir J. 2022 Oct 6;60(4):2102571.
7. Fernández Pérez ER, et al. Chest. 2021 Aug;160(2):e97-e156.
8. Costabel U, et al.Nat Rev Dis Primers. 2020 Aug 6;6(1):65.
9. Chami HA,et al.Ann Am Thorac Soc. 2021 Jan;18(1)148-161.
10. De Sadeleer LJ et al. J Clin Med 2018;8:14.
11. Morisset J,et al.Chest.2017 Mar;151(3):619-625.
12. Fiddler CA,et al.Clin Respir J. 2019 Dec;13(12):791-794.
13. Adegunsoye A et al. ERJ Open Res 2017;3:00016-2017.
14. Raghu G, et al.Am J Respir Crit Care Med. 2022 May 1;205(9):e18-e47.
15.Wells AU, et al. Lancet Respir Med. 2020 May;8(5):453-460.
审批号:SC-CN-14725
有效期至:2025年1月3日
仅供相关医药专业人士进行医学科学交流
↓↓↓
查看更多