查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





作者:郑州市中心医院卒中中心 张晓辉

目的:
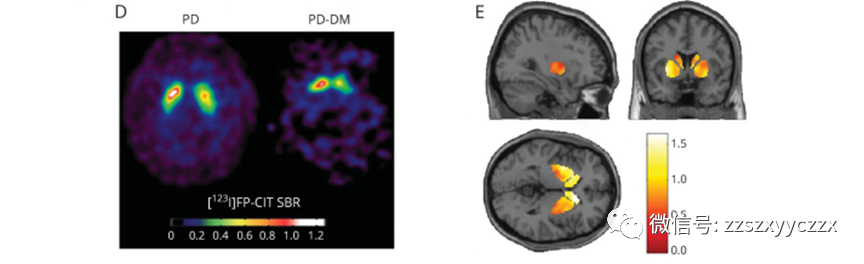
研究糖尿病(C-DM,controlswith DM)人群中是否出现帕金森样病理改变,同时评估帕金森合并糖尿病(PD-DM,PD and DM)早期未药物干预的病理改变和临床进展。
方法:
我们对25名PD-DM患者与25名PD患者、14C-DM与14名健康对照者(health control,HC)进行了比较。DM的临床诊断通过连续2次空腹测量血清葡萄糖水平>126 mL/dL确诊。通过36个月的随访,我们研究PD-DM患者是否更早出现运动障碍及认知衰退。
结果:
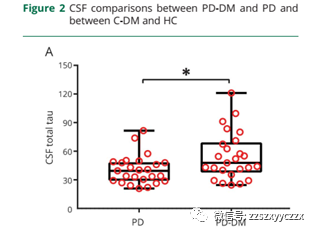
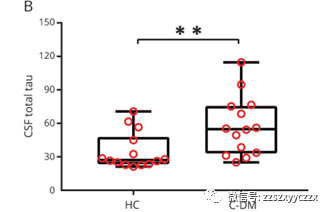
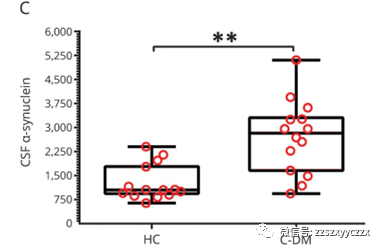
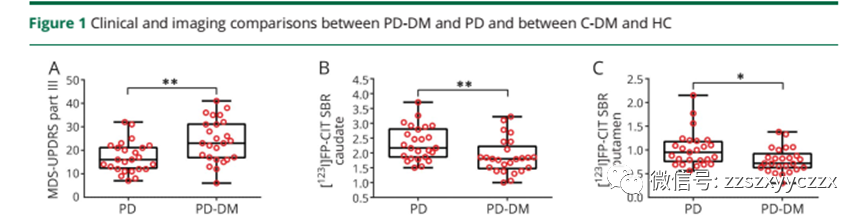
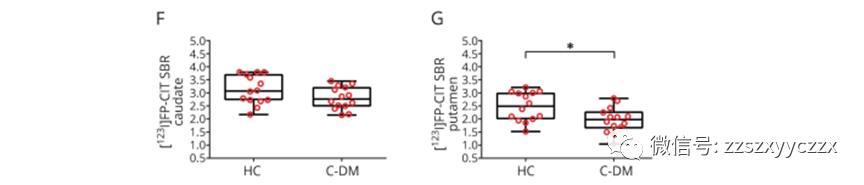
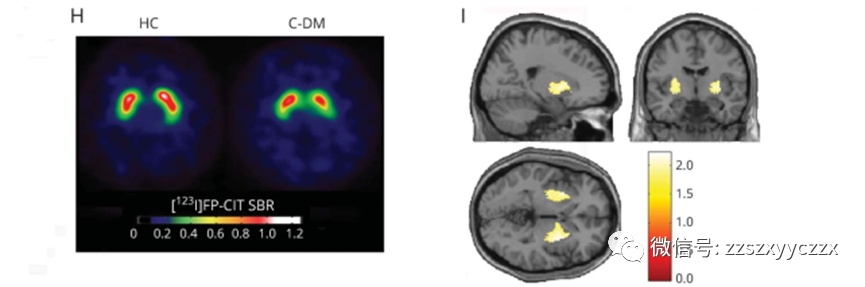
PD-DM存在较高的运动评分(P<0.01),纹状体多巴胺水平降低(P<0.05),在脑脊液中tau水平升高(P<0.05)。与HC对比,MD患者纹状体内多巴胺水平降低(P<0.05),脑脊液中tau(P<0.05)水平和α-突触核蛋白(P<0.05)升高。在PD人群比例风险回归模型发现:PD-DM患者运动障碍与认知能力下降的情况更严重。
结论:
与HC对比,DM患者可能更倾向出现帕金森样病理改变;PD-DM患者,可能加速疾病的恶化。
讨论:
我们的研究结果表明,PD-DM患者存在更加严重的运动症状,纹状体多巴胺能缺陷更突出,在疾病早期未予治疗的患者中脑脊液tau水平增加。DM是PD患者的有害因素,将会导致更快的运动障碍进展及认知功能下降;在C-DM患者中存在PD样病理改变,包括纹状体多巴胺功能缺陷、脑脊液中tau水平增加以及α-突触核蛋白升高。
在散发的PD患者早期,可以出现糖代谢异常,引起抗氧化功能降低,导致神经元减少,大脑对糖代谢紊乱。研究还发现控制糖代谢的基因与PD之间存在联系,然而这种关联的病理生理机制仍不清楚。研究表明糖尿病患者出现葡萄糖代谢失调与PD患者出现多巴胺功能障碍之间存在联系。(1)在链脲佐菌素诱导的DM大鼠模型中发现多巴胺水平减少;(2)在高脂饮食诱导的DM大鼠模型中发现多巴胺释放降低;(3)由高脂肪饮食诱发的DM大鼠模型中发现多巴胺能功能障碍;(4)给予葡萄糖的大鼠纹状体多巴胺转换减少。
临床研究还表明DM和PD之间存在病理联系:(1)在糖尿病大鼠模型大脑中发现过度磷酸化tau神经元增加;(2) 通过使用T2* 加权 MRI 序列测量,发现在高脂饮食 DM大鼠黑质铁沉积增加;(3)在α-突触核蛋白敲除小鼠模型中观察到乙醛酶-1表达增加并伴有糖基化损伤,提示葡萄糖摄取可能由α-突触核蛋白信号通路通过LPAR2/Gab1/PI3K /Akt通路调控;(4) 给予GLP-1类似物艾塞那肽可修复受损的多巴胺能细胞。


续:
帕金森病(Parkinson’s disease, PD) 和糖尿病 (diabetes mellitus, DM) 都是年龄相关的慢性疾病,但在临床特征方面,两者并不相同。PD 的主要病理改变为黑质致密部多巴胺神经元变性、α- 突触核蛋白异常聚集在细胞质内形成路易小体,临床上主要表现为肌强直、运动迟缓、静止性震颤、姿势不稳等;而 DM 主要为胰岛素分泌减少致胰岛素绝对缺乏 [称Ⅰ型糖尿病 (T1DM)] 或胰岛素抵抗致胰岛素相对缺乏 [称Ⅱ型糖尿病 (T2DM)],从而引起血糖升高,由此继发的一系列组织器官病变。越来越多的证据表明胰岛素分泌失调和 DM 可能在 PD 发病中起重要作用。
PD 和 DM 共病的可能机制
除上述机制外,有研究发现,线粒体功能障碍、内质网应激、炎症、维生素 D 缺乏、糖代谢异常、脂肪代谢异常等,都可能促进 PD 和 DM 发生或发展,但相关证据仍需进一步研究证实。
来源:郑州市中心医院卒中中心
最新指南 | 2022 AAN实践指南:症状性颅内大动脉粥样硬化性卒中预防
【PDF下载】急性脑梗死缺血半暗带临床评估和治疗中国专家共识
Neurology:中年时期进行中到剧烈运动有益于晚年的脑血管健康
查看更多