查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过






亲爱的读者朋友,您的意见对我们非常重要!为了更好地了解您的需求,提升文章内容质量,诚邀您花几分钟参与本次有奖问卷调研。参与者有机会获得精美奖品!
上期回顾

本文主要介绍指南推荐的IPMN规范化监测及干预时机,以及新近研究对于BD-IPMN的随访策略的建议,另外阐述EUS引导下化学消融、胰管镜下射频消融及化学消融对于IPMN的治疗应用及发展前景。
胰腺导管内乳头状黏液瘤(intraductal papillary mucinous neoplasm, IPMN)是一种源于胰腺导管内黏液分泌上皮细胞的乳头状增生性肿瘤,是胰腺癌的癌前病变之一。
依据受累胰管的分布,IPMN可分为三类:主胰管型IPMN(main duct IPMN,MD-IPMN)、分支胰管型IPMN(branch duct IPMN,BD-IPMN)及混合型IPMN(mix type-IPMN,MT-IPMN)。其中MD-IPMN和MT-IPMN进展为侵袭性腺癌的风险大约为50%, BD-IPMN的恶变风险为11%~30%。
2017年国际胰腺病协会(International Association of Pancreatology,IAP)福冈指南根据临床表现、实验室及影像学检查结果等将IPMN恶性危险因素分为“高危特征(high-risk stigmata,HRs)”和“担忧特征(worrisome features,WFs)”。2018年欧洲胰腺囊性肿瘤研究组(European Study Group on Cystic Tumors of the Pancreas,ESG)指南则采用绝对适应证(absolute indications,AI)和相对适应证(relative indications,RI)的手术策略。本中心曾主导编写指南,提出将IPMN患者列入胰腺癌高危人群1。
以上指南推荐的IPMN恶变征象主要通过影像学获取,较为一致的高危因素包括:囊性病变导致梗阻性黄疸,强化壁结节≥5 mm,主胰管扩张≥10 mm,细胞学检查结果可疑或阳性;担忧征象通常包括:新发胰腺炎或急性胰腺炎,囊肿直径≥3 cm,强化壁结节<5 mm,主胰管直径5~9 mm,胰管管径突然改变伴远端胰腺萎缩,淋巴结肿大,糖类抗原19-9(CA19-9)升高,囊肿直径增长速度≥5 mm/2年等。
2023年国际胰腺病协会(IAP)京都指南更新了HRs和WFs定义,并且提出,若IPMN患者存在任意1项HR,则在条件许可的情况下应考虑手术;若IPMN病人无HR,但存在任意1项WF,同时伴有下列因素之一,则在条件许可的情况下应考虑手术,包括:① 反复急性胰腺炎发作影响生活质量;② 有多重WF导致癌变风险升高;③ 年轻、适合手术者。
另外,2023年IAP版指南推荐,对于无上述因素,但存在非单发的直径≥30 mm囊肿的IPMN患者,则根据预期风险每1~6个月随访1次,一旦出现上述因素,则应手术治疗;若IPMN患者无HRs、WFs,或存在WFs但无上述因素的单发直径≥30 mm的囊肿,可行随访观察。
近期研究表明,BD-IPMN的进展发生率随着诊断时的初始大小而变化。对于直径<10 mm的BD-IPMN,进展为WF的比例为4.8%,中位时间为54个月;对于10 mm~20 mm的病变,比例为10%,中位时间为55个月;对于直径20m m~30 mm的BD-IPMN,比例为48.8%,中位时间为23个月。因此,2023年新版IPMN指南推荐基于3种不同囊肿大小分层的BD-IPMN随访方案,即:① BD-IPMN直径<20 mm者,首次6个月,如果稳定,之后每18个月随访1次;② BD-IPMN直径20 mm~30 mm者,前2次随访每隔6个月1次,如果稳定,之后每12个月随访1次;③ BD-IPMN直径≥30 mm者,每6个月随访1次2。
对于无变化且直径小的BD-IPMN患者,其长期随访是否必要,有研究提出,如BD-IPMN 5年间无变化且直径<20 mm,或75岁及以上人群囊肿直径<30 mm,或65岁以上人群囊肿直径<15 mm,在5年随访期间内囊肿稳定,则可终止随访3。
传统的外科手术虽然能够有效切除病灶,但创伤大、并发症多。近年来,EUS引导下的化学消融技术逐渐成为胰腺囊性肿瘤治疗的热点。
本中心自2014年开始尝试EUS引导下无水酒精消融治疗胰腺囊性肿瘤,结果发现该操作安全可行4。研究表明,酒精联合紫杉醇的消融效果优于单纯酒精消融,完全缓解率可提高至50%~70%,且并发症发生率较低。另外,吉西他滨联合紫杉醇的化学消融方案在治疗胰腺囊性肿瘤中表现出更高的完全缓解率(超过50%),且并发症发生率仅为2.66%,这样的消融方案对于与胰管相通的BD-IPMN更加的安全。近期研究表明,超声内镜引导下化学消融相较于外科手术具有更好的长期疗效及安全性5。本中心近期利用EUS引导下注射吉西他滨+紫杉醇化学消融治疗8例BD-IPMN,术后仅2例患者发生轻症胰腺炎,其余患者均未发生严重不良事件,术后复查影像学提示病灶较前有缩小趋势,还有待长期随访结果。
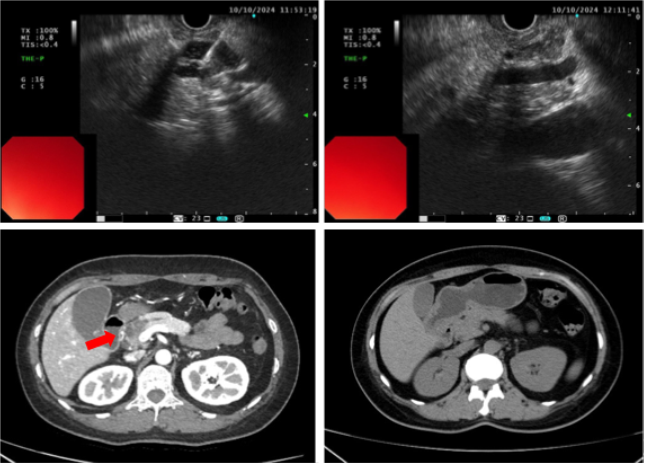
图1:EUS引导下紫杉醇+吉西他滨化学消融治疗一例BD-IPMN:左上:EUS-FNA下注射消融药物;右上:注射药物后;左下:术后3天影像;左下:术后1月影像。
不宜或不愿接受外科手术的主胰管型IPMN,胰管镜下射频消融(Radiofrequency ablation,RFA)可以作为一种新兴的姑息治疗手段。
既往研究表明,射频消融对胰腺囊性肿瘤完全缓解率在33%~65%。2018年,法国COCHIN医院首次报道了一例主胰管型IPMN的射频消融治疗,并成功置入7-Fr胰管支架,术后3个月随访未见肿瘤复发,胰液引流顺畅。
2024年3月,本中心报道了一例直接胰管镜下活检及胰管内射频消融诊治混合型胰腺导管内乳头状黏液瘤病例,该患者虽有手术指征,但患者高龄难以耐受外科手术,患者接受了累计3次胰管镜下胰管管腔内RFA姑息性治疗,术后无明显并发症出现,且未再发作胰腺炎,获得了良好的临床效果(见下图)6。
最新一项单中心回顾性研究纳入分析了14例接受胰管镜下RFA的MD-IPMN患者,结果表明,胰管镜下RFA对MD-IPMN进行局部治疗,在预防病变进展、缓解胰腺炎症状方面效果较好,且术后无严重并发症7。
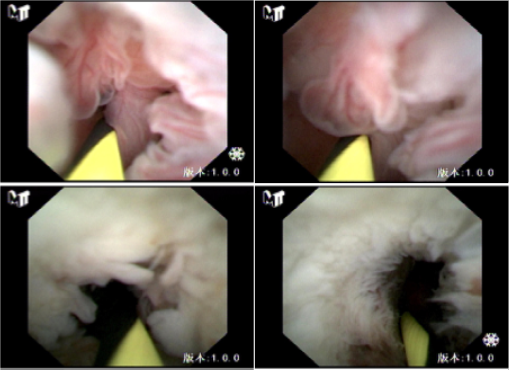
图2:混合型IPMN直接胰管镜下所见及射频消融治疗
针对IPMN,经口胰管镜(peroral pancreatoscopy, POP)在确定分型、位置、范围,改变临床决策、决定手术范围等方面发挥了重要作用。
本中心近期创新性地尝试在胰管镜直视下注射吉西他滨+紫杉醇化学消融治疗了6例IPMN,术后仅1例患者发生胰腺炎,其余患者均未发生严重不良事件。但针对此内镜下治疗手段,我们还需进一步开发更有效的消融装置来验证长期疗效。
虽然目前国际指南推荐,具有壁结节、胰管显著扩张、CA19-9升高、囊壁增厚伴强化等高危特征的IPMN均应进行手术切除,然而,报道显示,约二分之一的患者术后病理结果仅为低级别上皮内瘤变,这表明当前指南的预测准确性尚存局限,可能导致过度手术治疗。鉴于胰腺手术的高创伤性、并发症频发及高病死率,探索内镜下IPMN更精准的风险等级诊断及微创治疗仍是未来研究重点,而基于EUS、POP对囊液、胰液、活检病理等层面的分子诊断在IPMN中发挥的诊断作用也有待进一步探究。
1.IPMN的诊疗应结合影像特征、肿瘤标志物及个体状况,实施动态随访和精准干预。指南推荐的IPMN恶变征象主要通过影像学获取,较为一致的危险因素包括主胰管扩张≥10 mm、存在实性成分或强化的壁结节及梗阻性黄疸等。
2.内镜消融技术为高龄或不宜手术患者提供了可行的微创治疗选择,未来发展方向聚焦于风险精准评估与靶向治疗。
1. 关于主胰管型IPMN(MD-IPMN)以下哪项为其绝对手术指征?
A. 囊肿直径 ≥ 20 mm
B. 囊肿生长速度 > 2 mm/年
C. 主胰管扩张 ≥ 10 mm
D. CA19-9 正常但囊肿多发
2. 以下哪项是目前研究中EUS引导下化学消融最常用的药物组合?
A. 酒精 + 顺铂
D. 酒精单药

鼓楼领学⑧| “等待还是切除?”——主胰管型IPMN的内镜监测以及外科干预时机
作者:南京鼓楼医院 聂双
1. EUS引导下消融治疗PCNs的方式包括哪些?
A. 化学消融 B. 射频消融 C. 冷冻消融 D. 光动力消融
答案:A、B、C
2. EUS引导下化学消融治疗PCNs的适应证除外哪项?
A. 单囊或少囊的黏液性囊性肿瘤
B. 直径<1cm C. 直径>3cm
D. 不能耐受或拒绝外科手术
答案:B

查看更多